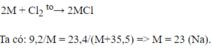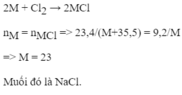cho 1 luồng khí có dư tác dụng với 9,2g kim loại hóa trị I sinh ra 23,4g muối clorua . Xác định kim loại

Những câu hỏi liên quan
cho luồng khí CLo dư tác dụng vs 9,2g Kim loại sinh ra 23,4g một kim loại. xác định công thức hóa học của muối
Đặt M là KHHH của kim loại hoá trị I.
PTHH: 2M + Cl2 → 2MCl
2M(g) (2M + 71)g
9,2g 23,4g
Ta có: 23,4 x 2M = 9,2(2M + 71)
Suy ra: M = 23.
Kim loại có khối lượng nguyên tử bằng 23 là Na.
Vậy muối thu được là: NaCl
Đúng 1
Bình luận (0)
Cho 9,2g 1 kim loại A chưa rõ hóa trị tác dụng với khí Clo dư, sau phản ứng tạo thành 23,4g muối clorua của kim loại đó. XĐ tên kim loại A
Gọi hóa trị của kim loại A là n
\(2A + nCl_2 \xrightarrow{t^o} 2ACl_n\)
Theo PTHH :
\(n_A = n_{ACl_n}\)
⇔ \(\dfrac{9,2}{A} = \dfrac{23,4}{A+35,5n}\)
⇔ A = 23n
Với n = 1 thì A = 23(Na)
Vậy kim loai A là Natri.
Đúng 3
Bình luận (0)
Cho luồng khí clo (dư) tác dụng với 9,2g kim loại hóa trị I, tạo ra 23,4 g muối. Xác định tên kim loại (Na=23, Ag=108, Li=7, K=39, Cl=35,5).
Cho một luồng khí clo dư tác dụng với 9,2g kim loại sinh ra 23,4g muối kim loại hoá trị I. Hãy xác định kim loại hoá trị I và muối kim loại đó
Giải
Đặt M là KHHH của kim loại hoá trị I.
PTHH: 2M + Cl2 → 2MCl
2M(g) (2M + 71)g
9,2g 23,4g
Ta có: 23,4 x 2M = 9,2(2M + 71)
Suy ra: M = 23.
Kim loại có khối lượng nguyên tử bằng 23 là Na.
Vậy muối thu được là: NaCl.
Bài này trên lp mk hc rồi,bn cứ yên tâm đi nha ![]()
Đúng 0
Bình luận (0)
Cho 9,2g 1 kim loại M tác dụng với khí Clo dư thu được 23,4g muối xác định kim loại đem dùng
PTHH : 2A+ Cl2 →→ 2ACl
Áp dụng bảo toàn khối lượng ta có :
mCl2= 23,4-9,2 =14,2g
nCl2=14,2 :35,5x2 0,2 mol
⇒nA⇒nA =0,4 mol
n.M=m ⇒⇒ M=9,2 :0,4 =23 ⇒⇒ A Là Na
Đúng 0
Bình luận (0)
Cho luống khí clo dư tác dụng với 9,2 gam kim loại sinh ra 23,4g muối kim loại hóa trị I. Xác định công thức hóa học của muối đó (Na=23, Ag=108, Li=7, K=39, Cl=35,5).
Cho 9,2g một kim loại A ( hóa trị từ I đến III) phản ứng với khí Clo dư tạo thành 23,4g muối. Hãy xác định kim loại A.
Cho một luồng khí clo dư tác dụng với 9,2 gam kim loại sinh ra 23,4 gam muối của kim loại có hoá trị I. Hãy xác định tên của kim loại.
- Gọi kí hiệu và nguyên tử khối của kim loại là M.
Phương trình hoá học :
2M + Cl 2 → 2MCl
9,2 x 2(M + 35,5) = 2M x 23,4
653,2 = 28,4M
M = 23. Vậy kim loại M là kim loại natri (Na).
Đúng 2
Bình luận (0)
Cho 1 lượng khí Clo dư tác dụng với 9,2g kim loại sinh ra 23,4g muối kim loại hóa trị I . Hãy xác định của kim loại I và muối kim loại đó
Gọi a là số mol khí Clo phản ứng
Phương trình phản ứng
\(Cl_2+2X\rightarrow2XCl\)
a------>2a------->2a
.........\(\dfrac{9,2}{M_X}\)......\(\dfrac{23,4}{M_X+35,5}\)
Từ phương trình ta thấy số mol của Kim loại và muối bằng nhau nên:
=> 9,2MX + 326,6 = 23,4MX
=> 326,6 = 14,2MX
=> MX =23 ( là kim loại Na )
Vậy kim loại đó là Natri
Muối của kim loại là NaCl
Đúng 0
Bình luận (0)
Giải:
Gọi kim loại hóa trị I là A
PTHH: 2A + Cl2 ----> 2ACl
Theo định luật bảo toàn khối lượng:
mA + m\(Cl_2\)= m\(ACl\)
=> m\(Cl_2\)= \(m_{ACl}-m_A\)= \(23,4-9,2=14,2\left(gam\right)\)
=> n\(Cl_2\) = \(\dfrac{14,2}{71}=0,2\left(mol\right)\)
Theo PTHH: nA= 2n\(Cl_2\) = 2.0,2 = 0,4 (mol)
MA = \(\dfrac{9,2}{0,4}\)= 23 (g/mol)
=> Kim loại hóa trị I là: Na
=> Muối của kim loại là: NaCl
Đúng 0
Bình luận (0)
- Gọi kim loại hóa trị I cần tìm là A.
PTHH: 2A+ Cl2 (dư) -> 2ACl
Ta có: \(n_A=\dfrac{9,2}{M_A};n_{ACl}=\dfrac{23,4}{M_A+35,5}\)
Theo PTHH \(n_A=n_{ACl}\\ < =>\dfrac{9,2}{M_A}=\dfrac{23,4}{M_A+35,5}\\ < =>9,2.\left(M_A+35,5\right)=23,4M_A\\ < =>9,2M_A+326,6=23,4M_A\\ < =>326,6=23,4M_A-9,2M_A\\ < =>326,6=14,2M_A\\ =>M_A=\dfrac{326,6}{14,2}=23\left(\dfrac{g}{mol}\right)\)
=>Kim loại A(I) cần tìm là natri (Na=23)
=> CTHH của muối : NaCl (tên: natri clorua hay muối ăn).
Đúng 0
Bình luận (0)
Xem thêm câu trả lời