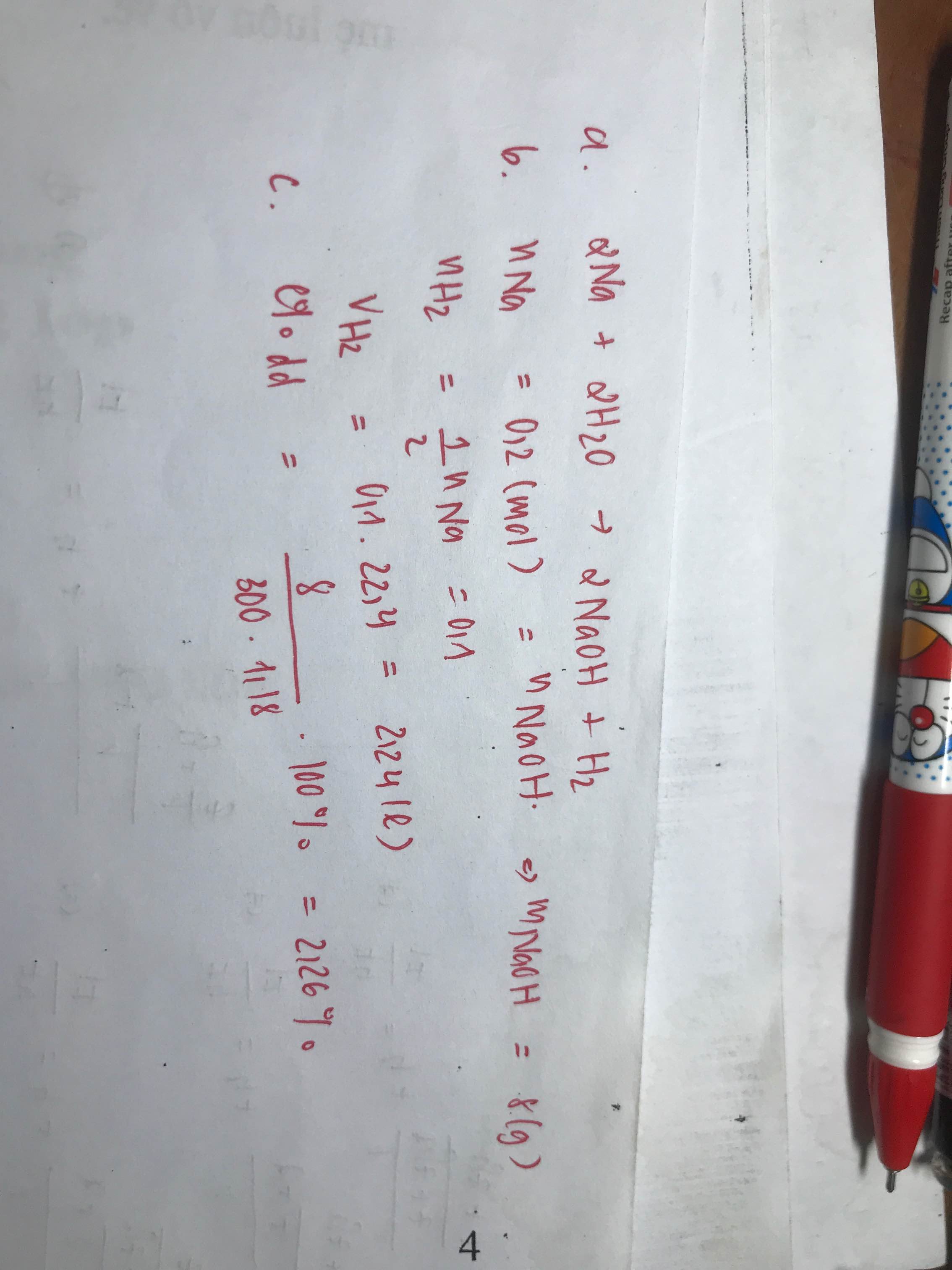hoà tan hoàn toàn 4,6g na vào h2o được 300ml dung dịch tính thể tích khí ở đktc

Những câu hỏi liên quan
Hoà tan hoàn toàn 7,2g kim loại magie vào 300ml dung dịch HCl thu được V lít khí H2 ở đktc 1. Viết PTHH 2. Tính nồng độ mol dung dịch HCl đã dùng 3. Tính thể tích H2 sinh ra ở đktc
\(1,n_{Mg}=\dfrac{7,2}{24}=0,3\left(mol\right)\)
PTHH: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
0,3---->0,6------------------>0,3
\(2,C_{M\left(HCl\right)}=\dfrac{0,6}{0,3}=2M\\ 3,V_{H_2}=0,3.22,4=6,72\left(l\right)\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 1,68 lít khí CH4 thu được thể tích lít CO2 ở ĐKTC Hoà tan 2,3(g)Na vào nước thu được dung dịch A a)Viết phương trình b)Tính m dung dịch A c)Cho VCO2 hấp thụ vào dung dịch A sau phản ứng thu được 250ml dung dịch B.Tính Cm dung dịch B
Hoà tan hoàn toàn 2.74 gam kim loại M vào 2.0 lit H2O dư, thu được dung dịch x và 224 ml khí y ở đktc kim loại M là
K
Na
Ba
Ca
Xem chi tiết
Theo gt ta có: $n_{H_2}=0,01(mol)$
Bảo toàn e ta có: $n_{M}=\frac{0,02}{n}(mol)$
$\Rightarrow M_{M}=137n$
Bạn xem lại đề nhé hình như mol H2 phải gấp đôi nữa
Đúng 2
Bình luận (0)
Hoà tan hoàn toàn 16,25 gam Zn vào dung dịch HCl loãng, dư. Tính thể tích khí H2 thu được sau phản ứng (ở đktc). (Biết Zn=65)
\(n_{Zn}=\dfrac{16,25}{65}=0,25\left(mol\right)\\ Zn+2HCl\rightarrow ZnCl_2+H_2\\ n_{H_2}=n_{Zn}=0,25\left(mol\right)\\ V_{H_2\left(đktc\right)}=0,25.22,4=5,6\left(l\right)\)
Đúng 1
Bình luận (0)
Zn + 2HCl -> ZnCl2 + H2
0.25 0.25
nZn = 0.25 mol
\(V_{H2}=0.25\times22.4=5.6l\)
Đúng 2
Bình luận (0)
Zn + 2HCl \(\rightarrow\) ZnCl2 + H2
\(n_{Zn}=\dfrac{16,25}{65}=0,25mol\)
\(n_{H_2}=0,25mol\\ V_{H_2}=0,25.22,4=5,6l\)
Đúng 1
Bình luận (0)
Hoà tan 13gam Zn vào 300ml dung dịch H2SO4 thu được dung dịch A và V lít khí H2 ở đktc , tính V và nồng độ mol/lít của dunh dịch A , biết thể tích thay đổi không đáng kể
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PTHH: Zn + H2SO4 --> ZnSO4 + H2
_____0,2---->0,2------>0,2----->0,2
VH2 = 0,2.22,4 = 4,48(l)
\(C_{M\left(ZnSO_4\right)}=\dfrac{0,2}{0,3}=0,667M\)
Đúng 0
Bình luận (0)
Hoà tan hoàn toàn 4,8g Mg vào dung dịch HCL 1M. a/ Thể tích dung dịch HCl. b/ Thể tích khí (đktc). c/ Tính nồng độ mol muối sau pứ
Ta có: \(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
a, \(n_{HCl}=2n_{Mg}=0,4\left(mol\right)\Rightarrow V_{ddHCl}=\dfrac{0,4}{1}=0,4\left(l\right)\)
b, \(n_{H_2}=n_{Mg}=0,2\left(mol\right)\) \(\Rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)\)
c, \(n_{MgCl_2}=n_{Mg}=0,2\left(mol\right)\Rightarrow C_{M_{MgCl_2}}=\dfrac{0,2}{0,4}=0,5\left(M\right)\)
Đúng 2
Bình luận (5)
Cho một mẩu Na hoà tan hoàn toàn vào nước sau phản ứng thu được dung dịch có chứa 8 gam NaOH. Khối lượng của Na đã phản ứng và thể tích khí H2 (đktc) đã sinh ra sau phản ứng lần lượt là:
2Na+2H2o->2NaOH+H2
0,2------------------0,2----0,1
n NaOH=0,2 mol
=>m Na=0,2.23=4,6g
=>VH2=0,1.22,4=2,24l
Đúng 3
Bình luận (0)
\(n_{NaOH}=\dfrac{8}{40}=0,2\left(mol\right)\)
PTHH: 2Na + 2H2O ---> 2NaOH + H2
0,2 0,2 0,1
\(\rightarrow\left\{{}\begin{matrix}m_{Na}=0,2.23=4,6\left(g\right)\\V_{H_2}=0,1.22,4=2,24\left(l\right)\end{matrix}\right.\)
Đúng 0
Bình luận (0)
PTHH: 2Na+2H2O→2NaOH+H2↑
nNaOH=mNaOH/MNaOH=8/40=0,2(mol)
Theo PTHH ta thấy: nNa=nNaOH=0,2mol
⇒mNa=0,2.23=4,6 gam
Theo PTHH ta cũng thấy:
nH2=1/2.nNaOH=1/2.0,2=0,1 mol
=> VH2= 0,1. 22,4= 2,24(l)
Vậy : mNa=4,6gam; VH2=2,24l
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 4,6g Natri vào nước thu được 300ml dd NaOH
a. Viết phương trình của phản ứng
b. Tính thể tích khí hidro tạo thành ở đktc
c. Tính nồng độ % của dd NaOH thu đc sau phản ứng
\(n_{Na}=\dfrac{4,6}{23}=0,2mol\)
\(2Na+2H_2O\rightarrow2NaOH+H_2\)
0,2 0,2 0,2 0,1
\(V_{H_2}=0,1\cdot22,4=2,24l\)
\(m_{NaOH}=0,2\cdot40=8g\)
\(m_{ddNaOH}=4,6+0,2\cdot18-0,1\cdot2=8g\)
\(\Rightarrow C\%=\dfrac{m_{NaOH}}{m_{ddNaOH}}\cdot100\%=\dfrac{8}{8}\cdot100\%=100\%???\)
Sửa đề: Tính nồng độ mol của dung dịch NaOH???
\(C_{M_{NaOH}}=\dfrac{0,2}{0,3}=\dfrac{2}{3}M\)
Đúng 4
Bình luận (0)
vì đề không cho \(D_{NaOH}=???\) nên không tính được dung dịch NaOH
Đúng 1
Bình luận (1)
Xem thêm câu trả lời
Hoà tan hoàn toàn 16.25gam kim loại M(chưa rõ hoá trị) vào dung dịch axit HCL. Khi phản ứng kết thúc thu được 5.6 lít khí hiđrô (ở đktc). a) Xác định kim loại M. b) Tính thể tích dung dịch HCL 0,2M cần dùng để hoà tan hết lượng kim loại này.
a) Gọi Kl cần tìm là X có hóa trị chưa biết là n
2X+ 2nHCl = 2XCln+ nH2
Có nH2=0,25 mol --> nX= 0,5/n mol ---> mX=0,5.MX/n=16,25 --> MX=32,5n
n=1 => MX=32,5( không có Kl nào tm)
n=2 => MX=65( Zn)
b) nHCl= 2nH2=2.0,25=0,5 mol
==> VddHCl cần = 0,5/0,2=2,5 lit
Đúng 0
Bình luận (0)