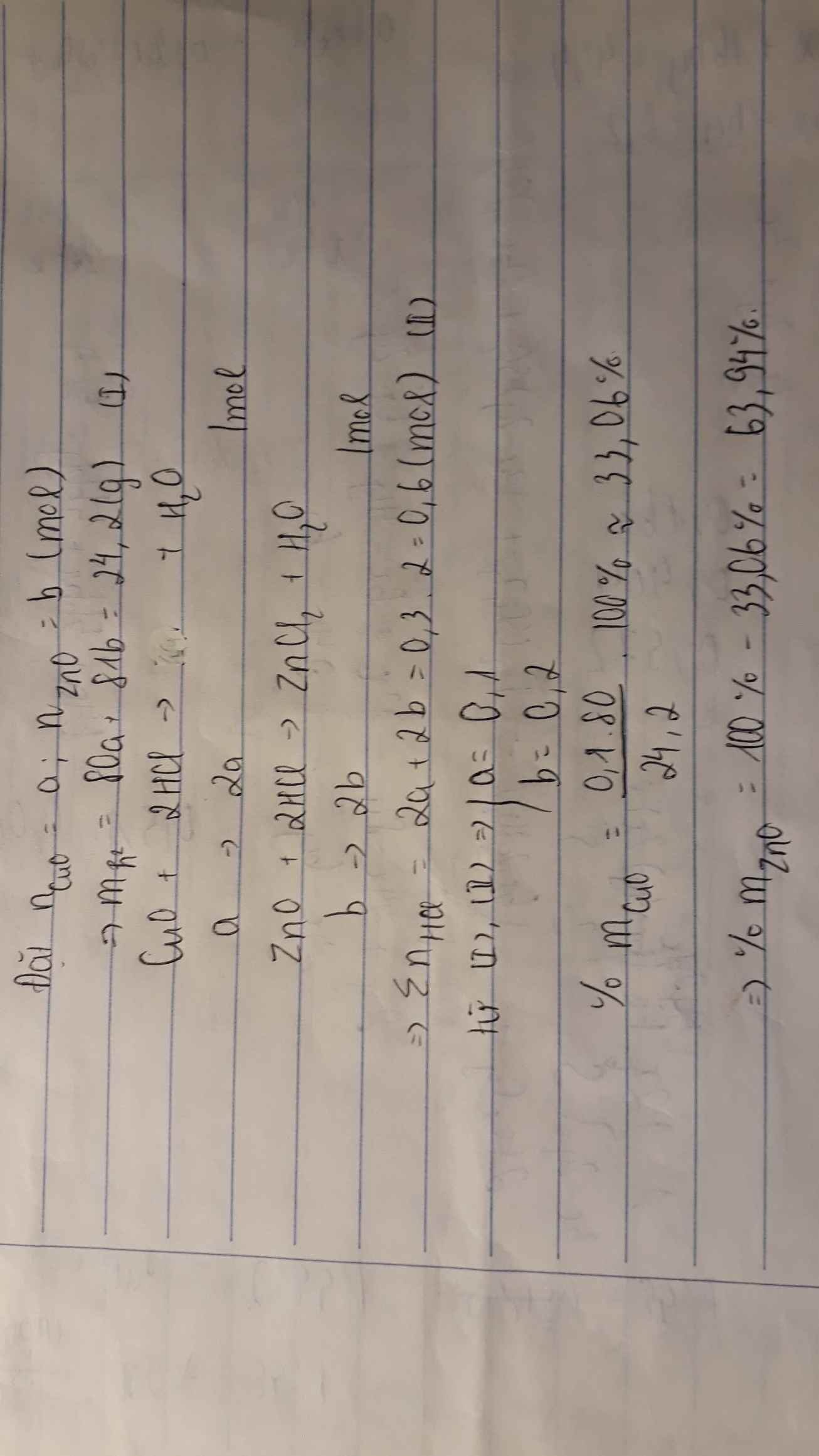Hòa tan 12,1 gam hỗn hợp gồm CuO và ZnO thì cần 100ml dung dịch HCl 3M
a, Viết PTHH xảy ra
b, Tính thành phần % theo khối lượng của mỗi oxit trong hỗn hợp
c, Tính khối lượng dung dịch H2SO4 nồng độ 20% để hòa tan hoàn toàn lượng hỗn hợp oxit trên

Những câu hỏi liên quan
Hòa tan 24,2 gam hỗn hợp gồm bột CuO và ZnO cần 300ml dung dịch HCl 2M.
a. Viết các PTHH.
b. Tính phần trăm theo khối lượng của mỗi oxit trong hỗn hợp ban đầu.
c. Hãy tính khối lượng dung dịch H2SO4 nồng độ 20% để hòa tan hoàn toàn hỗn hợp các oxit trên
Hòa tan 24,2 gam hỗn hợp gồm bột CuO và ZnO cần 300ml dung dịch HCl 2M.
a. Viết các PTHH.
b. Tính phần trăm theo khối lượng của mỗi oxit trong hỗn hợp ban đầu.
c. Hãy tính khối lượng dung dịch H2SO4 nồng độ 20% để hòa tan hoàn toàn hỗn hợp các oxit trên
Đổi 300ml = 0,3 lít
Ta có: \(n_{HCl}=2.0,3=0,6\left(mol\right)\)
a. PTHH:
CuO + 2HCl ---> CuCl2 + H2O (1)
ZnO + 2HCl ---> ZnCl2 + H2O (2)
b. Gọi x, y lần lượt là số mol của CuO và ZnO
Theo PT(1): \(n_{HCl}=2.n_{CuO}=2x\left(mol\right)\)
Theo PT(2): \(n_{HCl}=2.n_{ZnO}=2y\left(mol\right)\)
=> 2x + 2y = 0,6 (*)
Theo đề, ta có: 80x + 81y = 24,2 (**)
Từ (*) và (**), ta có HPT:
\(\left\{{}\begin{matrix}2x+2y=0,6\\80x+81y=24,2\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
=> \(m_{CuO}=0,1.80=8\left(g\right)\)
=> \(\%_{m_{CuO}}=\dfrac{8}{24,2}.100\%=33,06\%\)
\(\%_{m_{Zn}}=100\%-33,06\%=66,94\%\)
c. PTHH:
CuO + H2SO4 ---> CuSO4 + H2O (3)
ZnO + H2SO4 ---> ZnSO4 + H2O (4)
Theo PT(3): \(n_{H_2SO_4}=n_{CuO}=0,1\left(mol\right)\)
Theo PT(4): \(n_{H_2SO_4}=n_{ZnO}=0,2\left(mol\right)\)
=> \(n_{H_2SO_4}=0,1+0,2=0,3\left(mol\right)\)
=> \(m_{H_2SO_4}=0,3.98=29,4\left(g\right)\)
Ta có: \(C_{\%_{H_2SO_4}}=\dfrac{29,4}{m_{dd_{H_2SO_4}}}.100\%=20\%\)
=> \(m_{dd_{H_2SO_4}}=147\left(g\right)\)
Đúng 2
Bình luận (0)
Để hòa tan hoàn toàn 12,1 gam hỗn hợp bột CuO và ZnO cần 100ml dung dịch axit clohiric 3M.
b. tính khối lượng mỗi oxit trong hỗn hợp ban đầu.
c. Tính khối lượng dung dịch H2SO4 nồng độ 20% đủ để hòa tan hoàn toàn hỗn hợp oxit trên
mấy bạn giải thích rõ dùm mình đoạn sao ra x= 0.05 và y= 0.1 với ạ
nếu bn đoạn trên bn hiểu rồi thì thôi nhe
Ta có: \(\left\{{}\begin{matrix}80x+81y=12,1\\2x+2y=0,3\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}80x+81y=12,1\\80x+80y=12\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}y=0,1\\2x+2y=0,3\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}y=0,1\\x=0,05\end{matrix}\right.\)
Giống như giải hệ phương trình thôi bn
Đúng 0
Bình luận (0)
a,\(n_{HCl}=0,1.3=0,3\left(mol\right)\)
PTHH: CuO + 2HCl → CuCl2 + H2O
Mol: x 2x
PTHH: ZnO + 2HCl → ZnCl2 + H2O
Mol: y 2y
Ta có: \(\left\{{}\begin{matrix}80x+81y=12,1\\2x+2y=0,3\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,05\\y=0,1\end{matrix}\right.\)
\(m_{CuO}=0,05.80=4\left(g\right);m_{ZnO}=12,1-4=8,1\left(g\right)\)
c,
PTHH: CuO + H2SO4 → CuSO4 + H2O
Mol: 0,05 0,05
PTHH: ZnO + H2SO4 → ZnSO4 + H2O
Mol: 0,1 0,1
\(m_{ddH_2SO_4}=\dfrac{\left(0,05+0,1\right).98.100}{20}=73,5\left(g\right)\)
Đúng 1
Bình luận (0)
Hòa tan hòa toàn 12,1 gam hỗn hợp gồm CuO vào ZnO cần 100ml dung dịch HCl. Biết tỉ lệ số mol của 2 oxit lần lượt là 1:2
a) Tính phần trăm theo khối lượng của mỗi oxit trong hỗn hợp ban đầu
b) Tính nồng độ mol HCl đã dùng
a) Gọi x là số mol CuO => 2x là số mol ZnO
Ta có : 80x + 81.2x =12,1
=> x=0,05
=> \(\%m_{CuO}=\dfrac{0,05.80}{12,1}.100=33,06\%\);\(\%m_{ZnO}=66,94\%\)
b)CuO + 2HCl --------> CuCl2 + H2O
ZnO + 2HCl --------> ZnCl2 + H2O
\(CM_{HCl}=\dfrac{0,05.2+0,1.2}{0,1}=3M\)
Đúng 2
Bình luận (0)
Hòa tan hoàn toàn 12,1g hỗn hợp bột CuO và ZnO cần 100ml dd HCl 3M
a) Tính phần trăm theo khối lượng của mỗi oxit trong hh ban đầu.
b) Tính khối lượng dung dịch H2SO4 20% để hòa tan hoàn toàn hh oxit trên.
Pt : CuO + 2HCl → CuCl2 + H2O\(|\)
1 2 1 1
a 2a
ZnO + 2HCl → ZnCl2 + H2O\(|\)
1 2 1 1
b 2b
a) Gọi a là số mol của CuO
b là số mol của ZnO
Theo đề ta có : mCuO + mZnO = 12,1 (g)
⇒ nCuO . MCuO + nZnO . MZnO = 12,1 g
80a + 81b = 12,1g (1)
100ml= 0,1l
Số mol của dung dịch axit clohidric
CMHCl = \(\dfrac{n}{V}\Rightarrow n=C_M.V=3.0,1=0,3\left(mol\right)\)
⇒ 2a + 2b = 0,3 (2)
Từ (1),(2) ta có hệ phương trình :
80a + 81b = 12,1
2a + 2b = 0,3
⇒ \(\left\{{}\begin{matrix}a=0,05\\b=0,1\end{matrix}\right.\)
Khối lượng của đồng (II) oxit
mCuO = nCuO . MCuO
= 0,05 . 80
= 4 (g)
Khối lượng của kẽm oxit
mZnO = nZnO . MZnO
= 0,1. 81
= 8,1 (g)
0/0CuO = \(\dfrac{m_{CnO}.100}{m_{hh}}=\dfrac{4.100}{12,1}=33,06\)0/0
0/0ZnO = \(\dfrac{m_{ZnO}.100}{m_{hh}}=\dfrac{8,1.100}{12,1}=66,94\)0/0
b) Pt : CuO + H2SO4 → CuSO4 + H2O\(|\)
1 1 1 1
0,05 0,05
ZnO + H2SO4 → ZnSO4 + H2O\(|\)
1 1 1 1
0,1 0,1
Số mol tổng của axit sunfuric
nH2SO4 = 0,05 + 0,1
= 0,15 (mol)
Khối lượng của axit sunfuric
mH2SO4 = nH2SO4 . MH2SO4
= 0,15 . 98
= 14,7 (g)
Khối lượng của dung dịch axit sunfuirc cần dùng
C0/0H2SO4 = \(\dfrac{m_{ct}.100}{m_{dd}}\Rightarrow m_{dd}=\dfrac{m_{ct}.100}{C}=\dfrac{14,7.100}{20}=73,5\left(g\right)\)
Chúc bạn học tốt
Đúng 1
Bình luận (1)
Gọi x,y lần lượt là số mol của CuO và ZnO
Số mol HCl
N=Cm×V= 3×0,1=0,3mol
Lập PTHH
CuO + 2HCl --> CuCl2 + H2O
x-->2x
ZnO + 2HCl --> ZnCl2 + H2O
y--> 2y
Theo PTPƯ ta có
2x+2y=0.3 (1)
Theo đề bài ta có
mCuO+mZnO =80x + 81y= 12,1g (2)
Từ (1),(2) =>
80x+81y=12,1g=>x=0.05 mol
2x+2y=0,3=>y=0,1mol
a) %CuO=0,05×80×100/12,1=33,06%
%ZnO=0,1×80×100/12,1=66,94%
b)CuO+H2SO4-->CuSO4 +H2O
0,05---> 0,05
ZnO+H2SO4-->ZnSO4+H2O
0,1--->0,1
nH2SO4=0,05+0,1=0,15mol
mH2SO4=0,15×98=14,7g
mddH2SO4 =14,7:20=73,5g
Có j sai đừng trách nha
Đúng 0
Bình luận (1)
Hòa tan 24,2 gam hỗn hợp bột CuO và ZnO cần 300ml dung dịch HCL 2M
a. Viết các PTHH
b. Tính phần trăng theo khối lược của mỗi oxit trong hỗn hợp ban đầu
c. Hãy tính khối lượng dung dịch H2SO4 nồng độ 20% để hòa tan hoàn toàn hỗn hợp các oxit trên
200 ml =0,2 l
nHCl=0,2.3=0,6(mol)
CuO+2HCl−>CuCl2+H2O(1)
a 2a (mol)
ZnO+2HCl−>ZnCl2+H2O(2)
b 2b (mol)
ta có
{80a+81b=24,2
2a+2b=0,6{
giả ra ta được a =0,1 (mol)
=> mCuO=0,1.80=8(g)
thành phần % theo khối lượng mỗi oxit trong hỗn hợp ban đầu là
%CuO = 824,2.100%=33,06%
%ZnO= 100% - 33,06% = 66,94%
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 12,1g hỗn hợp bột CuO và ZnO cần 100ml dung dịch HCl 3M.
a, Viết các PTHH
b, Tính phần trăm theo khối lượng của mỗi oxit trong hỗn hợp ban đầu
c, Hãy tính khối lượng dung dịch H2SO4 nồng độ 20% để hòa tan hoàn toàn hỗn hợp các oxit trên
Các bạn giải giúp mình phần c nhé! Phần a, b mình làm được rồi!
CuO +2HCl= CuCl2 +H2O
ZnO+2HCl= ZnCl2 +H2O
gọi x,y là mol của CuO, ZnO
80x + 81y = 12.1
2x+2y = 0.3
=> x=0.05 , y=0.1 => mCuO= 4 %CuO=4/12.1 m ZnO=8.1 =>%ZnO=8.1/12.1
nH2SO4=1/2nHCl=0.3/2 =0.15
mH2SO4=0.15x98=14.7g => mddH2SO4=14.7/20%=73.5g
Đúng 0
Bình luận (2)
. Hòa tan hoàn toàn 12,1 gam hỗn hợp bột CuO và ZnO cần 73,5 gam dung dịch H2SO4 20% a) Viết các phương trình hóa học. b) Tính phần trăm theo khối lượng của mỗi oxit trong hỗn hợp ban đầu.
a)
$CuO + H_2SO_4 \to CuSO_4 + H_2O$
$ZnO + H_2SO_4 \to ZnSO_4 +H_2O$
b) Gọi $n_{CuO} = a(mol) ; n_{ZnO} = b(mol) \Rightarrow 80a +81b = 12,1(1)$
Theo PTHH :
$n_{H_2SO_4} = a + b = \dfrac{73,5.20\%}{98} = 0,15(mol)(2)$
Từ (1)(2) suy ra : a = 0,05 ; b = 0,1
$\%m_{CuO} = \dfrac{0,05.80}{12,1}.100\% = 33,06\%$
$\%m_{ZnO} = 100\% - 33,06\% = 66,94\%$
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn 12,1 gam hỗn hợp bột CuO và ZnO cần 100ml dd HCl 3M.
a) Viết các phương trình hóa học
b) Tính % theo khối lượng của mỗi oxit trong hỗn hợp ban đầu
c) Hãy tính khối lượng dd H2SO4 ngồng độ 20% để hòa tan hoàn toàn hỗn hợp các oxit trên