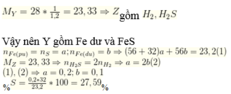Nếu đốt cháy hỗn hợp 12g bột Fe với 6,4g S trong 1 bình kín k có không khí , sau phản ứng còn dư 0,8g Fe. Tính khối lượng FeS thu được

Những câu hỏi liên quan
Trong bình kín không có không khí chứa bột hỗn hợp của 2,8 g Fe và 3,2 g S. Đốt nóng hỗn hợp cho phản ứng xảy ra hoàn toàn, sau phản ứng thu được sắt (II) sunfua (FeS).
a) Viết phương trình hoá học của phản ứng.
b) Tính khối lượng FeS thu được sau phản ứng biết lưu huỳnh dư 1,6 g.
PTHH: \(Fe+S\xrightarrow[]{t^o}FeS\)
Tính theo Fe
Ta có: \(n_{Fe}=\dfrac{2,8}{56}=0,05\left(mol\right)=n_{FeS}\) \(\Rightarrow m_{FeS}=0,05\cdot88=4,4\left(g\right)\)
Đúng 3
Bình luận (4)
Một hỗn hợp có 6 gam bột S và 28 gam bột Fe đốt nóng hỗn hợp thu được FeS
a)tính khối lượng FeS
b) nếu hỗn hợp cho 8 gam bột lưu huỳnh và 28 g bột Fe
Hãy cho biết sau phản ứng khối lượng của Fe chất nào còn dư sau phản ứng và khối lượng là bao nhiêu
Fe + S -> FeS
nS=0,1875(mol)
nFe=0,5(mol)
Vì 0,1875<0,5 nên Fe dư
Theo PTHH ta có:
nS=nFeS=0,1875(mol)
mFeS=88.0,1875=16,5(g)
b;
nS=0,25(mol)
Vì 0,25<0,5 nên Fe dư 0,25 mol
mFe dư=56.0,25=14(g)
Đúng 0
Bình luận (0)
Bài 1: trong bình kín ko có không khí chứa bột hỗn hợp của 2,8g Fe và 3,2g S. Đốt nóng hỗn hợp cho phản ứng xảy ra hoàn toàn sau phản ứng thu được sắt(II) sunfua(FeS). Tính khối lượng FeS thu được sau phản ứng biết lưu huỳnh dư 1,6gBài 2:Fe3O4 là thành phần chính của quặng manhetit. Khi nung 232 tấn quặng manhetit thì cần 8 tấn khí hidro, sau phản ứng thu được sắt nguyên chất và 72 tấn hơi nước. Tính tỉ lệ phần trăm về khối lượng Fe3O4 trong quặng manhetit. Biết chỉ có Fe3O4 phản ứngbài 3: Có 1...
Đọc tiếp
Bài 1: trong bình kín ko có không khí chứa bột hỗn hợp của 2,8g Fe và 3,2g S. Đốt nóng hỗn hợp cho phản ứng xảy ra hoàn toàn sau phản ứng thu được sắt(II) sunfua(FeS). Tính khối lượng FeS thu được sau phản ứng biết lưu huỳnh dư 1,6g
Bài 2:Fe3O4 là thành phần chính của quặng manhetit. Khi nung 232 tấn quặng manhetit thì cần 8 tấn khí hidro, sau phản ứng thu được sắt nguyên chất và 72 tấn hơi nước. Tính tỉ lệ phần trăm về khối lượng Fe3O4 trong quặng manhetit. Biết chỉ có Fe3O4 phản ứng
bài 3: Có 1 viên đá vôi nhỏ, 1 ống nghiệm đựng axit clohidric và 1 cân nhỏ với độ chính xác cao. Làm thế nào để xác định được khối lượng khí cacbonic thoát ra khi cho viên đá vôi vào ống nghiệm đựng axit
giúp mình đi ạ, mình cần gấp lắm
Bài 1 :
Khối lượng FeS thu được sau phản ứng biết lưu huỳnh dư 1,6 g :
mFe = mFe + mS - mS.dư
= 2,8 + 3,2 - 1,6
= 4,4 (g)
Đúng 0
Bình luận (0)
a/Fe + S = FeS
2,8 +3,2= FeS
6 = FeS
=> FeS=6g
Đúng 0
Bình luận (1)
đổi 8 tấn = 8000000g
\(n_{H_2}=\dfrac{8000000}{2}=4000000\left(mol\right)\)
Fe3O4 + 4H2 \(\underrightarrow{t^o}\) 3Fe + 4H2O
de:1000000\(\leftarrow\) 4000000
\(m_{Fe_3O_4}=232.1000000=232000000g=232\left(t\right)\)
\(\%m_{Fe}=\dfrac{232}{232}.100\%=100\%\)
Đúng 0
Bình luận (0)
Bài 14: Một bình kín có dung tích 1,4l đầy không khí (đktc). Nếu đốt cháy 2,5g photpho P trong bình, thì photpho có cháy hết không?Bài 15: Đốt cháy 100g hỗn hợp bột lưu huỳnh S và sắt Fe dùng hết 33,6l khí oxi (đktc). Tính khối lượng mỗi chất trong hỗn hợp. Biết rằng đốt Fe tạo ra Fe3O4Bài 16: Dẫn 11,2 lít khí H2 (đktc) qua ống nghiệm chứa 16 gam CuO. Sau khi phản ứng kết thúc, hãy tính: khối lượng kim loại thu được. Sau phản ứng có chất nào còn dư, dư bao nhiêu?
Đọc tiếp
Bài 14: Một bình kín có dung tích 1,4l đầy không khí (đktc). Nếu đốt cháy 2,5g photpho P trong bình, thì photpho có cháy hết không?
Bài 15: Đốt cháy 100g hỗn hợp bột lưu huỳnh S và sắt Fe dùng hết 33,6l khí oxi (đktc). Tính khối lượng mỗi chất trong hỗn hợp. Biết rằng đốt Fe tạo ra Fe3O4
Bài 16: Dẫn 11,2 lít khí H2 (đktc) qua ống nghiệm chứa 16 gam CuO. Sau khi phản ứng kết thúc, hãy tính: khối lượng kim loại thu được. Sau phản ứng có chất nào còn dư, dư bao nhiêu?
Bài 14
\(n_{O_2}=\dfrac{1.4}{22,4}=0,0625\left(mol\right)\)
\(n_P=\dfrac{2.5}{31}=0,0806451\left(mol\right)\)
4P + 5O2 ----to--->2P2O5
Xét tỉ lệ : \(\dfrac{0.0625}{5}< \dfrac{0.0806451}{4}\)
=> P ko cháy hết
Đúng 2
Bình luận (0)
bài 15
\(n_{O_2}=\dfrac{3.36}{22,4}=0,15\left(mol\right)\)
Gọi nFe = a ( mol ) và nS = b (mol )
PTHH :
S + O2 ---to---> SO2
3Fe + 2O2 ----to----> Fe3O4
Ta có 32b + 56a= 100
Theo PT : nS = nO2 = b (mol)
Theo PT : nO2 = 2/3 nFe = 2/3a ( mol)
=> 2/3a + b = 1,5
Từ những điều trên \(\left[{}\begin{matrix}56a+32b=100\\\dfrac{2}{3}a+b=1,5\end{matrix}\right.\Leftrightarrow\left[{}\begin{matrix}a=1,5\left(mol\right)\\b=0,5\left(mol\right)\end{matrix}\right.\)
\(m_{Fe}=1,5.56=84\left(g\right)\)
\(m_S=0,5.32=16\left(g\right)\)
Đúng 2
Bình luận (0)
Bài 16 :
\(n_{H_2}=\dfrac{11.2}{22,4}=0,5\left(mol\right)\)
\(n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)\)
Ta thấy : 0,5 > 0,2 => H2 dư , CuO đủ
PTHH : CuO + H2 -> Cu + H2O
0,2 0,2 0,2
\(m_{Cu}=0,2.64=12,8\left(g\right)\)
\(m_{H_2\left(dư\right)}=\left(0,5-0,2\right).2=0,6\left(g\right)\)
Đúng 2
Bình luận (0)
Thực hiện các thí nghiệm sau:(1) Đốt dây sắt dư trong khí clo(2) Đốt nóng hỗn hợp bột Fe và S (trong điều kiện không có oxi)(3) Cho FeO vào dung dịch HNO3 (loãng dư)(4) Cho Mg vào dung dịch Fe2(SO4)3(5) Cho Fe vào dung dịch H2SO4(loãng, dư)(6) Nung hỗn hợp Fe và I2 trong bình kínSố thí nghiệm sau khi phản ứng hoàn toàn thu được muối sắt (II) là: A. 2 B. 3 C. 4 D. 5
Đọc tiếp
Thực hiện các thí nghiệm sau:
(1) Đốt dây sắt dư trong khí clo
(2) Đốt nóng hỗn hợp bột Fe và S (trong điều kiện không có oxi)
(3) Cho FeO vào dung dịch HNO3 (loãng dư)
(4) Cho Mg vào dung dịch Fe2(SO4)3
(5) Cho Fe vào dung dịch H2SO4(loãng, dư)
(6) Nung hỗn hợp Fe và I2 trong bình kín
Số thí nghiệm sau khi phản ứng hoàn toàn thu được muối sắt (II) là:
A. 2
B. 3
C. 4
D. 5
Đáp án B
Các trường hợp thỏa mãn: 2-5-6
Đúng 0
Bình luận (0)
Thực hiện các thí nghiệm sau: (1) Đốt dây sắt dư trong khí clo (2) Đốt nóng hỗn hợp bột Fe và S (trong điều kiện không có oxi) (3) Cho FeO vào dung dịch HNO3 (loãng dư) (4) Cho Mg vào dung dịch Fe2(SO4)3 (5) Cho Fe vào dung dịch H2SO4(loãng, dư) (6) Nung hỗn hợp Fe và I2 trong bình kín Số thí nghiệm sau khi phản ứng hoàn toàn thu được muối sắt (II) là: A. 2 B. 3 C. 4 D. 5
Đọc tiếp
Thực hiện các thí nghiệm sau:
(1) Đốt dây sắt dư trong khí clo
(2) Đốt nóng hỗn hợp bột Fe và S (trong điều kiện không có oxi)
(3) Cho FeO vào dung dịch HNO3 (loãng dư)
(4) Cho Mg vào dung dịch Fe2(SO4)3
(5) Cho Fe vào dung dịch H2SO4(loãng, dư)
(6) Nung hỗn hợp Fe và I2 trong bình kín
Số thí nghiệm sau khi phản ứng hoàn toàn thu được muối sắt (II) là:
A. 2
B. 3
C. 4
D. 5
Đáp án B
Các trường hợp thỏa mãn: 2-5-6
Đúng 0
Bình luận (0)
Cho 23,2 gam hỗn hợp X gồm S và Fe vào một bình kín không chứa không khí. Nung bình đến khi phản ứng kết thúc thu được chất rắn Y. Cho Y tác dụng với axit H2SO4 loãng, dư thu được khí Z có tỉ khối đối với N2 là 1/1,2. Phần trăm khối lượng của S trong hỗn hợp X là A. 20,69% B. 27,59% C. 16,55% D. 48,28%
Đọc tiếp
Cho 23,2 gam hỗn hợp X gồm S và Fe vào một bình kín không chứa không khí. Nung bình đến khi phản ứng kết thúc thu được chất rắn Y. Cho Y tác dụng với axit H2SO4 loãng, dư thu được khí Z có tỉ khối đối với N2 là 1/1,2. Phần trăm khối lượng của S trong hỗn hợp X là
A. 20,69%
B. 27,59%
C. 16,55%
D. 48,28%
Nung nóng hỗn hợp gồm 4,4 gam Fe và 3,2 gam S ở dạng bột trong ống nghiệm không có không khí . Tính khối lượng FeS tạo thành sau phản ứng.
a) nS= 0,1(mol)
nFe= 11/140(mol)
Vì: 0,1/1 < 11/140:1
=> Fe hết, S dư, tính theo nFe.
PTHH: Fe + S -to-> FeS
11/140____11/140__11/140(mol)
=> mFeS= 11/140 x 88 \(\approx\) 6,914(g)
Đúng 2
Bình luận (0)
Bài 1: a/ Hỗn hợp gồm có 16g bột S và 28g bột Fe. Đốt nóng hỗn hợp thu được chất duy nhất là FeS. Tính khối lượng của sản phẩm.
b/ Nếu hỗn hợp có 8g bột S và 28g bột Fe. Hãy cho biết:
- Khối lượng của FeS thu được là bao nhiêu gam?
- Chất nào còn dư sau phản ứng và dư bao nhiêu gam ?
1)a) Fe+S=to=>FeS
\(n_S=\frac{16}{32}=0,5mol;n_{Fe}=\frac{28}{56}=0,5mol\)
Dựa theo PTHH=> Hai chất đều hết.
\(n_{FeS}=n_{Fe}=0,5mol\Rightarrow m_{FeS}=0,5.88=44g\)
b) Fe+S=to=>FeS
\(n_S=\frac{8}{32}=0,25mol;n_{Fe}=\frac{28}{56}=0,5mol\)
Vì: \(\frac{0,25}{1}< \frac{0,5}{1}\Rightarrow\)S hết, Fe dư
-\(n_{FeS}=n_S=0,25mol\)
\(m_{FeS}=0,25.88=22g\)
\(n_{Fe\left(dư\right)}=0,5-\left(\frac{0,25.1}{1}\right)=0,25mol\)
\(m_{Fe\left(dư\right)}=0,25.56=14g\)
Đúng 0
Bình luận (0)