Có bao nhiêu gam đồng điều chế được khi cho tương tác 16g đồng sunfat với một lượng sắt cần thiết.
Cần bao nhiêu gam Pôtat ăn da cho phản ứng với 10g sắt III clorua ?
Có bao nhiêu gam đồng điều chế được khi cho tương tác 16g đồng sunfat với một lượng sắt cần thiết
Phương trình Hoá học: CuSO4 + Fe - > FeSO4 + Cu
160g 64g
16g xg
=> x = 16,64 : 160 = 6,4
Vậy điều chế được 6,4g đồng.
Phương trình Hoá học: CuSO4 + Fe - > FeSO4 +Cu
160g 64g
16g xg
=> x = 
Vậy điều chế được 6,4g đồng.
Câu 1: Cho 325 gam sắt clorua (chưa biết hóa trị) tác dụng với dung dịch AgNOз dư, thu được 8,61 gam kết tủa. Xác định công thức xỉa muối sắt clorua. Câu 2: Ngâm một lá kẽm trong 20 gam dung dịch muối đồng sunfat 10% cho đến khi phản ứng kết thúc. Tính khối lượng kẽm đã phản ứng với dung dịch trên và nồng độ phần trăm của dung dịch sau phản ứng. Câu 3: Cho 5,6 gam Fe tác dụng với 100ml dung dịch HCl 1M. Thể tích khí Hշ thu được (đktc) là?
Câu 3:
\(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right);n_{HCl}=0,1.1=0,1\left(mol\right)\\ Fe+2HCl\rightarrow FeCl_2+H_2\\ Vì:\dfrac{0,1}{1}>\dfrac{0,1}{2}\Rightarrow Fe.dư\\ n_{H_2}=\dfrac{n_{HCl}}{2}=\dfrac{0,1}{2}=0,05\left(mol\right)\\ V_{H_2\left(đktc\right)}=0,05.22,4=1,12\left(l\right)\)
Câu 1:
\(Đặt:FeCl_x\) (x: nguyên dương, x hoá trị của Fe)
\(FeCl_x+xAgNO_3\rightarrow xAgCl\downarrow+Fe\left(NO_3\right)_x\\ n_{AgCl}=\dfrac{8,61}{143,5}=0,06\left(mol\right)\\ n_{FeCl_x}=\dfrac{0,06}{x}\left(mol\right)\\ M_{FeCl_x}=\dfrac{3,25}{\dfrac{0,06}{x}}=\dfrac{3,25x}{0,06}\left(\dfrac{g}{mol}\right)\)
Xét x=1;x=2;x=3;x=4, ta thấy có lúc x=3 thì\(M_{FeCl_3}=162,5\left(\dfrac{g}{mol}\right)\)
Vậy nhận x=3 => CTHH FeCl3
Câu 2:
\(n_{CuSO_4}=\dfrac{20.10\%}{160}=0,0125\left(mol\right)\\ Zn+CuSO_4\rightarrow ZnSO_4+Cu\\ n_{Zn}=n_{Cu}=n_{ZnSO_4}=n_{CuSO_4}=0,0125\left(mol\right)\\ m_{Zn}=0,0125.65=0,8125\left(g\right)\\ m_{ddZnSO_4}=0,8125+20-0,0125.64=20,0125\left(g\right)\\ C\%_{ddZnSO_4}=\dfrac{0,0125.161}{20,0125}.100\%\approx10,056\%\)
Cho 20 gam sắt(III) sunfat F e 2 S O 4 3 tác dụng với natri hiđroxit (NaOH) thu được 10,7 gam sắt(III) hiđroxit F e 2 S O 4 3 và 21,3 gam natri sunfat N a 2 S O 4 Tính khối lượng natri hiđroxit tham gia phản ứng.
Cho 20 gam sắt III sunfat F e 2 S O 4 3 tác dụng với natri hidroxit NaOH, thu được 10,7 gam sắt III hidroxit F e ( O H ) 3 và 21,3 gam natri sunfat N a 2 S O 4 . Xác định khối lượng natri hidroxit tham gia vào phản ứng.
Sơ đồ
Sắt (III) sunfat + Natri hidroxit → Sắt (III) hidroxit + natri sunfat
Áp dụng ĐLBTKL, ta có
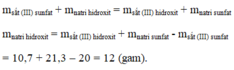
Bài 1: Cho kim loại sắt vào dung dịch axit H2SO4 loãng. Sau một thời gian, sắt tan hết thu được 6,72 lit khí hiđrô (đktc).
a) Tính khối lượng sắt ban đầu?
b) Để có lượng sắt tham gia phản ứng trên, phải cho bao nhiêu gam sắt(III) oxit tác dụng với khí hiđrô?
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3mol\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
0,3 0,3
a)\(m_{Fe}=0,3\cdot56=16,8g\)
b)\(Fe_2O_3+3H_2\rightarrow3Fe+3H_2O\)
0,1 0,3 0,3
\(m_{Fe_2O_3}=0,1\cdot160=16g\)
a)nH2 =6,72:22,4=0,3(mol)
PTHH Fe+H2SO4--->FeSO4+H2
theo pt , nFe = nH2 = 0,3 (mol)
=> mFe =n.M=0,3.56=16,8(g)
b) Ta có nH2=nFe=0,3(MOL)
Pthh: Fe2O3 + 3H2 ---> 2Fe + 3H2O
theo pt , nFe2O3=1/3 nH2=0,1(mol)
=> mFe2O3= n.M=0,1.(56.2+16.3)=16(g)
Vậy để có lượng sắt tham gia phản ứng trên phải có 16g Fe2O3 để tác dụng với H2
cho bột sắt vào dd chứa 0,2 mol H2SO4 loãng phản ứng hoàn toàn ng ta thu được 1,68 lít khí H2 tính khối lượng sắt phản ứng và để có sắt trên ng ta phải dùng bao nhiêu gam sắt (III) oxit tác dụng với khí H2 dư
Phải dùng 4,2 g Fe
Cần 6g sắt (III) oxit tác dụng với H2 dư
Cho mạt sắt vào một dung dịch chứa 0,2 mol H 2 S O 4 loãng. Sau một thời gian, bột sắt tan hoàn toàn và người ta thu được 1,68 lit khí hidro (đktc). Để có lượng sắt tham gia phản ứng trên, người ta phải dùng bao nhiêu gam sắt (III) oxit tác dụng với khí hidro.
.Cho sắt (III) clorua FeCl3 tác dụng với 5,5 gam kali hidroxit thu được 7 gam sắt (III) hiđroxit Fe(OH)3 và 8,25 kali clorua. Khối lượng FeCl3 đã tham gia vào phản ứng trên *
A 9,7gam
B 9 gam
C 9,5 gam
D 9,75gam
Bảo toàn KL: \(m_{FeCl_3}+m_{KOH}=m_{Fe\left(OH\right)_3}+m_{KCl}\)
\(\Rightarrow m_{FeCl_3}=7+8,25-5,5=9,75\left(g\right)\)
Chọn D
Cho 6,4 gam đồng tác dụng vừa đủ với khí oxi ở nhiệt độ cao. Sau phản ứng thu được chất rắn màu đen là đồng (II) oxit. a. Viết PTHH của phản ứng. b. Tính khối lượng oxit sắt từ thu được. c. Tính khối lượng thuốc tím KMnO4 cần dùng để điều chế được khí oxi cho phản ứng trên. d. Nếu cho không khí tác dụng với lượng đồng ở trên thì cần bao nhiêu lít không khí (ở đktc). Biết oxi chiếm 20% thể tích không khí. Cho Cu = 64 ; O = 16
a)
\(2Cu + O_2 \xrightarrow{t^o} 2CuO\)
b)
\(n_{CuO} = n_{Cu} = \dfrac{6,4}{64} = 0,1(mol)\\ \Rightarrow m_{CuO} = 0,1.80 = 8(gam)\)
c)
\(n_{O_2} = \dfrac{1}{2}n_{Cu} = 0,05(mol)\\ 2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2\\ m_{KMnO_4} = 2n_{O_2} = 0,05.2 = 0,1.158 = 15,8(gam)\)
d)
\(V_{không\ khí} = 5V_{O_2} = 0,05.22,4.5 = 5,6(lít)\)