Oxi hoá hoàn toàn 5,1g hỗn hợp gồm 2 kim loại X,Y thu được 24,56g hỗn hợp X gồm 2 oxit. Hoà tan hoàn toàn hỗn hợp X bằng 1 lượng vừa đủ dung dịch H2SO4 (d = 1,25 g/ml). Tính thể tích dung dịch H2SO4 đã dùng

Những câu hỏi liên quan
Oxi hoá hoàn toàn 16,8g hỗn hợp gồm 2 kim loại X,Y thu được 50,8g hỗn hợp Z gồm 2 oxit. Hoà tan hoàn toàn hỗn hợp Z bằng 1 lượng vừa đủ dung dịch H2SO4 (d = 1,25 g/ml). Tính thể tích dung dịch H2SO4 đã dùng
Đốt cháy hoàn toàn 33,4 gam hỗn hợp X gồm bột các kim loại Al, Fe và Cu ngoài không khí, thu được 41,4 gam hỗn hợp Y gồm 3 oxit. Cho toàn bộ hỗn hợp Y tác dụng hoàn toàn với dung dịch H2SO4 20% có khối lượng riêng d1,14 g/ml. Thể tích tối thiểu của dung dịch H2SO4 20% để hoà tan hết hỗn hợp Y là A. 300 ml B. 175 ml C. 200 ml D. 215 ml
Đọc tiếp
Đốt cháy hoàn toàn 33,4 gam hỗn hợp X gồm bột các kim loại Al, Fe và Cu ngoài không khí, thu được 41,4 gam hỗn hợp Y gồm 3 oxit. Cho toàn bộ hỗn hợp Y tác dụng hoàn toàn với dung dịch H2SO4 20% có khối lượng riêng d=1,14 g/ml. Thể tích tối thiểu của dung dịch H2SO4 20% để hoà tan hết hỗn hợp Y là
A. 300 ml
B. 175 ml
C. 200 ml
D. 215 ml
Đốt cháy hoàn toàn 15 gam hỗn hợp gồm 3 kim loại A,B,C thu được 16,6 gam hỗn hợp oxit. Hoà tan hoàn toàn 16,6 gam hỗn hợp oxit trên bằng dung dịch H2SO4 loãng (vừa đủ).
a. Thể tích dung dịch H2SO4 0,2M đã dùng.
b. Tổng khối lượng muối sunfat tạo thành.
a)
\(n_{O_2\left(pư\right)}=\dfrac{16,6-15}{32}=0,05\left(mol\right)\)
Bảo toàn O: nH2O = 0,1 (mol)
Bảo toàn H: nH2SO4 = 0,1 (mol)
=> \(V_{dd.H_2SO_4}=\dfrac{0,1}{0,2}=0,5\left(l\right)\)
b)
Theo ĐLBTKL: moxit + mH2SO4 = mmuối + mH2O
=> 16,6 + 0,1.98 = mmuối + 0,1.18
=> mmuối = 24,6 (g)
Đúng 4
Bình luận (0)
Đốt cháy hoàn toàn 15 gam hỗn hợp gồm 3 kim loại A, B, C thu được 16,6 gam hỗn hợp oxit. Hòa tan hoàn toàn 16,6 gam hỗn hợp oxi trên bằng dung dịch H2SO4 loãng(vừa đủ).a.Thể tích dung dịch H2SO4 0,2M đã dùng.b.Tổng khối lượng muối sunfat tạo thành.
Đọc tiếp
Đốt cháy hoàn toàn 15 gam hỗn hợp gồm 3 kim loại A, B, C thu được 16,6 gam hỗn hợp oxit. Hòa tan hoàn toàn 16,6 gam hỗn hợp oxi trên bằng dung dịch H2SO4 loãng(vừa đủ).
a.Thể tích dung dịch H2SO4 0,2M đã dùng.
b.Tổng khối lượng muối sunfat tạo thành.
BTKL
mO2=16.6−15=1.6(g)
nO2=\(\dfrac{1,6}{32}\)=0.05(mol)
O2+4e→2O2−
0.05....0.2
2H++2e→H2
0.2......0.2
VH2SO4=\(\dfrac{0,2}{0,2}\)=1l
nH2O=nH2SO4=0.1(mol)
BTKL
mM=16.6+0.1⋅98−0.1⋅18=24.6(g)
Đúng 2
Bình luận (0)
Chia hỗn hợp gồm 2 kim loại X, Y có hoá trị không đổi thành 2 phần bằng nhau: Phần 1: Hoà tan hoàn toàn trong dung dịch hỗn hợp gồm HCl và H2SO4 thu được 3,36 lít H₂(ở đktc). Phần 2: Hoà tan hoàn toàn trong dung dịch HNO3 thu được V lít NO duy nhất (ở đktc). Giá trị của V
Đốt cháy hoàn toàn m gam hỗn hợp gồm 3 kim loại A,B,C thu được 16,6g hỗn hợp oxit. Hòa tan hoàn toàn 16,6 g hỗn hợp oxit trên bằng dung dịch H2SO4 loãng (vừa đủ). Cô cạn dung dịch sau PƯ được 24,6g muối khan. Tính m và khối lượng H2SO4 đã dùng
Gọi số mol H2O sinh ra là a (mol)
=> \(n_{H_2SO_4}=a\left(mol\right)\)
Theo ĐLBTKL: moxit + mH2SO4 = mmuối + mH2O
=> 16,6 + 98a = 24,6 + 18a
=> a = 0,1 (mol)
=> nO = 0,1 (mol)
=> mkim loại = 16,6 - 0,1.16 = 15 (g)
\(m_{H_2SO_4}=0,1.98=9,8\left(g\right)\)
Đúng 2
Bình luận (0)
Câu 1: Hòa tan hoàn toàn 3,645 gam hỗn hợp gồm Mg và Zn vào một lượng vừa đủ dung dịch H2SO4 loãng, sau phản ứng thu được 1,68 lít H2 (đktc) và dung dịch X. Tính khối lượng muối trong dung dịch X ( 3 cách) Bài 3: Hoà tan hoàn toàn 2,49 g hỗn hợp kim loại Y gồm Zn, Fe, Mg bằng dung dịch H2SO4 loãng thu được 8,25g muối sunfat và V lit H2 (đktc). a) Tính khối lượng H2SO4 cần dùng ? b) Tính V ?
Chia hỗn hợp gồm 2 kim loại X, Y có hoá trị không đổi thành 2 phần bằng nhau: + Phần 1: Hoà tan hoàn toàn trong dung dịch hỗn hợp gồm HCl và H2SO4 được 3,36 lít H2 (đktc). + Phần 2: Hoà tan hoàn toàn trong dung dịch HNO3 thu được V lít NO duy nhất (đktc). Giá trị của V là: A. 2,24 lít. B. 3,36 lít. C. 4,48 lít. D. 5,60 lít.
Đọc tiếp
Chia hỗn hợp gồm 2 kim loại X, Y có hoá trị không đổi thành 2 phần bằng nhau:
+ Phần 1: Hoà tan hoàn toàn trong dung dịch hỗn hợp gồm HCl và H2SO4 được 3,36 lít H2 (đktc).
+ Phần 2: Hoà tan hoàn toàn trong dung dịch HNO3 thu được V lít NO duy nhất (đktc). Giá trị của V là:
A. 2,24 lít.
B. 3,36 lít.
C. 4,48 lít.
D. 5,60 lít.
Đáp án A
Vì hai kim loại X, Y đều có hóa trị không đổi và khối lượng hai phần bằng nhau nên ở hai phần, số mol electron mà kim loại nhường bằng nhau.
Khi đó
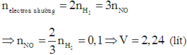
Đúng 0
Bình luận (0)
Câu 1: Hòa tan hoàn toàn 3,645 gam hỗn hợp gồm Mg và Zn vào một lượng vừa đủ dung dịch H2SO4 loãng, sau phản ứng thu được 1,68 lít H2 (đktc) và dung dịch X. Tính khối lượng muối trong dung dịch X ( 3 cách) ?
Bài 2: Hoà tan hoàn toàn m gam hỗn hợp A gồm Mg, Al bằng dung dịch HCl sau phản ứng thu được dung dịch Y và 5,6 lit H2 (đktc). Cô cạn dung dịch Y thu được 22,85gam muối khan.
a. Tính mHCl đã tham gia phản ứng?
b. Tính khối lượng hỗn hợp A?
Đọc tiếp
Câu 1: Hòa tan hoàn toàn 3,645 gam hỗn hợp gồm Mg và Zn vào một lượng vừa đủ dung dịch H2SO4 loãng, sau phản ứng thu được 1,68 lít H2 (đktc) và dung dịch X. Tính khối lượng muối trong dung dịch X ( 3 cách) ? Bài 2: Hoà tan hoàn toàn m gam hỗn hợp A gồm Mg, Al bằng dung dịch HCl sau phản ứng thu được dung dịch Y và 5,6 lit H2 (đktc). Cô cạn dung dịch Y thu được 22,85gam muối khan. a. Tính mHCl đã tham gia phản ứng? b. Tính khối lượng hỗn hợp A?
Bài 2 :
a)
$Mg + 2HCl \to MgCl_2 + H_2$
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
$n_{H_2} = \dfrac{5,6}{22,4} = 0,25(mol)$
$n_{HCl} = 2n_{H_2} = 0,5(mol)$
$m_{HCl} = 0,5.36,5 = 18,25(gam)$
b)
Bảo toàn khối lượng :
$m_A = 22,85 + 0,25.2 - 18,25 = 5,1(gam)$
Đúng 0
Bình luận (0)














