khi nồng độ CO tăng từ 0.03M đến 0.12M thì nồng độ CL2 tăng từ 0.02 đến 0.06 thì vận tốc phản ứng tăng lên bn lần ? Pthh : CO + CL2 -> COCL2

Những câu hỏi liên quan
Khi nhiệt độ tăng lên 25°C thì tốc độ phản ứng: H2 + Cl2
→
2HCl tăng lên 3 lần. Khi nhiệt độ tăng từ 20°C đến 95°C thì tốc độ phản ứng tăng lên A. 3 lần B. 9 lần C. 6 lần D. 27 lần.
Đọc tiếp
Khi nhiệt độ tăng lên 25°C thì tốc độ phản ứng: H2 + Cl2 → 2HCl tăng lên 3 lần. Khi nhiệt độ tăng từ 20°C đến 95°C thì tốc độ phản ứng tăng lên
A. 3 lần
B. 9 lần
C. 6 lần
D. 27 lần.
Cho phản ứng: 2CO
→
CO2 + C. Để tốc độ phản ứng trên tăng lên 4 lần thì nồng độ của CO phải tăng lên: A. 2 lần B. 3 lần C. 4 lần D. 8 lần
Đọc tiếp
Cho phản ứng: 2CO → CO2 + C.
Để tốc độ phản ứng trên tăng lên 4 lần thì nồng độ của CO phải tăng lên:
A. 2 lần
B. 3 lần
C. 4 lần
D. 8 lần
Trong các câu sau, câu nào đúng ?
A. Khi nồng độ chất phản ứng tăng thì tốc độ phản ứng tăng.
B. Khi nồng độ chất phản ứng giảm thì tốc độ phản ứng tăng.
C. Khi nồng độ chất phản ứng tăng thì tốc độ phản ứng giảm.
D. Nồng độ chất phản ứng không ảnh hưởng đến tốc độ phản ứng.
Thực hiện phản ứng sau trong bình kín:
C
O
(
k
)
+
C
l
2
(
k
)
→
C
O
C
l
2
(
k
)
Lúc đầu nồng độ
C
l
2
là 0,08 mol/l. Sau 1 phút 20 giây, nồng độ
C
l
2
là 0,024 mol/l. Tính tốc độ trung bình của phản ứng tính theo...
Đọc tiếp
Thực hiện phản ứng sau trong bình kín: C O ( k ) + C l 2 ( k ) → C O C l 2 ( k )
Lúc đầu nồng độ C l 2 là 0,08 mol/l. Sau 1 phút 20 giây, nồng độ C l 2 là 0,024 mol/l. Tính tốc độ trung bình của phản ứng tính theo C l 2 trong khoảng thời gian trên.
Biết rằng khi nhiệt độ tăng lên 100C thì tốc độ của một phản ứng tăng lên 2 lần . Vậy tốc độ phản ứng tăng lên bao nhiêu lần khi tăng nhiệt độ từ 200C đến 1000C. A. 64 lần. B. 14 lần. C. 256 lần. D. 16 lấn.
Đọc tiếp
Biết rằng khi nhiệt độ tăng lên 100C thì tốc độ của một phản ứng tăng lên 2 lần .
Vậy tốc độ phản ứng tăng lên bao nhiêu lần khi tăng nhiệt độ từ 200C đến 1000C.
A. 64 lần.
B. 14 lần.
C. 256 lần.
D. 16 lấn.
Chọn đáp án C
Cứ tăng lên 100C thì tốc độ tăng 2 lần
Vậy tăng 10.k0C thì vận tốc tăng 2k lần
k=8 ∆ v = 2 8 = 256 (lần)
Đúng 0
Bình luận (0)
Khi nhiệt độ tăng thêm 10° thì tốc độ phản ứng tăng 3 lần. Khi nhiệt độ tăng từ 20°C lên 80°C thì tốc độ phản ứng tăng lên A. 18 lần. B. 27 lần. C. 243 lần. D. 729 lần.
Đọc tiếp
Khi nhiệt độ tăng thêm 10° thì tốc độ phản ứng tăng 3 lần. Khi nhiệt độ tăng từ 20°C lên 80°C thì tốc độ phản ứng tăng lên
A. 18 lần.
B. 27 lần.
C. 243 lần.
D. 729 lần.
Đáp án D
Theo định nghĩa, số lần tăng tốc độ phản ứng khi nhiệt độ thay đổi 10°C chính là hệ số nhiệt độ g
Suy ra g = 3.
Thay vào công thức ta có tỉ số tốc độ phản ứng:
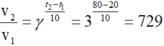
Vậy tốc độ phản ứng tăng 729 lần khi nhiệt độ tăng từ 20°C tới 80°C.
Đúng 0
Bình luận (0)
Khi nhiệt độ tăng thêm 10° thì tốc độ phản ứng tăng 3 lần. Khi nhiệt độ tăng từ 20°C lên 80°C thì tốc độ phản ứng tăng lên A. 18 lần. B. 27 lần. C. 243 lần. D. 729 lần.
Đọc tiếp
Khi nhiệt độ tăng thêm 10° thì tốc độ phản ứng tăng 3 lần. Khi nhiệt độ tăng từ 20°C lên 80°C thì tốc độ phản ứng tăng lên
A. 18 lần.
B. 27 lần.
C. 243 lần.
D. 729 lần.
Đáp án D
Theo định nghĩa, số lần tăng tốc độ phản ứng khi nhiệt độ thay đổi 10°C chính là hệ số nhiệt độ g
Suy ra g = 3.
Thay vào công thức ta có tỉ số tốc độ phản ứng:

Vậy tốc độ phản ứng tăng 729 lần khi nhiệt độ tăng từ 20°C tới 80°C.
Đúng 0
Bình luận (0)
Cho phản ứng: A + α B → A B α . Khi tăng nồng độ của A và B lên gấp đôi thì tốc độ của phản ứng tăng lên 16 lần. Hệ số α bằng
A. 1
B. 2
C. 3
D. 4
Trong công nghiệp, người ta tổng hợp NH3 theo phương trình hóa học sau: N2(k) + 3H2(k) D 2NH3(k). Khi tăng nồng độ H2 lên hai lần (giữ nguyên nồng độ của khí nitơ và nhiệt độ của phản ứng) thì tốc độ phản ứng tăng lên bao nhiêu lần: A. 2 lần B. 4 lần C. 8 lần D. 16 lần
Đọc tiếp
Trong công nghiệp, người ta tổng hợp NH3 theo phương trình hóa học sau: N2(k) + 3H2(k) D 2NH3(k). Khi tăng nồng độ H2 lên hai lần (giữ nguyên nồng độ của khí nitơ và nhiệt độ của phản ứng) thì tốc độ phản ứng tăng lên bao nhiêu lần:
A. 2 lần
B. 4 lần
C. 8 lần
D. 16 lần
Đáp án C
Tốc độ phản ứng tức thời: v = k[H2]3.[N2]
Vậy khi tăng nồng độ H2 lên hai lần (giữ nguyên nồng độ của khí nitơ và nhiệt độ của phản ứng) thì tốc độ phản ứng tăng lên 23 = 8 lần.
Đúng 0
Bình luận (0)







