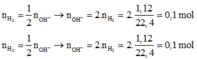3,6 hỗn hợp kali và kim loại kiềm tác dụng hết vơi nước sinh ra 1,12 lít khí H2 ở đktc,tìm kim loại kiềm biết số mol của nó nhỏ hơn 10% tổng số mol 2 kim loại trong hỗn hợp

Những câu hỏi liên quan
Cho 3,6 g hỗn hợp Kali và một kim loại X hóa trị I tác dụng vừa hết với nước được 1,12 lít khí H2 (đktc). Biết số mol X trong hỗn hợp lớn hơn 10% tổng số mol hai kim loại Kali và X.
a. Xác định kim loại X.
b. Tính thành phần phần trăm về khối lượng của mỗi kim loại trong hỗn hợp trên.
n H2 = 1,12/22,4 = 0,05(mol)
Gọi n K = a(mol) ; n X = b(mol)
$2K + 2H_2O \to 2KOH + H_2$
$2X + 2H_2O \to 2XOH + H_2$
n K + n X= a + b = 2n H2 = 0,1(mol)
=> n X = b > 0,1.10% = 0,01
Suy ra : 0,01 < b < 0,1
Ta có : 39a + Xb = 3,6
<=> 39(0,1 - b) + Xb = 3,6
<=> Xb - 39b = -0,3
<=> X = (-0,3 + 39b)/b
Với 0,01 < b < 0,1 thì 29 < X < 38
Vậy X không có giá trị X thỏa mãn
(Sai đề)
Đúng 1
Bình luận (2)
cho 3,6 gam hỗn hợp (kali và 1 kim loai M hóa trị 1 tan trong nước) tác dụng hết với nước sinh ra 1,12 l H2 . tìm M Biết số mol của nhóm nhỏ hơn 10% tổng số mol của 2 kim loại trong hỗn hợp
\(n_{H_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
PTHH: 2K + 2H2O → 2KOH + H2
Mol: x 0,5x
PTHH: 2M + 2H2O → 2MOH + H2
Mol: y 0,5y
TH1: x=10%(x+y) ⇒ 9x=y
Ta có hệ pt:
\(\left\{{}\begin{matrix}39x+M_M.y=3,6\\0,5x+0,5y=0,05\\9x=y\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}39x+M_M.y=3,6\\x+9x=0,1\\9x=y\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}M_M=\dfrac{3,6-39.0,01}{0,09}=35,7\left(g/mol\right)\\x=0,01\\y=0,09\end{matrix}\right.\left(loại\right)\)
TH2: y=10%(x+y) ⇒ 9y=x
Ta có hệ pt:
\(\left\{{}\begin{matrix}39x+M_M.y=3,6\\0,5x+0,5y=0,05\\9y=x\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}39x+M_M.y=3,6\\9y+y=0,1\\9y=x\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}M_M=\dfrac{3,6-39.0,09}{0,01}=9\left(g/mol\right)\\y=0,01\\x=0,09\end{matrix}\right.\left(loại\right)\)
Đúng 1
Bình luận (0)
Cho 3,6 g hỗn hợp X gồm K và 1 kim loại kiềm M tác dụng vừa hết với nước, thu đc 2,24 lít H2 ở 0,5 atm và 0 độ C . Biết số mol kim loại M trong hỗn hợp lớn hơn 10% tổng số mol 2 kim loại . Xác định kim loại M
Cho 3.6g hỗn hợp K và một kim loại kiềm tác dụng hết với H2O thu được 1.12 lít H2 (đktc). Tìm kim loại kiềm biết số mol của nó lớn hơn 10% tổng số mol của hai kim loại trong hỗn hợp.
Tính khối lượng từng chất trong hỗn hợp ban đầu và khối lượng sản phẩm ?
Cho 5,05 gam hỗn hợp gồm kali và một kim loại kiềm khác tác dụng hết với nước. Để trung hoà hoàn toàn dung dịch thu được cần dùng hết 250 ml dung dịch
H
2
SO
4
0,3M. Biết rằng tỉ lệ về số mol của kim loại kiềm chưa biết và kali trong hỗn hợp lớn hơn
1
4
. Phần trăm khối lượng kali trong hỗn hợp là A, 22,6%. B. 38,6%. C. 77,2%. D. 96,5%.
Đọc tiếp
Cho 5,05 gam hỗn hợp gồm kali và một kim loại kiềm khác tác dụng hết với nước. Để trung hoà hoàn toàn dung dịch thu được cần dùng hết 250 ml dung dịch H 2 SO 4 0,3M. Biết rằng tỉ lệ về số mol của kim loại kiềm chưa biết và kali trong hỗn hợp lớn hơn 1 4 . Phần trăm khối lượng kali trong hỗn hợp là
A, 22,6%.
B. 38,6%.
C. 77,2%.
D. 96,5%.
Hoà tan hết hỗn hợp gồm một kim loại kiềm và một kim loại kiềm thổ trong nước được dung dịch A và có 1,12 lít H2 bay ra (ở đktc). Cho dung dịch chứa 0,03 mol AlCl3 vào dung dịch A. Khối lượng kết tủa thu được là A. 0,78 gam. B. 0,81 gam C. 1,56 gam. D. 2,34 gam.
Đọc tiếp
Hoà tan hết hỗn hợp gồm một kim loại kiềm và một kim loại kiềm thổ trong nước được dung dịch A và có 1,12 lít H2 bay ra (ở đktc). Cho dung dịch chứa 0,03 mol AlCl3 vào dung dịch A. Khối lượng kết tủa thu được là
A. 0,78 gam.
B. 0,81 gam
C. 1,56 gam.
D. 2,34 gam.
Cho 3,6g hỗn hợp gồm kali và một kim loại kiềm A tác dụng vừa hết với nước cho 2,24 lít H2 ở 0,5 atm và 0oC
a) Khối lượng nguyên tử A lớn hơn hay nhỏ hơn kali
b) Bik số mol kim loại trong hỗn hợp lớn hơn 10% tổng số mol 2 kim loại vậy A là ngto nào
c) Xđ klg từng chất trong hỗn hợp ban đầu và hỗn hợp sản phẩm
Mong mb giải dễ hiểu dùm mình nha
0,5atm và 0oC hình như là 44,8 lít đó.
Tính số mol H2 = 0,05 (mol )
Gọi M là KLTB của hai kim loại
\(M_A< \overline{M}< M_B\)
\(\overline{M}+H_2O\rightarrow\overline{M}OH+\dfrac{1}{2}H_2\uparrow\)
0,1 <-----------------------0,05
\(M_{\overline{M}}=\dfrac{3,6}{0,1}=36\)
=> \(M_A< 36< M_K\) (1)
Vậy khối lượng ngtử A < Kali
b) Theo gt: \(n_A>0,1.10\%=0,01\)
=> \(n_K< 0,09\)
=> \(m_K< 0,09.39=3,51\)
\(M_A>\dfrac{3,6-3,51}{0,01}=9\) (2)
(1)(2) \(\Rightarrow\) A là Natri
c) \(\left\{{}\begin{matrix}39x+23y=3,6\\0,5x+0,5y=0,05\end{matrix}\right.\)\(\Rightarrow\left\{{}\begin{matrix}x=0,08125\\y=0,01875\end{matrix}\right.\)
\(m_K=39.0,08125=3,16875\left(g\right)\)
\(m_{Na}=0,01875.23=0,43125\left(g\right)\)
sản phẩm tự thế số vô tính đi nha
Đúng 0
Bình luận (2)
Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2 : 3) tác dụng với 3,36 lít Cl2, thu được hỗn hợp rắn Y. Hòa tan hết toàn bộ Y trong lượng dư dung dịch HCl, thu được 1,12 lít H2. Biết các phản ứng đều xảy ra hoàn toàn, các thể tích khí đều đo ở đktc. Kim loại M là Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2 : 3) tác dụng với 3,36 lít Cl2, thu được hỗn hợp rắn Y. Hòa tan hết toàn bộ Y trong lượng dư dung dịch HCl, th...
Đọc tiếp
Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2 : 3) tác dụng với 3,36 lít Cl2, thu được hỗn hợp rắn Y. Hòa tan hết toàn bộ Y trong lượng dư dung dịch HCl, thu được 1,12 lít H2. Biết các phản ứng đều xảy ra hoàn toàn, các thể tích khí đều đo ở đktc. Kim loại M là
Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2 : 3) tác dụng với 3,36 lít Cl2, thu được hỗn hợp rắn Y. Hòa tan hết toàn bộ Y trong lượng dư dung dịch HCl, thu được 1,12 lít H2. Biết các phản ứng đều xảy ra hoàn toàn, các thể tích khí đều đo ở đktc. Kim loại M là
Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2 : 3) tác dụng với 3,36 lít Cl2, thu được hỗn hợp rắn Y. Hòa tan hết toàn bộ Y trong lượng dư dung dịch HCl, thu được 1,12 lít H2. Biết các phản ứng đều xảy ra hoàn toàn, các thể tích khí đều đo ở đktc. Kim loại M là
A. Al.
B. Na
C. Ca.
D. K.
cho 3,6g hỗn hợp gồm kali và môt kim loại kiềm A tác dụng vừa hết vs nước cho 2,24 lít H2 (ở 0,5atm và 0oC)
a) khối lượng ngtu A lớn hay nhỏ hơn K
b) Biết số mol kim loại A trong hỗn hợp lớn hơn 10% tổng số mol 2 kim loại vậy A lf nguyên tố nào
c) Xđ m từng chất trong hh ban đầu và sản phẩm
Đề bài : n(H2)=2,24.0,50,082.273=0,05n(H2)=2,24.0,50,082.273=0,05 (mol) => M(tb hh) = 3,60,1=363,60,1=36 => A là Na hoặc Li . Vì n(A) > 10% tổng số mol 2 KL tức n(A) > 0,01 => A chỉ có thể là Na
32/ cho 12,2 g hỗn hợp 2 muối cacbonat của kim loại kiềm ở 2 chu kì liên tiếp tác dụng hết với dung dịch HCl,thu được 2,24lit khí (đktc) .Khối lượng muối tạo ra sau phản ứng là??
=>Do hỗn hợp 2 muối cacbonat của kim loại kiềm ở 2 chu kì liên tiếp .Dùng tăng giảm khối lượng : m(muối) = 12,2 + 1,1 = 13,3 (g)
Đúng 0
Bình luận (1)
Đề bài : n(H2)=2,24.0,50:082.273=0,05(mol)
=> M(tb hh) = 3,6:0,1=36 => A là Na hoặc Li . Vì n(A) > 10% tổng số mol 2 KL tức n(A) > 0,01 => A chỉ có thể là Na
32/ cho 12,2 g hỗn hợp 2 muối cacbonat của kim loại kiềm ở 2 chu kì liên tiếp tác dụng hết với dung dịch HCl,thu được 2,24lit khí (đktc) .Khối lượng muối tạo ra sau phản ứng là??
=>Do hỗn hợp 2 muối cacbonat của kim loại kiềm ở 2 chu kì liên tiếp .Dùng tăng giảm khối lượng : m(muối) = 12,2 + 1,1 = 13,3 (g)
Đúng 0
Bình luận (0)