Cho 36g hh X gồm 2 oxit của kim loại Natri và Canxi trộn theo tỉ lệ số mol tương ứng 2:1.Hoà tan hết hh X vào 214g nước được dd Y.
Tính nồng độ % và nông độ M của dd Y, biết khối lượng riêng ddY là 1,08g/ml
Cho 36g hh X gồm 2 oxit của kim loại Natri và Canxi trộn theo tỉ lệ số mol tương ứng 2: 1.
a) Tính thành phần % khối lượng hh X.
b) Hoà tan hết hh X vào 214g nước được dd Y. Tính C% và nồng độ M của dd Y, biết khối lượng riêng ddY là 1,08g/ml.
Hoà tan hoàn toàn 24,4 gam hh gồm FeCl2 và NaCl (có tỉ lệ số mol tương ứng là 1:2) vào một lượng nước (dư), thu được dd X. Cho dd AgNO3 (dư) vào dd X, sau khi pư xảy ra hoàn toàn sinh ra m gam chất rắn. Giá trị của m là
A. 57,4
B. 28,7
C. 10,8
D. 68,2
cho hh gồm Fe và kim loại X hoá trị n hoà tan hết dd HCl dư sau phản ứng thu được 7,84l khí H2 ở đktc. Nếu cho hh trên tác dụng với khí Clo thì thể tích khí Clo tham gia phản ứng là 8,4l. Biết tỉ lệ số mol của Fe và X là 1:4 và X có khối lượng là 5,4g. Xác định X
giúp mình với chiều mình đi học r
Hoà tan hoàn toàn 8,94 gam hh gồm Na, K và Ba vào nước, thu đươc dd X và 2,688 lít khí H2 (đktc). Dd Y gồm HCl và H2SO4, tỉ 1ệ mol tương ứng 1à 4: 1. Trung hòa dd X bởi dd Y, tổng khối lượng các muối được tạo ra 1à
A. 13,70 gam.
B. 12,78 gam.
C. 18,46 gam.
D. 14,62 gam.
Đáp án C
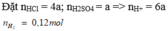
Do kim 1oại kiềm và kiềm thổ phản ứng với H2O
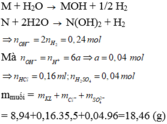
Hòa tan hoàn toàn 12,1 gam hh bột gồm CuO và 1 oxit Kim loại hóa trị II khác cần 100 ml dd HCl 3 M. Biết tỉ lệ mol của 2 oxit là 1:2
a, xác địng CTHH của oxit còn lại
,tính %theo khối lượng của mỗi oxit trong hh ban đầu,
Gọi công thức tổng quát của oxit đó là MO
PTHH:Mo+2HCl->MCl2+H2O(1)
CuO+2HCl->CuCl2+H2O(2)
nHCl=0.1*3=0.3(mol)
Gọi nCuO là x
Ta có:nMO/nCuO=2->nMO=2x(mol)
Theo pthh(1):nHCl:nMO=2->nHCl(1)=2*2x=4x(mol)
Theo pthh(2):nHCl:nCuO=2->nHCl(2)=2*x=2x(mol)
Ta có:4x+2x=0.3
<->6x=0.3
->x=0.05(mol)
mMo=12.1-(80*0.05)=8.1(g)
nMo=2*0.05=0.1(mol)
Khối lượng mol Mo=8.1:001=81(g/mol)
->M=81-16=65(g/mol)->M là Zn
b)mCuO=0.05*80=4(g)
mZnO=0.1*81=8.1(g)
Bạn tự tính % ra nhé ^^
Bài 1:
X, Y là 2 dd HCl có nồng độ mol/lit khác nhau. Cho V1 lít dd X + ddNagNO3 dư thì thu được 37,875 g kết tủa. Trung hòa V2 lít dd Y cần 500ml dd NaOH 0,3M. Trộn V1 lít dd Y thu được 2l dd Z. Tính nồng đồ mol/lit của dd Z. Biết tỷ lệ nồng độ ddX và ddY là 1:5. Tính nồng độ mol/lit của ddX và ddY.
Bài 2:
Hỗn hợp A gồm kim loại Mg, Al, Fe.
a. Lấy 14,7g hỗn hợp A cho td với dd NaOH dư, sinh ra e,36l khí ở dktc. Mặt khác cũng lấy 14,7g hỗn hợp A cho td với dd HCl dư, sinh ra 10,08l khí dktc và dd B. Cho dd B td với dd NaOH dư, kết tủa tạo thành được rửa sạch, nung nóng trong không khí đến khối lượng không đổi thu được m gam chất rắn. Tính m và tính % theo khối lượng của mỗi kim loại trong hh A.
b. Cho m gam hh A td với dd CuSO4 dư, sau khi phản ứng kết thúc, lọc lấy chất rắn đem hòa tan hết chất rắn trong dd HNO3 loãng dư, thu được 26,88l khí NO dktc. Tính khối lượng m
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15mol\)
2Al+2NaOH+2H2O\(\rightarrow\)2NaAlO2+3H2
\(n_{Al}=\dfrac{2}{3}n_{H_2}=\dfrac{2}{3}.0,15=0,1mol\)\(\rightarrow\)\(m_{Al}=2,7g\)
\(m_{Mg,Fe}=14,7-2,7=12g\)
\(n_{Mg}=xmol\);\(n_{Fe}=ymol\)
Mg+2HCl\(\rightarrow\)MgCl2+H2
Fe+2HCl\(\rightarrow\)FeCl2+H2
- Ta có hệ phương trình:
\(\left\{{}\begin{matrix}24x+56y=12\\x+y=\dfrac{10,08}{22,4}=0,45\end{matrix}\right.\)
Giải ra x=0,4125 và y=0,0375
\(\%Al=\dfrac{2,7}{14,7}.100\approx18,4\%\)
\(\%Mg=\dfrac{0,4125.24}{14,7}.100\approx67,35\%\)
\(\%Fe=100\%-18,4\%-67,35\%=14,25\%\)
- Tóm tắt PTHH:
MgCl2\(\rightarrow\)Mg(OH)2\(\rightarrow\)MgO
FeCl2\(\rightarrow\)Fe(OH)2\(\rightarrow\)Fe(OH)3\(\rightarrow\)Fe2O3
\(m=m_{MgO}+m_{Fe_2O_3}=0,4125.40+\dfrac{1}{2}.0,0375.160=19,5g\)
cho 15,6 g hh gồm kim loại M (hóa trị II) và Al (có tỉ lệ mol tương ứng là 1:2) vào bình đựng 13,44 lít khí Cl2 (đktc), sau khi các pư hoàn toàn thu được hh chất rắn X. Cho X tan hết trong dd HCl dư thu được 4,48 lít khí H2 (đktc) thoát ra.
a) xác định kim loại M
b) mặt khác, hòa tan hoàn toàn 0,1 mol M và 0,2 mol Al vào dd HNO3 loãng dư, sau pư khối lượng dd tăng thêm 7,8g. Tính số mol HNO3 đã tham gia pư
a) \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Gọi \(\left\{{}\begin{matrix}n_M=a\left(mol\right)\\n_{Al}=2a\left(mol\right)\end{matrix}\right.\)
=> a.MM + 54a = 15,6 (1)
\(n_{Cl_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
M0 - 2e --> M+2
a--->2a
Al0 - 3e --> Al+3
2a-->6a
Cl20 + 2e --> 2Cl-1
0,6-->1,2
2H+1 + 2e --> H20
0,4<--0,2
Bảo toàn e: 2a + 6a = 1,6
=> a = 0,2
Thay vào (1) => MM = 24 (g/mol)
=> M là Mg
b) Xét \(m_{Mg}+m_{Al}=0,1.24+0,2.27=7,8\left(g\right)\)
=> Không có khí thoát ra
=> pư tạo ra sản phẩm khử là NH4NO3
PTHH: 4Mg + 10HNO3 --> 4Mg(NO3)2 + NH4NO3 + 3H2O
0,1---->0,25
8Al + 30HNO3 --> 8Al(NO3)3 + 3NH4NO3 + 9H2O
0,2--->0,75
=> nHNO3 = 0,25 + 0,75 = 1 (mol)
Cho 21,2g hh E gồm Cu và Fe3O4 với tỉ lệ mol tương ứng là 3:1 vào 125g dd HCl 14,6%. Sau khi pứ xảy ra hoàn toàn thu được chất rắn X và dd Y a, Tính khối lượng chất rắn X b, Tính C% các chất tan trong dd Y
Gọi \(n_{Fe_3O_4}=a\left(mol\right)\rightarrow n_{Cu}=3a\left(mol\right)\)
\(232a+64.3a=21,2\\ \Leftrightarrow a=0,05\left(mol\right)\)
\(m_{HCl}=125.14,6\%=18,25\left(g\right)\)
PTHH:
Fe3O4 + 8HCl ---> FeCl2 + 2FeCl3 + 4H2O
0,05------>0,4------->0,05---->0,1
\(m_X=0,05.3.64=9,6\left(g\right)\)
\(m_{dd}=232.0,05+125=136,6\left(g\right)\\ \rightarrow\left\{{}\begin{matrix}C\%_{FeCl_2}=\dfrac{0,05.127}{136,6}.100\%=4,65\%\\C\%_{FeCl_3}=\dfrac{0,1.162,5}{136,6}.100\%=11,9\%\\C\%_{HCl\left(dư\right)}=\dfrac{18,25-0,4.36,5}{136,6}=2,67\%\end{matrix}\right.\)
Hòa tan hết hh X gồm oxit của một kim loại hóa trị II và muối cacbonat của kim loại đó H2SO4 loãng cừa đủ, sau PỨ thu được sản phẩm gồm khí Y và dd Z. Biết lượng khí Y bằng 44% lượng X. Đem cô cạn dd Z thu được một lượng muối khan bằng 168% lượng X. Tìm kim loại hóa trị II. Tính % theo khối lượng mỗi chất trong hh X.
Ta có: MO + H2SO4 ---> MSO4 + H2O
a a
MCO3 + H2SO4 ---> MSO4 + H2O + CO2
b b b
Chọn b=1 => khối lượng CO2 = 44g => mA = 100g => mMSO4 = 168g
(M + 16)a + (M + 60)b = 100 (1)
(M + 96)(a + b) = 168 (2)
Thế b=1 vào (1) và (2) => a = 0,4 mol ; M = 24 (kim loại Mg)
%MO = (40*0,4/100)*100= 16%
%MCO3 = 100% -16% = 84%
Vậy kim loại 2 là mg và khối lượng hóa học x là 84 %