1 nguyên tử X có 3 đồng vị. A1=24 chiếm 78,6%. A2=25 chiếm 10%. A3=26 chiếm 11,4%. Mỗi khi có 50 nguyên tử X, A=25 thì có bao nhiêu nguyên tử các đồng vị còn lại?
Giải dùm mình cụ thể nha..cảm ơn nhiều ạ !
Nguyên tử X có 3 đồng vị có số khối lần lượt là A1, A2, A3. Tổng số khối là 51, A2 nhiều hơn A1 là 1 đơn vị, A3 bằng 9/8 A1.a) Tính số khối của mỗi đồng vị.b) Biết rằng đồng vị thứ nhất chiếm 99,577%, đồng vị thứ hai chiếm 0,339%. Tìm nguyên tử khối trung bình của X.
Nguyên tố X có 3 đồng vị: A1 chiếm 92,3%, A2 chiếm 4,7% và A3 chiếm 3%. Tổng số khối của 3 đồng vị là 87. Số nơtron trong 1 nguyên tử A2 nhiều hơn trong nguyên tử A1 là một hạt. Nguyên tử khối trung bình của X là 28,107. Vậy số khối của 3 đồng vị là:
A. 27,28,32.
B. 26,27, 34.
C. 28,29,30.
D. 29,30,28.
Đáp án C
Gọi số khối của X lần lượt là A1, A2, A3
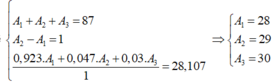
Nguyên tố X có 3 đồng vị: A1 chiếm 92,3%, A2 chiếm 4,7% và A3 chiếm 3%. Tổng số khối của 3 đồng vị là 87. Số nơtron trong 1 nguyên tử A2 nhiều hơn trong nguyên tử A1 là một hạt. Nguyên tử khối trung bình của X là 28,107. Vậy số khối của 3 đồng vị là:
A. 27,28,32.
B. 26,27, 34.
C. 28,29,30.
D. 29,30,28.
Đáp án C
Gọi số khối của X lần lượt là A1, A2, A3
Ta có hệ
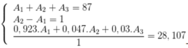
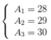
Mg có 3 đồng vị bền: 24Mg ( chiếm 79,4%); 25Mg ( chiếm 9,2%) còn lại là đồng vị 26Mg.
a. Tính nguyên tử khối trung bình của Mg.
b. Hỏi mỗi khi có 460 nguyên tử đồng vị 25Mg thì có bao nhiêu nguyên tử 24Mg, bao nhiêu nguyên tử 26Mg?
Nguyên tố R có 3 đồng vị .Đồng vị thứ nhất chứa 12 nơtron, chiếm 78,6%.Đồng vị thứ hai chứa 13 nơtron,chiếm 10/5.Đồng vị thứ 3 chứa 14 nơtron, chiếm 11,4% về số nguyên tử.Biết nguyên tử khối trung bình của R là 24,348.Tính số khối mỗi đồng vị và viết kí hiệu mỗi đồng vị
X là một kim loại hóa trị hai .hòa tan hoàn toàn 6,082g X vào đ HCL dư thì thu được 5,6l khí dktc?
tìm khối lưongj nguyên tử và tên nguyên tố X.b) X có 3 đồng vị bik tổng số khối của 3 đồng vị là 75.số khối của đồng vị thứ hai bằng trung bình cộng số khối của hai đơn vị kia,đơn vị thứ nhất có số proton = notron,đơn vị thứ ba chiếm 11,4% số nguyên tử và có số nôtrn nhìu hơn đồng vị thứ hai la` 1 đơn vị.tTÌM số khối và số n of mỗi loại đồng vị.tìm % về số nguyên tử của hai đông vị còn lại.khi có 50 nguyên tử của đồng vị thứ hai thì có bao nhiu nguyên tử của các đồng vị còn lại a.
X + 2HCl = XCl2 + H2
nX = nH2 = 5,6/22,4 = 0,25 mol
=> X = 6,082/0,25 = 24,328 (Mg)
b.
Mg có Z = 12
Gọi A1, A2, A3 lần lượt là số khối của 3 đồng vị
Tổng số khối của 3 đồng vị là 75
=> A1 + A2 + A3 = 75 (1)
Số khối của đồng vị thứ hai bằng trung bình cộng số khối của hai đồng vị kia
A2 = (A1 + A3)/2 => A1 - 2A2 + A3 = 0 (2)
Lấy (1) trừ (2) => 3A2 = 75 => A2 = 25 => N2 = A2 - Z = 25 - 12 = 13
Đồng vị thứ 3 có số neutron nhiều hơn đồng vị thứ 2 là 1 đơn vị
N3 - N2 = 1 => N3 = 1 + 13 = 14
=> A3 = 12 + 14 = 26
=> A1 = 75 - 26 - 25 = 24
Đồng vị 26Mg trong tự nhiên chiếm 11,4% số nguyên tử
=> %(24Mg, 25Mg) = 100% - 11,4% = 88,6%
Ta có : (88,6 - x)A1 + xA2 + 11,4A3 = 24,328.100
=> x = 10(%)
Vậy thành phần % của 3 đồng vị 24Mg, 25Mg và 26Mg lần lượt là
78,6%, 10% và 11,4%
c.
Giả sử có 100 nguyên tử Mg thì sẽ có
78,6 nguyên tử 24Mg ; 10 nguyên tử 25Mg ; 11,4 nguyên tử 26Mg
Vậy nếu có 50 nguyên tử 25Mg thì sẽ có
393 nguyên tử 24Mg và 57 nguyên tử 26Mg
Nguyên tử khối trung bình của Mg là 24,327. Số khối các đồng vị lần lượt là 24, 25, 26. Phần trăm số nguyên tử của đồng vị 1 là 78,6%. Tìm % số nguyên tử mỗi đồng vị.
Phần trăm đồng vị thứ nhất \(^{24}Mg\) là 78,6%.
Gọi phần trăm đồng vị \(^{25}Mg\) và \(^{26}Mg\) lần lượt là a và b.
\(\Rightarrow\left\{{}\begin{matrix}78,6\%+a\%+b\%=100\%\\24\cdot78,6\%+25\cdot a\%+26\cdot b\%=24,327\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}a=10,1\%\\b=11,3\%\end{matrix}\right.\)
Câu 15: Cac bon trong tự nhiên là hỗn hợp các đồng vị C chiếm 98,89% và "C chiếm 1,11%. Khi có 35 nguyên tử C thì có: a) Bao nhiêu nguyên tử C? b) Bao nhiêu nguyên tử cacbon? Câu 16: Hiđro có 3 đồng vị là H(99,984%); H (0,016%); và ¡H (107%). Tổng số nguyên tử của hidro nếu trong hỗn hợp có chứa 500 nguyên tử đồng vị H ?
Câu 16:
Em gõ đề khúc 107% khó hiểu quá
hóa học 10 tính nguyên tử khối của đồng vị còn lại nếu biết nguyên tử khối trung bình của nguyên tố X là 79,91. biết X có hai đồng vị trong đó đồng vị 79X chiếm 54,5% số nguyên tử
Đặt x nguyên tử khối của đồng vị còn lại
Ta có : \(\overline{M}=\dfrac{54,5.79+\left(100-54,5\right).x}{100}=79,91\)
\(\rightarrow x=81\)
Vậy nguyên tử khối của đồng vị còn lại : \(^{81}X\)