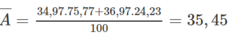![]() trong tự nhiên Clo có hai đồng vị là 35 và 37 .nguyên tử khối trung bình của Clo là 35,45 .hãy tính % về khối lượng của Clo 35 trong hợp chất CaCl2 (biết nguyên tử khối trung bình Ca là 40 )
trong tự nhiên Clo có hai đồng vị là 35 và 37 .nguyên tử khối trung bình của Clo là 35,45 .hãy tính % về khối lượng của Clo 35 trong hợp chất CaCl2 (biết nguyên tử khối trung bình Ca là 40 )![]()

Những câu hỏi liên quan
Trong tự nhiên clo có 2 đồng vị bền 35 17Cl và 37 17Cl . Nguyên tử khối trung bình của nguyên tố clo là 35,485. Tính thành phần phần trăm khối lượng của 37 17Cl có trong hợp chất HClO2
Nguyên tử khối trung bình của Clo là 35,5. Clo trong tự nhiên có hai đồng vị là 35 Cl và 37 Cl. Tính phần trăm về khối lượng của 37 Cl chứa trong HClO4 (với Hidro đồng vị là 1 H, oxi đồng vị là 16 O)
\(\%^{35}Cl=x\%\Rightarrow\%^{37}Cl=\left(100-x\right)\%\)
\(\overline{M}=\dfrac{35x+37\cdot\left(100\%-x\right)}{100\%}=35.5\left(g\text{/}mol\right)\)
\(\Rightarrow x=75\%\)
\(\%^{37}Cl_{\left(HClO_4\right)}=\dfrac{25\%\cdot37}{1+35.5+16\cdot4}\cdot100\%=9.2\%\)
Đúng 3
Bình luận (1)
Phần trăm đồng vị 35Cl = x, thì % đồng vị 37Cl = 100 - x
Ta có:
, vậy x = 75%.
Phần trăm khối lượng của 37Cl trong HClO4=
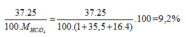
Đúng 1
Bình luận (2)
Clo có nguyên tử khối trung bình là 35,45. Hỏi có bao nhiêu nguyên tử của đồng vị Cl 17 35 trong 100 ml dung dịch HCl 0,1M?
Biết: Clo chỉ có hai đồng vị Cl 17 35 và Cl 17 37 ; số Avogadro N = 6,02.10^23
Clo trong tự nhiên có 2 đồng vị là 35 Cl và 37 Cl. Biết nguyên tử khối trung bình của Na và Cl lần lượt là 23 và 35,5. Tính phần trăm về khối lượng của 35 Cl trong NaCl.
Gọi phần trăm đồng vị của 35Cl là x
⇒ Phần trăm đồng vị của 37Cl là 100-x
Ta có: \(A=\dfrac{35x+37\left(100-x\right)}{100}=35,5\Rightarrow x=75\%\)
Phần trăm k/lg của 35Cl trong NaCl là:\(\dfrac{35.75\%}{23+35,5}.100\%=44,87\%\)
Đúng 2
Bình luận (1)
1.Trong các hợp chất thiên nhiên, nguyên tố clo gồm 2 đồng vị 35 17 Cl và 37 17 Cl; khối lượng nguyên tử trung bình của clo là 35, 5. Tính thành phần phần trăm các đồng vị của clo. 2.Trong một bình kín chứa 10lít nitơ và 10 lít hiđro ở nhiệt độ OoC và áp suất 10 atm. Sau phản ứng tổng hợp amoniac, đưa nhiệt độ về OoC . Tính áp suất trong bình sau phản ứng, biết rằng có 60% hiđro tham gia phản ứng.
Đọc tiếp
1.Trong các hợp chất thiên nhiên, nguyên tố clo gồm 2 đồng vị 35 17 Cl và 37 17 Cl; khối lượng nguyên tử trung bình của clo là 35, 5. Tính thành phần phần trăm các đồng vị của clo. 2.Trong một bình kín chứa 10lít nitơ và 10 lít hiđro ở nhiệt độ OoC và áp suất 10 atm. Sau phản ứng tổng hợp amoniac, đưa nhiệt độ về OoC . Tính áp suất trong bình sau phản ứng, biết rằng có 60% hiđro tham gia phản ứng.
Câu 8: Trong tự nhiên, clo có 2 đồng vị 35Cl và 37Cl. Nguyên tử khối trung bình của clo là 35,48u. Thành phần % theo khối lượng của đồng vị 37Cl trong CaCl2 (biết MCa=40) là bao nhiêu
Mong giúp mọi người giúp mình với
Giả sử : %số nguyên tử 35Cl và 37Cl lần lượt là : x , y
Ta có : \(x+y=1\)\(35x+37y=35.48\) \(\Rightarrow x=0.76\)\(y=0.24\)\(\%^{37}Cl=\dfrac{0.24\cdot37\cdot2}{40+35.48\cdot2}\cdot100\%=16\%\)
Đúng 1
Bình luận (0)
Clo tự nhiên là hỗn hợp của hai đồng vị :
Cl
35
có nguyên tử khối là 34,97.
Cl
37
có nguyên tử khối ià 36,97.Biết rằng đồng vị
Cl
35
hiếm 75,77% ; hãy tính nguyên tử khối trung bình của clo tự nhiên.
Đọc tiếp
Clo tự nhiên là hỗn hợp của hai đồng vị :
Cl 35 có nguyên tử khối là 34,97.
Cl 37 có nguyên tử khối ià 36,97.
Biết rằng đồng vị Cl 35 hiếm 75,77% ; hãy tính nguyên tử khối trung bình của clo tự nhiên.
Nguyên tử khối trung bình của clo là 35,5. Clo trong tự nhiên có 2 đồng vị là 35 Cl và 37Cl. Phần trăm khối lượng của 3717Cl chứa trong HClO4 ?(với hidro là đồng vị 11H, oxi là đồng vị 168O) là.
Tham thảo :
Phần trăm đồng vị 35Cl = x, thì % đồng vị 37Cl = 100 - x
Ta có:
![]() , vậy x = 75%.
, vậy x = 75%.
Phần trăm khối lượng của 37Cl trong HClO4= 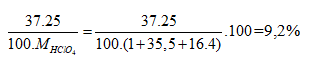
Đúng 0
Bình luận (0)
Trong tự nhiên, clo có 2 đồng vị: 35 Cl và 37 Cl . Số nguyên tử 35 Cl có trong 14,244
gam MgCl2 (Mg=24) là \(1.368\cdot10^{23}\). Cho hằng số Avogagro \(N_A=6\cdot10^{23}\). Tính
nguyên tử khối trung bình của clo.