Hoà tan hoàn toàn 2,4g kim loại A hóa trị II vào trong 100ml dung dịch HCl 1,5M. Sau phản ứng vẫn thấy còn một phần A chưa tan hết. Cũng 2,4g A trên nếu tác dụng với 125ml dung dịch HCl 2M thì thấy còn dư axit sau phản ứng. Xác đinh kim loại R.

Những câu hỏi liên quan
Cho 11,7 gam một kim loại X hóa trị II vào 350 ml dung dịch HCl 1M, khi phản ứng kết thúc ta thấy kim loại vẫn còn dư. Mặt khác để hòa tan hoàn toàn lượng kim loại trên phải cần chưa đến 200 ml dung dịch HCl 2M. Tìm X.
nHCl = 0,35 . 1 = 0,35 (mol)
\(X+2HCl\rightarrow XCl_2+H_2\)
0,175 0,35 0,175 0,175 (mol)
nHCl (pứ 2 ) = 0,2 . 2 = 0,4 (mol)
\(X+2HCl\rightarrow XCl_2+H_2\)
0,2 0,4
\(nX=0,175+0,2=0,375\left(mol\right)\)
=> \(MX=\dfrac{11,7}{0,375}=\) 31,2 .-. k ra là s
Đúng 3
Bình luận (0)
Cho 2,4 gam kim loại X hóa trị II vào 200 ml dung dịch HCl 0,75M thấy sau phản ứng vẫn còn một phần kim loại chưa tan hết. Cũng 2,4 gam X tác dụng với 250ml dung dịch HCl 1M thấy sau phản ứng vẫn còn axit dư. Kim loại X là?
- Khi cho 2,4g X vào 200ml ddHCl 0,75M
nHCl = 0,2.0,75 = 0,15 (mol)
....\(X+2HCl\rightarrow XCl_2+H_2\)
0,075.....0,15...............................(mol)
do X còn dư nên \(\dfrac{2,4}{X}>0,075\Leftrightarrow X< 32\) (1)
- Khi cho 2,4g X vào 250ml ddHCl 1M
nHCl = 0,25.1 = 0,25 (mol)
...\(X+2HCl\rightarrow XCl_2+H_2\)
\(\dfrac{2,4}{X}\)......\(\dfrac{4,8}{X}\)..............................(mol)
axit còn dư \(\Rightarrow\dfrac{4,8}{X}< 0,25\Leftrightarrow X>19,2\) (2)
Từ (1) và (2) \(\Rightarrow\) 19,2 < X < 32 mà X là kim loại hóa trị II \(\Rightarrow X=24\)
Vậy kim loại X là Mg
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 4g hỗn hợp X gồm Fe và kim loại hóa trị II vào dung dịch HCl dư thu được 2,24 lít khí H2 ở (đkt). Nếu dùng 2,4g kim loại hóa trị II hòa tan vào dung dịch HCl thì dùng không hết 0,5 mol dung dich HCl.
a. Xác định tên kim loại hóa trị II.
b. Tính thành phần % theo khối lượng của mỗi kim loại trong 4g hỗn hợp X
Hòa tan hoàn toàn 2,4g một kim loại X hóa trị II vào dung dịch HCl dư.Sau phản ứng thu được dung dịch A và 2,24l khí ở đktc.
a Xác định kim loại X
b, tính khối lượng muối khan thu được
c tính C % dung dịch thu được
\(n_{H_2}=\frac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH
\(X+2HCl\rightarrow XCl_2+H_2\)
0,1mol 0,2mol 0,1mol 0,1 mol
\(M_X=\frac{2,4}{0,1}=24\left(g\right)\)
Vậy kim loại X thuộc nguyên tố Mg
Đúng 0
Bình luận (0)
nH2=2,24/22,4=0,1 mol
X +2HCl =>XCl2 +H2
0,1 mol<= 0,1 mol<=0,1 mol
a) Từ PTHH=>nX=0,1 mol
MÀ mX=2,4(g)=>MX=24=>X là Mg
b) nXCl2=nMgCl2=0,1 mol=>mMgCl2=0,1.95=9,5g
c) đề bài thiếu dữ kiện em
Đúng 0
Bình luận (0)
b,\(Mg+2HCl\rightarrow MgCl_2+H_2\)
0,1mol 0,2mol 0,1mol 0,1mol
\(m_{MgCl_2}=95.0,1=9,4\left(g\right)\)
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Bài 7.Cho 16,2g kẽm oxit tác dụng với 100g dung dịch axit sunfuric 40%.Tính nồng độ phần trăm các chất có trong dung dịch sau khi pư kết thúc
Bài 8.Để hòa tan hoàn toàn 2,4g oxit kim loại hóa trị II cần dùng 10g dung dịch HCL 21,9%.Hỏi đó là oxit của kim loại nào?
Giúp mình với!Mình đang cần gấp
Bài 7:
Ta có: \(n_{ZnO}=\dfrac{16,2}{81}=0,2\left(mol\right)\)
\(m_{H_2SO_4}=100.40\%=40\left(g\right)\Rightarrow n_{H_2SO_4}=\dfrac{40}{98}=\dfrac{20}{49}\left(mol\right)\)
PT: \(ZnO+H_2SO_4\rightarrow ZnSO_4+H_2O\)
Xét tỉ lệ: \(\dfrac{0,2}{1}< \dfrac{\dfrac{20}{49}}{1}\), ta được H2SO4 dư.
Theo PT: \(n_{ZnSO_4}=n_{H_2SO_4\left(pư\right)}=n_{ZnO}=0,2\left(mol\right)\)
\(\Rightarrow n_{H_2SO_4\left(dư\right)}=\dfrac{20}{49}-0,2=\dfrac{51}{245}\left(mol\right)\)
Ta có: m dd sau pư = 16,2 + 100 = 116,2 (g)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{ZnSO_4}=\dfrac{0,2.161}{116,2}.100\%\approx27,71\%\\C\%_{H_2SO_4\left(dư\right)}=\dfrac{\dfrac{51}{245}.98}{116,2}.100\%\approx17,56\%\end{matrix}\right.\)
Đúng 2
Bình luận (0)
Bài 8:
Gọi oxit cần tìm là AO.
Ta có: \(m_{HCl}=10.21,9\%=2,19\left(g\right)\Rightarrow n_{HCl}=\dfrac{2,19}{36,5}=0,06\left(mol\right)\)
PT: \(AO+2HCl\rightarrow ACl_2+H_2O\)
Theo PT: \(n_{AO}=\dfrac{1}{2}n_{HCl}=0,03\left(mol\right)\)
\(\Rightarrow M_{AO}=\dfrac{2,4}{0,03}=80\left(g/mol\right)\)
\(\Rightarrow M_A+16=80\Rightarrow M_A=64\left(g/mol\right)\)
→ A là Cu.
Vậy: Đó là oxit của đồng.
Đúng 2
Bình luận (0)
Các bạn ơi giúp mình với, mình mới làm quen với dạng này nên còn lúng túng lắm !!!!!!!!!!
Đề: Hoà tan 4g hỗn hợp gồm Fe và một kim loại M hoá trị II vào dung dịch HCl thu được 2,24 l khí (dktc). Xác định tên kim loại M. Biết khi hoà tan 2,4g M vào 500ml dung dịch HCl 1M thì dung dịch thu được vẫn còn dư HCl
Hòa tan 4g hỗn hợp gồm kim loại: sắt và M hóa trị II vào dung dịch HCl thu được 2,24 lít khí H2. Nếu chỉ dùng 2,4g M cho vào dung dịch HCl thì không dùng hết 500ml dung dịch HCl 1M. Xác định tên kim loại M.
nH2=0,1 mol
Gọi R là khối lượng mol trung bình của Fe và kl hoá trị II
R + 2HCl ----> RCl2 + H2
-> R = 4/0,1 =40
-> M(kl)< 40 < 56(Fe) (1)
M + 2HCl -----> RCl + H2
0,5 0,5
nHCl=0,5mol
Theo đề bài: 2,4g KL hoá trị II không dùng hết 0,5 mol HCl
-> 2,4/M< 0,25
->M< 4,9 (2)
Từ (1) và (2) ta có:
9,6< M <40
Duwaj vào bảng THHH -> M là Mg (24)
Thấy đúng thì follow nhé fb : https://www.facebook.com/themlannua.haytinanh.7 ![]()
Đúng 1
Bình luận (1)
Mình cũng mới gặp bài này mới đây thôi,phương pháp này có thể sử dụng Bảng THHH có gì không hiểu lên hệ facebook mình : https://www.facebook.com/themlannua.haytinanh.7
Đúng 0
Bình luận (2)
Cho 2,4g kim loại A tác dụng với dung dịch HCl 7,3% vừa đủ sau khi phản ứng kết thúc thu được 2,24l H2(ở đktc).
a)Xác định kim loại A
b)Tính nồng độ % chất tan trong dung dịch mới
\(n_{H_2}=\dfrac{2.24}{22.4}=0.1\left(mol\right)\)
\(2A+2nHCl\rightarrow2ACl_n+nH_2\)
\(\dfrac{0.2}{n}.......................0.1\)
\(M_A=\dfrac{2.4}{\dfrac{0.2}{n}}=12n\left(\dfrac{g}{mol}\right)\)
\(BL:n=2\Rightarrow M=24\)
\(A:Mg\)
\(m_{MgCl_2}=0.1\cdot95=9.5\left(g\right)\)
\(m_{ddHCl}=\dfrac{0.2\cdot36.5}{7.3\%}=100\left(g\right)\)
\(m_{dd}=2.4+100-0.1\cdot2=102.2\left(g\right)\)
\(C\%_{MgCl_2}=\dfrac{9.5}{102.2}\cdot100\%=9.3\%\)
Đúng 2
Bình luận (0)
Cho 6,2 gam oxit của kim loại hóa trị I tác dụng với nước dư thu được dung dịch A có tính kiềm. Chia A thành 2 phần bằng nhau: Phần 1 tác dụng với 95ml dung dịch HCl 1M thấy dung dịch sau phản ứng làm xanh quỳ tím. Phần 2 tác dụng với 55ml dung dịch HCl 2M thấy dung dịch sau phản ứng làm đỏ quỳ tím. Công thức oxit kim loại đã dùng là: A.Li2O. B. Na2O. C.K2O. D.Rb2O.
Đọc tiếp
Cho 6,2 gam oxit của kim loại hóa trị I tác dụng với nước dư thu được dung dịch A có tính kiềm. Chia A thành 2 phần bằng nhau:
Phần 1 tác dụng với 95ml dung dịch HCl 1M thấy dung dịch sau phản ứng làm xanh quỳ tím.
Phần 2 tác dụng với 55ml dung dịch HCl 2M thấy dung dịch sau phản ứng làm đỏ quỳ tím.
Công thức oxit kim loại đã dùng là:
A.Li2O.
B. Na2O.
C.K2O.
D.Rb2O.
Gọi n M 2 O = a thì nMOH = 2a, mỗi phần có nMOH = a
Khi nHCl = 0,095 thì dung dịch sau phản ứng làm quỳ tím hóa xanh nên MOH dư => a > 0,095
Khi nHCl = 0,11 thì dung dịch sau phản ứng làm quỳ tím hóa đỏ nên HCl dư => a < 0,11
Có 0,095 < a < 0,11
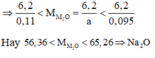
Đáp án B
Đúng 0
Bình luận (0)



































