Hòa tan ag tinh thể CuSO4.5H2O vào nước rồi cho tác dụng với dd Ba(NO3)2. Lọc kết tủa làm bay hơi dd nước lọc thu được 4,48g tinh thể muối Cu. Nung tinh thể đến khối lượng không đổi thấy khối lượng giảm 3,24g. Xác định CTHH của tinh thể muối Cu

Những câu hỏi liên quan
Cho 250 ml dd NaOH 1M tác dụng với dd CuSO4 0,5 M thu được kết tủa và nước lọc. Lọc kết tủa nung đến khối lượng không đổi. a) Viết Các PTHH . b) Tính khối lượng chất rắn thu được sau khi nung? c) Tính thể tích dd CuSO4 0,5 M cần phản ứng? d) Tính khối lượng chất tan có trong nước lọc? (Cho Cu= 64, H = 1 , S = 32, O = 16,Na = 23)
Một hh X gồm FeCl3 và CuCl2 hòa tan trong nước cho dd A. Chia A làm 2 phần bằng nhauPhần 1: Cho tác dụng với 0.5lit dd AgNO3 0,3M tao thành 17.22g kết tủaPhần 2: Cho tác dụng với một lượng NaOH 2M vừa đủ để thu được kết tủa lớn nhất. Lọc kết tủa đem nung đến khối lượng không đổi thu được một chất rắn nặng 4 gama) Chứng minh FeCl3 và CuCl2 đã tham gia pứ hết với AgNO3. Tính khối lượng FeCl3 và CuCl2 trong hh Xb) Tính dd NaOH 2M đã dùngc) Thêm m gam AlCl3 vào lượng hh X trên được hh Y. Hòa tan hết...
Đọc tiếp
Một hh X gồm FeCl3 và CuCl2 hòa tan trong nước cho dd A. Chia A làm 2 phần bằng nhau
Phần 1: Cho tác dụng với 0.5lit dd AgNO3 0,3M tao thành 17.22g kết tủa
Phần 2: Cho tác dụng với một lượng NaOH 2M vừa đủ để thu được kết tủa lớn nhất. Lọc kết tủa đem nung đến khối lượng không đổi thu được một chất rắn nặng 4 gam
a) Chứng minh FeCl3 và CuCl2 đã tham gia pứ hết với AgNO3. Tính khối lượng FeCl3 và CuCl2 trong hh X
b) Tính dd NaOH 2M đã dùng
c) Thêm m gam AlCl3 vào lượng hh X trên được hh Y. Hòa tan hết Y và thêm từ từ dd NaOH 2m. Khi thể tích NaOH 2M Thêm vào là 0.14lit thì kết tủa không thay đổi nữa. Tính khối lượng chất rắn thu được sau khi nung kết tủa và khối lượng mcua3 AlCl3 đã hte6m vào hh X
Hòa tan hoàn toàn 24.625g hh gồm KCl, MgCl2, NaCl vào nước, rồi thêm vào đó 300ml dd AgNO3 1.5M. Sau PỨ thu được dd A, kết tủa B. Cho Cho 2.4g Mg vào dd A, PỨ kết thúc lọc tách riêng chất rắn C và dd D. Cho toàn bộ chất rắn vào dd HCl loãng dư, sau PỨ thấy khối lượng chất rắn C giảm 1.92g. Thêm dd NaOH dư vào dd D, lọc lấy kết tủa đem nung đến khối lượng không đổi được 4g chất rắn E. Tính %m các muối có trong hh đầu.
Đọc tiếp
Hòa tan hoàn toàn 24.625g hh gồm KCl, MgCl2, NaCl vào nước, rồi thêm vào đó 300ml dd AgNO3 1.5M. Sau PỨ thu được dd A, kết tủa B. Cho Cho 2.4g Mg vào dd A, PỨ kết thúc lọc tách riêng chất rắn C và dd D. Cho toàn bộ chất rắn vào dd HCl loãng dư, sau PỨ thấy khối lượng chất rắn C giảm 1.92g. Thêm dd NaOH dư vào dd D, lọc lấy kết tủa đem nung đến khối lượng không đổi được 4g chất rắn E. Tính %m các muối có trong hh đầu.
Trong dd ban đầu:
K+_____a mol
Mg2+___b mol
Na+____c mol
Cl-_____a + 2b + c mol
mhhbđ = 74.5a + 95b + 58.5c = 24.625 g______(1)
nAgNO3 = 0.3*1.5 = 0.45 mol
Cho Mg vào A có phản ứng (theo gt) nên Ag(+) còn dư, Cl(-) hết. Rắn C gồm Ag và có thể cả Mg còn dư nữa. Thật vậy, khi cho rắn C vào HCl loãng thì khối lượng rắn bị giảm đi, chính do Mg pư, Ag thì không. Vậy mrắn C giảm = mMg chưa pư với A = 1.92 g.
=> nMg dư = 1.92/24 = 0.08 mol
=> nMg pư với A = 2.4/24 - 0.08 = 0.02 mol________(*)
Khi cho Mg vào A có pư:
Mg + 2Ag(+) ---> 2Ag(r) + Mg(2+)
0.02__0.04
=> nAg(+) pư với dd ban đầu = 0.45 - 0.04 = 0.41 mol
Ag(+) + Cl(-) ---> AgCl(r)
0.41___0.41
Có: nCl(-) = a + 2b + c = 0.41_____________(2)
Trong các cation trên, Mg(2+) và Ag(+) có pư với OH(-), tuy nhiên trong D chỉ có Mg(2+) nên kết tủa là Mg(OH)2:
Mg(2+) + 2OH(-) ---> Mg(OH)2
Khi nung:
Mg(OH)2 ---> MgO + H2O
Ta có: nMg(2+)trongD = nMgO = 4/40 = 0.1 mol
Trong đó 0.02 mol Mg(2+) được thêm vào bằng cách cho kim loại Mg vào (theo (*)), vậy còn lại 0.08 mol Mg(2+) là thêm từ đầu, ta có:
b = 0.08 mol_________________________(3)
(1), (2), (3) => a = 0.15, b = 0.08, c = 0.1
mKCl = 74.5*0.15 = 11.175 g
mMgCl2 = 95*0.08 = 7.6 g
mNaCl = 58.5*0.1 = 5.85 g
Đúng 0
Bình luận (0)
Hòa tan 26,64 gam chất tinh thể muối sunfat của kim loại M vào nước dung dịch X. Cho X tác dụng với dung dịch NH3 vừa đủ thu được kết tủa Y, nung Y ở nhiệt độ cao đến khối lượng không đổi được 4,08 gam oxit. Mặt khác, cho X tác dụng với dung dịch BaCl2 dư được 27,96 gam kết tủa. Công thức tnh thể trên là A.CuSO4.6H2O B. Fe2(SO4)3.12H2O C. Al2(SO4)3.24H2O D. Al2(SO4)3.18H2O
Đọc tiếp
Hòa tan 26,64 gam chất tinh thể muối sunfat của kim loại M vào nước dung dịch X. Cho X tác dụng với dung dịch NH3 vừa đủ thu được kết tủa Y, nung Y ở nhiệt độ cao đến khối lượng không đổi được 4,08 gam oxit. Mặt khác, cho X tác dụng với dung dịch BaCl2 dư được 27,96 gam kết tủa. Công thức tnh thể trên là
A.CuSO4.6H2O
B. Fe2(SO4)3.12H2O
C. Al2(SO4)3.24H2O
D. Al2(SO4)3.18H2O
Câu 1: Tính khối lượng muối NaNO3 cần lấy để khi hòa tan vào 170 g nước thì thu được dung dịch có nồng độ 15 %
Câu 2: Hòa tan 75 g tinh thể CuSO4.5H2O vào trong nước thu được 900 ml dd CuSO4. Tính CM dd này
Câu 3: Khối lượng riêng dd CuSO4 là 1,206 g/ml. Đem cô cạn 414,594 ml dd này thu được 140,625 g tinh thể CuSO4.5H2O . Tính nồng độ mol và nồng độ % dd nói trên.
Câu 1 :
Khối lượng dung dịch là : \(m_{ct}+170\)
Gọi khối lượng muối \(NaNO_3\)cần dùng là x
Ta có :\(m_{ct}=\frac{C\%.m_{dd}}{100}\)
hay \(x=\frac{15.\left(x+170\right)}{100}\)
Ta tính được x=30 (g)
Vậy khối lượng \(NaNO_3\)cần lấy là 30 g
Đúng 1
Bình luận (0)
Câu 2 :
Số mol \(CuSO_4.5H_2O\)là :
\(n_{CuSO_4.5H_2O}=\frac{m}{M}=\frac{75}{250}=0,3\left(mol\right)\)
\(\Rightarrow n_{CuSO_4}=0,3\left(mol\right);V_{dd}=900ml=0,9l\)
\(C_{M_{dd}}=\frac{n}{V}=\frac{0,3}{0,9}=\frac{1}{3}M\)
Vậy...
Đúng 0
Bình luận (0)
Lấy 10 g bột đá có thành phần chính là MgCO3 và CaCO3 cho tác dụng với dd HCl dư, thu được 2,296 lít CO2(đktc). Lọc bỏ tạp chất không tan. Cho toàn bộ phần nước lọc phản ứng với dd NaOH loãng, dư, lọc kết tủa. Nung kết tủa đến khối lượng không đổi, thu được 2,4g chất rắn.a. Tính khối lượng mỗi chất có trong hỗn hợp.b.Tính phần trăm khối lượng các chất có trong hỗn hợp ban đầu
Đọc tiếp
Lấy 10 g bột đá có thành phần chính là MgCO3 và CaCO3 cho tác dụng với dd HCl dư, thu được 2,296 lít CO2(đktc). Lọc bỏ tạp chất không tan. Cho toàn bộ phần nước lọc phản ứng với dd NaOH loãng, dư, lọc kết tủa. Nung kết tủa đến khối lượng không đổi, thu được 2,4g chất rắn.
a. Tính khối lượng mỗi chất có trong hỗn hợp.
b.Tính phần trăm khối lượng các chất có trong hỗn hợp ban đầu
a)
\(MgCO_3+2HCl\rightarrow MgCl_2+CO_2+H_2O\)
\(CaCO_3+2HCl\rightarrow CaCl_2+CO_2+H_2O\)
=> \(n_{MgCO_3}+n_{CaCO_3}=\dfrac{2,296}{22,4}=0,1025\)
\(MgCl_2+2NaOH\rightarrow Mg\left(OH\right)_2\downarrow+2NaCl\)
\(Mg\left(OH\right)_2\underrightarrow{t^o}MgO+H_2O\)
\(n_{MgO}=\dfrac{2,4}{40}=0,06\left(mol\right)\)
=> \(n_{MgCO_3}=0,06\left(mol\right)\)
=> \(n_{CaCO_3}=0,0425\left(mol\right)\)
=> \(\left\{{}\begin{matrix}m_{MgCO_3}=0,06.84=5,04\left(g\right)\\m_{CaCO_3}=0,0425.100=4,25\left(g\right)\end{matrix}\right.\)
b)
\(\left\{{}\begin{matrix}\%m_{MgCO_3}=\dfrac{5,04}{10}.100\%=50,4\%\\\%m_{CaCO_3}=\dfrac{4,25}{10}.100\%=42,5\%\end{matrix}\right.\)
Đúng 2
Bình luận (0)
\(MgCO_3 + 2HCl \rightarrow MgCl_2 + CO_2 + H_2O\) (1)
\(CaCO_3 + 2HCl \rightarrow CaCl_2 + CO_2 + H_2O\) (2)
\(MgCl_2 + 2NaOH \rightarrow Mg(OH)_2 + 2NaCl\) (3)
\(Mg(OH)_2 -t^o-> MgO + H_2O\) (4)
\(n_{CO_2}= \dfrac{2,296}{22,4}=0,1025 mol\)
\(n_{MgO}= \dfrac{2,4}{40}=0,06 mol\)
Theo PTHH: \(n_{CO_2(1)}= n_{MgCl_2}= n_{Mg(OH)_2}=n_{MgO}= 0,06 mol\)\(=n_{MgCO_3}\)
\(\Rightarrow n_{CO_2(2)}= n_{CO_2} - n_{CO_2(1)}= 0,1025 - 0,06=0,0425 mol\)
Theo PTHH (1): \(n_{CaCO_3}= n_{CO_2(2)}= 0,0425 mol\)
\(m_{MgCO_3}= 0,06 . 84=5,04 g\)
\(m_{CaCO_3}= 0,0425 . 100= 4,25 g\)
b)
%mMgCO3= \(\dfrac{5,04}{10}\). 100%=50,4 %
%mCaCO3=\(\dfrac{4,25}{10}\).100%= 42,5%
Đúng 1
Bình luận (1)
Trộn dung dịch có hòa tan 0,2 mol CuCl2 với dung dịch có hòa tan 20g NaOH . Lọc hỗn hợp các chất sau phản ứng được chất kết tủa ( chất rắn không tan ) và nước lọc . Nung kết tủa đến khối lượng không đổi
a) Tinh khối lượng chất rắn sau khi nung
b) Tính khối lượng các chất có trong nước lọc
a) \(n_{NaOH}=\dfrac{20}{40}=0,5\left(mol\right)\)
PTHH: CuCl2 + 2NaOH --> Cu(OH)2 + 2NaCl
Xét tỉ lệ: \(\dfrac{0,2}{1}< \dfrac{0,5}{2}\) => CuCl2 hết, NaOH dư
PTHH: CuCl2 + 2NaOH --> Cu(OH)2 + 2NaCl
0,2------>0,4-------->0,2------->0,4
Cu(OH)2 --to--> CuO + H2O
0,2-------------->0,2
=> mCuO = 0,2.80 = 16(g)
b)
\(\left\{{}\begin{matrix}m_{NaOH\left(dư\right)}=20-0,4.40=4\left(g\right)\\m_{NaCl}=0,4.58,5=23,4\left(g\right)\end{matrix}\right.\)
Đúng 3
Bình luận (0)
Hòa tan hoàn toàn 1,28 g Cu vào 12,6 gam dd NO3 60% thu được dung dịch X. Cho X tác dụng hoàn toàn với 105ml dung dịch KOH 1M, sau đó lọc bỏ kết tủa thu được dung dịch Y. Cô cạn Y được chất rắn Z. Nung Z đến khối lượng không đổi, thu được 8,78 gam chất rắn. Nồng độ phần trăm của Cu(NO3)2 trong X là: A. 28,66% B. 29,89%. C. 30,08% D. 27,09%
Đọc tiếp
Hòa tan hoàn toàn 1,28 g Cu vào 12,6 gam dd NO3 60% thu được dung dịch X. Cho X tác dụng hoàn toàn với 105ml dung dịch KOH 1M, sau đó lọc bỏ kết tủa thu được dung dịch Y. Cô cạn Y được chất rắn Z. Nung Z đến khối lượng không đổi, thu được 8,78 gam chất rắn. Nồng độ phần trăm của Cu(NO3)2 trong X là:
A. 28,66%
B. 29,89%.
C. 30,08%
D. 27,09%
Đáp án A
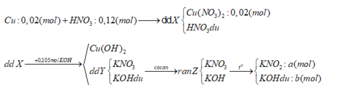
∑nKOH = a + b = 0,105 (1)
∑ mrắn = 85a + 56b = 8,78 (2)
Từ (1) và (2) => a = 0,1 (mol) ; b = 0,005 (mol)
nKNO3 tạo ra từ Cu(NO3)2 = 0,04 (mol)
=> nKNO3 tạo ra từ HNO3 dư = 0,1 – 0,04 = 0,06 (mo)
=> nHNO3 dư = 0,12- 0,06 = 0,06 (mol)
=> nHNO3 bị khử = 0,06 – 0,02.2 = 0,02 (mol)
Với ne( Cu nhường) = 2.nCu = 0,04 (mol) => Trung bình mỗi N+5 nhận 0,04/0,02 = 2e
=> Tạo NO2 (1e) và NO ( 3e)
=> nNO = nNO2 = 0,02/ 2= 0,01(mol)
Vậy mdd X = mCu + mdd HNO3 – m khí = 1,28 + 12,6 – 0,01.30 – 0,01.46 = 13,12 (g)
=> C% Cu(NO3)2 = [( 0,02.188) : 13,12].100% = 28,66%
Đúng 0
Bình luận (0)
Cho 27,2g dd CuCl2 td với 20g NaOH. Lọc hỗn hợp chất sau p/ ứng được kết tủa và nước lọc. Nung kết tủa đến khối lượng không đổi
a) Viết PTHH
b) Tính KL chất rắn thu được sau khi nung
c) Tính khối lượng các chất tan có trong nước lọc
\(n_{NaOH}=\dfrac{20}{40}=0,5\left(mol\right)\)
a) \(CuCl_2+2NaOH\rightarrow Cu\left(OH\right)_2+2NaCl\left(1\right)\)
\(Cu\left(OH\right)_2\xrightarrow[t^o]{}CuO+H_2O\left(2\right)\)
b) \(Pt\left(1\right):n_{Cu\left(OH\right)2}=\dfrac{1}{2}n_{NaOH}=0,25\left(mol\right)\)
\(Pt\left(2\right):n_{Cu\left(OH\right)2}=n_{CuO}=0,25\left(mol\right)\Rightarrow m_{Cu}=0,25.64=16\left(g\right)\)
c) Pt(1) : \(n_{NaOH}=n_{NaCl}=0,5\left(mol\right)\Rightarrow m_{NaCl}=0,5.58,5=29,25\left(g\right)\)
Đúng 3
Bình luận (0)
























