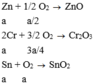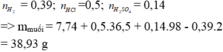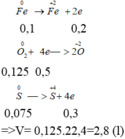Đốt cháy x gam hh 3 kim loại Mg , Al , Fe bằng 0,8 mol O2 , thu được 37,4 gam hh rắn B và còn lại 0,2 mol O2 . Hoà tan 37,4 gam hh B bằng y lít dd H 2SO4 2 M ( vừa đủ ) , thu được z gam hh muối khan . Tính x, y,z .

Những câu hỏi liên quan
Cho hh x gồm 3 este đơn chức .Đốt cháy m gam x cần vừa đủ 0.465 mol O2 , sản phẩm cháy thu đc chứa x mol CO2.Thủy phân m gam x trong 90ml dd NaOH 1M ( vừa đủ ) thì thu được 8.86 gam hh muối Y và ancol Z no đơn hở . Đem đốt cháy hoàn toàn hh muối Y thì cần vừa đủ 7.392 l O2 . x là
Đốt cháy hỗn hợp gồm 1,92 gam Mg và 4,48 gam Fe với khí X gồm O2 và Cl2 sau pư chỉ thu được hh Y gồm các oxit và muối clorua ( không còn khí dư). Hòa tan Y bằng một lượng vừa đủ 120 ml dd HCl 2M, thu được dd Z. Cho AgNO3 dư vào dd Z thu được 56,69 gam kết tủa. Tính % thể tích clo trong hỗn hợp X A. 76,7% B. 56,36% C. 51,72% D. 53,85%
Đọc tiếp
Đốt cháy hỗn hợp gồm 1,92 gam Mg và 4,48 gam Fe với khí X gồm O2 và Cl2 sau pư chỉ thu được hh Y gồm các oxit và muối clorua ( không còn khí dư). Hòa tan Y bằng một lượng vừa đủ 120 ml dd HCl 2M, thu được dd Z. Cho AgNO3 dư vào dd Z thu được 56,69 gam kết tủa. Tính % thể tích clo trong hỗn hợp X
A. 76,7%
B. 56,36%
C. 51,72%
D. 53,85%
Đáp án : D
nMg = 0,08 mol ; nFe = 0,08 mol
Khi phản ứng với X thì có x mol Cl2 và y mol O2 phản ứng
Giả sử tạo a mol Fe2+ và (0,08 – a) mol Fe3+
Bảo toàn điện tích : 2.0,08 + 2a + 3(0,08 – a) = 2x + 4y
Hòa tan Y bằng HCl : 2Cl thay thế 1 O => nO = ½ nHCl = 0,12 mol = 2y
=> 0,4 – a = 2x + 4.0,06 (1)
,Sau đó : phản ứng với AgNO3 tạo : (2x + 0,24) mol AgCl và a mol Ag
=> 56,69 = 143,5(2x + 0,24) + 108a (2)
Từ (1),(2) => x = 0,07 ; a = 0,02 mol
=> %VCl2(X) = 53,85%
Đúng 0
Bình luận (0)
Cho 11,5 gam hh ( Na , Mg, Al ) hoà tan vào nước thu được 4,48 lit khí đo ở đktc , 6,15 gam chất rắn không tan và dd Y. lấy chất rắn không tan tavs dụng với dd HCl dư thu được 0.275 mol H2 . Tính % về khối lượng kim loại Na, Mg , Al trong 11,5 gam ban đầu
na+2h20->2naoh+h2
nh2=4.48/22.4=0.2mol
->nNa=0.2mol
bt e
2nMg+3nAl=2*0.275
bt kl
24nMg+27nAl=6.15
->nMg=0.2mol
nAl=0.05mol
->kl tung cai roi tinh phan tram
Đúng 0
Bình luận (1)
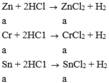
Cho m gam hh bột X gồm ba kim loại Zn, Cr, Sn có số mol bằng nhau t/d hết với lượng dư dd HCl loãng, nóng thu được dd Y và khí H2. Cô cạn dd Y thu được 8,98 gam muối khan. Nếu cho m gam hh X t/d hoàn toàn với O2 (dư) để tạo hh 3 oxit thì thể tích khí O2 (đktc) pư là A. 2, 016 lít. B. 1,008 lít. C. 0,672 lít. D. 1,344 lít.
Đọc tiếp
Cho m gam hh bột X gồm ba kim loại Zn, Cr, Sn có số mol bằng nhau t/d hết với lượng dư dd HCl loãng, nóng thu được dd Y và khí H2. Cô cạn dd Y thu được 8,98 gam muối khan. Nếu cho m gam hh X t/d hoàn toàn với O2 (dư) để tạo hh 3 oxit thì thể tích khí O2 (đktc) pư là
A. 2, 016 lít.
B. 1,008 lít.
C. 0,672 lít.
D. 1,344 lít.
22. Hoà tan 5,5 gam hh 2 kim loại Al, Fe trong 500 ml dd HCl vừa đủ thu được 4,48 lít khí đktc
a. Tính % khối lượng 2 kim loại b. Tính CM dd HCl
\(a.n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\ 2Al+6HCl\rightarrow2AlCl_3+3H_2\\ a............3a.......a.........1,5a\left(mol\right)\\ Fe+2HCl\rightarrow FeCl_2+H_2\\ b.........2b........b.........b\left(mol\right)\\ \rightarrow\left\{{}\begin{matrix}27a+56b=5,5\\1,5a+b=0,2\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,1\\b=0,05\end{matrix}\right.\\ \rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{27.0,1}{5,5}.100\approx49,091\%\\\%m_{Fe}=\dfrac{0,05.56}{5,5}.100\approx50,909\%\end{matrix}\right.\\ b.C_{MddHCl}=\dfrac{3a+2b}{0,5}=\dfrac{3.0,1+2.0,05}{0,5}=0,8\left(M\right)\)
Đúng 2
Bình luận (1)
Hoà tan hết 7,74 gam hh bột Mg, Al bằng 500 ml dd hh HCl 1M và H2SO4 0,28M thu được dd X và 8,736 lít khí H2 (ở đktc). Cô cạn dd X thu được lượng muối khan là A. 38,93 gam. B. 103,85 gam. C. 25,95 gam. D. 77,86 gam.
Đọc tiếp
Hoà tan hết 7,74 gam hh bột Mg, Al bằng 500 ml dd hh HCl 1M và H2SO4 0,28M thu được dd X và 8,736 lít khí H2 (ở đktc). Cô cạn dd X thu được lượng muối khan là
A. 38,93 gam.
B. 103,85 gam.
C. 25,95 gam.
D. 77,86 gam.
Nhiệt phân 98 gam KClO3 (có xt MnO2) sau một thời gian thu được 93,2 gam chất rắn và khí A. Cho toàn bộ lượng khí A pư hết với hh kim loại X gồm Mg , Fe thu đc hh chất rắn Y cân nặng 15,6 gam . Hòa tan hoàn toàn hh Y bằng dd H2SO4 đặc nóng dư thu đc 0,56 lít SO2 ( đktc, sp khử duy nhất) .Tính thành phần % khối lượng của Mg trong hh
23. Hoà tan 20 gam hh gồm Ag, Zn, Mg trong dd H2SO4 0,5 M (vừa đủ) thu được 6,72 lít H2 đktc và 8,7 gam kim loại không tan
a. Tính % khối lượng mỗi KL b. Tính V ml dd H2SO4
a.
\(m_{Ag}=m_{k.tan}=8,7\left(g\right)\\ m_{Zn,Mg}=20-8,7=11,3\left(g\right)\\ \left\{{}\begin{matrix}n_{Zn}=a\left(mol\right)\\n_{Mg}=b\left(mol\right)\end{matrix}\right.\left(a,b>0\right)\\Zn+H_2SO_4\rightarrow ZnSO_4+H_2\\ Mg+H_2SO_4\rightarrow MgSO_4+H_2\\ \rightarrow\left\{{}\begin{matrix}65a+24b=11,3\\a+b=0,3\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,1\\b=0,2\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%m_{Ag}=\dfrac{8,7}{20}.100=43,5\%\\\%m_{Mg}=\dfrac{24.0,2}{20}.100=24\%\\\%m_{Zn}=\dfrac{0,1.65}{20}.100=32,5\%\end{matrix}\right.\)
b.
\(n_{H_2SO_4\left(tổng\right)}=a+b=0,3\left(mol\right)\\ V_{ddH_2SO_4\left(tổng\right)}=\dfrac{0,3}{0,5}=0,6\left(lít\right)=600\left(ml\right)\)
Đúng 2
Bình luận (1)
Trộn 5,6 gam bột sắt với 2,4 gam bột lưu huỳnh rồi nung nóng (trong điều kiện không có không khí), thu được hh rắn M. Cho M t/d với lượng dư dd HCl, giải phóng hh khí X và còn lại một phần không tan G. Để đốt cháy hoàn toàn X và G cần vừa đủ V lít khí O2 (ở đktc). Giá trị của V là A. 2,80 B. 3,36 C. 3,08 D. 4,48
Đọc tiếp
Trộn 5,6 gam bột sắt với 2,4 gam bột lưu huỳnh rồi nung nóng (trong điều kiện không có không khí), thu được hh rắn M. Cho M t/d với lượng dư dd HCl, giải phóng hh khí X và còn lại một phần không tan G. Để đốt cháy hoàn toàn X và G cần vừa đủ V lít khí O2 (ở đktc). Giá trị của V là
A. 2,80
B. 3,36
C. 3,08
D. 4,48