Hỗn hợp X gồm N2 và H2 có dX/H2 =4,9. Cho X vào bình kín rồi nung nóng ở nhiệt độ thích hợp một thời gian được hỗn hợp khí Y có dY/H2 =6,125.Tính hiệu suất phản ứng.
Mình cần gấp lắm, mọi người giúp mình với
Một hỗn hợp khí X gồm 2 khí N2 và H2 có tỉ khối so với H2 bằng 4,9. Đun nóng hỗn hợp X một thời gian trong bình kín (có bột Fe làm xúc tác), thu được hỗn hợp khí Y có tỉ khối so với H2 bằng 6,125. Hiệu suất của phản ứng tổng hợp NH3 là?
A. 33,33%
B. 42,85%
C. 66,67%
D. 30%
Đáp án B
Áp dụng phương pháp đường chéo cho hỗn hợp X:
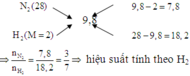
Cách 1: Gọi số mol N2 là 3x thì số mol H2 là 7x ⇒ tổng số mol hỗn hợp X là 3x + 7x = 10x
Thay vào công thức:
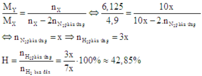
Cách 2: Áp dụng công thức tính nhanh với trường hợp x < 3y:
Hiệu suất phản ứng:
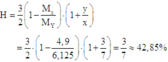
x là hỗn hợp so2 và o2 có dx/h2 = 22,4 . nung nóng x 1 thời gian trong bình kín có xúc tác thích hợp thu được hỗn hợp y có dy/h2 =26,67. xác định hiệu suất phản ứng tổng hợp so2
SO2 + 1/2O2 ---> SO3
Gọi a, b tương ứng là số mol SO2 và O2 trong hh X: 64a + 32b = 22,4.2.(a + b).
Hay b = 1,5a.
Giả sử có x mol tham gia phản ứng, do đó hh Y gồm: SO3 (x mol); SO2 (a-x); O2 (1,5a-0,5x).
80x + 64(a-x) + 32(1,5a-0,5x) = 26,67.2.(x + a-x + 1,5a-0,5x). Thu được: x = 0,8a.
Vậy: H = x/a = 80%.
Trong bình kín chứa đầy hỗn hợp khí X gồm C2H4 và H2 với lượng dư bột Ni, dX/H2 = 6,2 . Đun nóng bình một thời gian thu được hỗn hợp khí Y,dY/H2 = 8,0 . Hiệu suất của phản ứng hiđro hoá C2H4 là
A. 37,50%.
B. 43,75%.
C. 62,50%.
D. 56,25%.
Đáp án D

Giả sử ban đầu có 40 mol khí, sau phản ứng sẽ có 31 mol khí.
Sử dụng đường chéo, ta tính được
Do sau phản ứng vẫn thu được hỗn hợp khí nên H2 sẽ dư
Số mol H2 phản ứng: 40-31=9
Hiệu suất phản ứng: H=
9
16
=
56
,
25
%
Một hỗn hợp khí X gồm N2 và H2 có tỉ khối so với hiđro là 4,9. Cho hỗn hợp đi qua xúc tác thích hợp, nung nóng được hỗn hợp mới Y có tỉ khối so với hiđro là 6,125. Hiệu suất tổng hợp NH3 là:
A. 42,85%
B. 16,67%
C. 40%
D. 33,33%
Đáp án A.
Giả sử ban đầu hỗn hợp có 1 mol trong đó có x mol N2 và y mol H2
Ta có x + y =1 mol (1)

→28x+ 2y= 9,8 gam (2)
Giải hệ gồm (1) và (2) suy ra x= 0,3 và y= 0,7
N2+ 3H2 ⇌ 2NH3
Do  nên hiệu suất tính theo H2
nên hiệu suất tính theo H2
Đặt số mol H2 phản ứng là a mol
N2+ 3H2 ⇌ 2NH3
Ban đầu 0,3 0,7 mol
Phản ứng a/3 a 2a/3 mol
Sau pứ (0,3-a/3) (0,7-a) 2a/3 mol

cho 50l hỗn hợp khí X gồm N2 và H2 vào bình kín ( không có không khí ) . Tiến hành tổng hợp khí Amoniac ở điều khiện thích hợp : N2 + H2 --> NH3 . Sau một thời gian phản ứng đưa về điều kiện nhiệt độ , áp suất ban đầu thì thu được 44 lít hỗn hợp khí Y có 25% thể tích khí N2 . Thêm vào Y 6 lít N2O ở cùng điều kiện được hỗn hợp Z
a) Tính thành phần % theo thể tích từng khí trong X
b) Tính khối lượng của 11,2 lít hỗn hợp Z ở đktc
a) Giả sử các khí đo ở điều kiện sao cho 1 mol khí chiếm thể tích 1 lít
Gọi số mol N2, H2 ban đầu là a, b (mol)
=> a + b = 50 (1)
Gọi số mol N2 pư là x (mol)
PTHH: N2 + 3H2 --to,xt--> 2NH3
Trc pư: a b 0
Pư: x---->3x----------->2x
Sau pư (a-x) (b-3x) 2x
=> a + b - 2x = 44
=> x = 3 (mol)
Có \(n_{N_2\left(sau.pư\right)}=a-x=44.25\%=11\left(mol\right)\)
=> a = 14 (mol)
=> b = 36 (mol)
\(\left\{{}\begin{matrix}\%V_{N_2}=\dfrac{14}{50}.100\%=28\%\\\%V_{H_2}=\dfrac{36}{50}.100\%=72\%\end{matrix}\right.\)
Y chứa \(\left\{{}\begin{matrix}N_2:11\left(mol\right)\\H_2:27\left(mol\right)\\NH_3:6\left(mol\right)\end{matrix}\right.\)
Z chứa \(\left\{{}\begin{matrix}N_2:11\left(mol\right)\\H_2:27\left(mol\right)\\NH_3:6\left(mol\right)\\N_2O:6\left(mol\right)\end{matrix}\right.\)
\(Z\left\{{}\begin{matrix}\%V_{N_2}=\dfrac{11}{11+27+6+6}.100\%=22\%\\\%V_{H_2}=\dfrac{27}{11+27+6+6}.100\%=54\%\\\%V_{NH_3}=\dfrac{6}{11+27+6+6}.100\%=12\%\\\%V_{N_2O}=\dfrac{6}{11+27+6+6}.100\%=12\%\end{matrix}\right.\)
b)
11,2 lít hh Z ở đktc chứa \(\left\{{}\begin{matrix}n_{N_2}=\dfrac{11,2.22\%}{22,4}=0,11\left(mol\right)\\n_{H_2}=\dfrac{11,2.54\%}{22,4}=0,27\left(mol\right)\\n_{NH_3}=\dfrac{11,2.12\%}{22,4}=0,06\left(mol\right)\\n_{N_2O}=\dfrac{11,2.12\%}{22,4}=0,06\left(mol\right)\end{matrix}\right.\)
=> mZ = 0,11.28 + 0,27.2 + 0,06.17 + 0,06.44 = 7,28 (g)
Hỗn hợp khí X gồm N2 và H2 có tỉ khối so với H2 là 3,6. Nung nóng X một thời gian trong bình kín (có bột Fe làm xúc tác), thu được hỗn hợp khí Y có tỉ khối đối với H2 là 4. Hiệu suất của phản ứng tổng hợp NH3 là
A. 36%
B. 25%
C. 50%
D. 40%
Hỗn hợp khí X gồm N2 và H2 có tỉ khối so với H2 là 3,6. Nung nóng X một thời gian trong bình kín (có bột Fe làm xúc tác), thu được hỗn hợp khí Y có t khối đối với H2 là 4. Hiệu suất của phản ứng tổng hợp NH3 là
A. 36%.
B. 25%.
C. 50%.
D. 40%.
Hỗn hợp ban đầu chứa 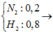 Hiệu suất tính theo N2
Hiệu suất tính theo N2
![]()
Đáp án B
Hỗn hợp khí X gồm N2 và H2 có tỉ khối so với H2 là 3,6. Nung nóng X một thời gian trong bình kín (có bột Fe làm xúc tác), thu được hỗn hợp khí Y có tỉ khối đối với H2 là 4. Hiệu suất của phản ứng tổng hợp NH3 là
A. 36%.
B. 25%.
C. 50%.
D. 40%.
Đáp án B
Hỗn hợp ban đầu chứa N 2 : 0 , 2 H 2 : 0 , 8
→ Hiệu suất tính theo N2.
nsau = 3,6/4 = 0,9 → N2 phản ứng = 0,05 → H = 25%
X là hỗn hợp của N2 và H2 có tỉ khối so với H2 là 4,25. Nung nóng X một thời gian trong bình kín có xúc tác phù hợp thu được hỗn hợp khí Y có tỉ khối Y so với X bằng 0,7. Hiệu suất của phản ứng tổng hợp NH3 là:
A. 50%
B. 40%
C. 20%
D. 60%
MX = 8,5 . Theo qui tắc đường chéo ta có : 3n N2 = nH2 => Chọn n H2 = 3 mol => n N2 = 1 mol
Xét cân bằng: N2 + 3H2 ó 2NH3
Số mol ban đầu 1 3
Số mol phản ứng x 3x 2x Số mol cân bằng (1-x) (3-3x) 2x Số mol sau phản ứng = (4 – 2x) mol
=>dY/X = nX/nY (do khối lượng chất trong hỗn hợp không đổi)
=> 0,7.4 = 4-2x => x = 0,6 mol
=>H% = 60%
=>D