Dung dịch A hỗn hợp NaOh và Ba(OH)2. Để trung hòa 50ml dung dịch A cần dùng 60ml dung dịch HCl 0.1M. Khi cho 50ml dung dịch A tác dụng với 1 lượng dư Na2CO3 thấy tạo thành 0.197 kết tủa. Tính nồng độ mol của mỗi chất trong dung dịch A.

Những câu hỏi liên quan
Dung dịch A hỗn hợp NaOh và Ba(OH)2. Để trung hòa 50ml dung dịch A cần dùng 60ml dung dịch HCl 0.1M. Khi cho 50ml dung dịch A tác dụng với 1 lượng dư Na2CO3 thấy tạo thành 0.197 kết tủa. Tính nồng độ mol của mỗi chất trong dung dịch A. Ai giải giúp em được không
gọi nồng độ mol của \(NaOH\) và \(Ba\left(OH\right)_2\) lần lược là : \(a;b\)
ta có : \(\dfrac{NaOH}{0,05a}\dfrac{\rightarrow}{ }\dfrac{Na^+}{ }\dfrac{+}{ }\dfrac{OH^-}{0,05a}\)
\(\dfrac{Ba\left(OH\right)_2}{0,05b}\dfrac{\rightarrow}{ }\dfrac{Ba^{2+}}{ }\dfrac{+}{ }\dfrac{2OH^-}{0,1b}\)
\(\dfrac{HCl}{0,006}\dfrac{\rightarrow}{ }\dfrac{H^+}{0,006}\dfrac{+}{ }\dfrac{Cl^-}{ }\)
\(\Rightarrow\dfrac{H^+}{0,006}\dfrac{+}{ }\dfrac{OH^-}{0,006}\dfrac{\rightarrow}{ }\dfrac{H_2O}{ }\) (để trung hòa)
\(\Rightarrow0,05a+0,1b=0,006\)
ta có : \(Na_2CO_3+NaOH\rightarrow khôngphảnứng\)
\(\dfrac{Ba\left(OH\right)_2}{0,001}\dfrac{+}{ }\dfrac{Na_2CO_3}{ }\dfrac{\rightarrow}{ }\dfrac{2NaOH}{ }\dfrac{+}{ }\dfrac{BaCO_3}{0,001}\)
\(\Rightarrow0,05a=0,001\Leftrightarrow a=0,02\left(M\right)\) \(\Rightarrow\) \(b=0,05\)
vậy .....................................................................................................................................
Đúng 0
Bình luận (0)
Cho m1 gam hỗn hợp gồm NaCO3 và K2CO3 , trong đó khối lượng K2CO3 gấp 2,604 lần khối lượng K2CO3.Hòa tan hỗn hợp trên trong 61,8 gam nước thu được dung dịch A.Cho dd A tác dụng với HXl dư ,khí tạo thành được hấp thụ bởi 500ml đ Ba(OH)2 0,5M thu được m2 gam kết tủa . Lọc kết tủa dung dịch được trung hòa bởi 50ml dung dịch NaOH 2M
a) Tính m1,m2
b) Tính C% của 2 muối trong dung dịch A
a/ A+ HCl
CO3 2- + 2H+ ---> H2O+ CO2
dd B trung hòa bởi NaOH--> trong B có Ba(HCO3)2
CO2 + Ba(OH)2 --> BaCO3 + H2O
0.2<---0.25-0.05-------->0.2
2Co2+ Ba(OH)2--> Ba(HCO3)2
0.1<--------0.05<---------0.05
Ba(HCO3)2+ 2NaOH---> BaCO3+ Na2CO3+ 2H2O
0.05<-------------0.1
--> m2= 0.2*197=39,4g
Na2CO3 va K2CO3 : x,y mol
x+y=0.3
138y=106x*2,604
-->x=0.1,y=0.2
--> m1=0.1*106+ 0,2*138=38,2
b/
C%Na2CO3= (0.1*106*100)/ (61,8+ 38,2)=10,6%
C%K2CO3=(0.2*138*100)/(61,8+ 38,2)=27,6%
Đúng 0
Bình luận (3)
Có 1 hỗn hợp A gồm CaCO3, Mg CO3, Al2O3 cân nặng 0,602 gam. Hòa tan A vào 50ml dung dịch HCl 0,5M. Để trung hòa lượng axit dư cần 41,4 ml dung dịch NaOH 0,2M. Khí CO2 thoát ra ngoài khi hòa tan A hấp thự vào 93,6 ml dung dịch NaOH có nồng độ % bằng a% ( d1,0039g/ml), sau đó thêm lượng dư dung dịch BaCl2, thấy tạo ra 0,788 gam kết tủa và khi đun sôi lại tạo thêm được 0,134 gam kết tủa nữa. Giả thiết các phản ứng sảy ra hoàn toàn. Hãy cho biết:a. thành phần % các chất trong Ab. Tính a?
Đọc tiếp
Có 1 hỗn hợp A gồm CaCO3, Mg CO3, Al2O3 cân nặng 0,602 gam. Hòa tan A vào 50ml dung dịch HCl 0,5M. Để trung hòa lượng axit dư cần 41,4 ml dung dịch NaOH 0,2M. Khí CO2 thoát ra ngoài khi hòa tan A hấp thự vào 93,6 ml dung dịch NaOH có nồng độ % bằng a% ( d=1,0039g/ml), sau đó thêm lượng dư dung dịch BaCl2, thấy tạo ra 0,788 gam kết tủa và khi đun sôi lại tạo thêm được 0,134 gam kết tủa nữa. Giả thiết các phản ứng sảy ra hoàn toàn. Hãy cho biết:
a. thành phần % các chất trong A
b. Tính a?
Hòa tan 7.6g hỗn hợp nahco3 và na2co3 vào nước thành dung dịch X. Chia X thành 2 phần bằng nhau : - Phần 1 cho tác dụng với 300ml dung dịch hcl 0.3M thu được dung dịch A và khí B. Để trung hòa dung dịch hcl dư trong A cần dùng 10ml dung dịch naoh 3M. Tính khối lượng mỗi muối trong hỗn hợp ban đầu. - Phần 2 cho phản ứng với dung dịch ca(oh)2 dư. Tính khối lượng kết tủa sinh ra
Phần 1:
Đặt `n_{NaHCO_3}=x(mol);n_{Na_2CO_3}=y(mol)`
`->84x+106y={7,6}/2=3,8(1)`
`10ml=0,01l;300ml=0,3l`
`n_{HCl\ bd}=0,3.0,3=0,09(mol)`
`NaHCO_3+HCl->NaCl+CO_2+H_2O`
`Na_2CO_3+2HCl->2NaCl+CO_2+H_2O`
`NaOH+HCl->NaCl+H_2O`
Theo PT: `n_{HCl\ du}=n_{NaOH}=0,01.3=0,03(mol)`
`->n_{HCl\ pu}=x+2y=0,09-0,03=0,06(2)`
`(1)(2)->x=0,02(mol);y=0,02(mol)`
`->` Hỗn hợp ban đầu có \(\begin{cases}m_{NaHCO_3}=0,02.84.2=3,36(g)\\ m_{Na_2CO_3}=7,6-3,36=4,24(g)\end{cases}\)
Phần 2:
`NaHCO_3+Ca(OH)_2->CaCO_3+NaOH+H_2O`
`Na_2CO_3+Ca(OH)_2->CaCO_3+2NaOH`
Theo PT: `n_{CaCO_3}=x+y=0,04(mol)`
`->m_{\downarrow}=m_{CaCO_3}=0,04.100=4(g)`
Đúng 0
Bình luận (0)
dung dịch x chứa hỗn hợp koh và baoh2 để trung hòa 25 ml dung dịch x cần 30 ml dung dịch hcl 1m khi cho 25 ml dung dịch x tác dụng với một lượng dư na2co3 thấy tạo thành 1,97 gam kết tủa tính nồng độ mol của naoh và baoh2 lần trong dung dịch x
hòa tan hoàn toàn 5,12g hỗn hợp X gồm mg và fe trong mg dung dịch hcl 36,5% đến khi phản ứng kết thúc thu được 2,688l H2 dttc và dung dịch Y. để trung hòa hết lượng hcl dư trong Y cần dùng 60ml naoh 1M tính nồng độ % các chất tan trong dung dịch Y.
Đặt \(\left\{{}\begin{matrix}n_{Mg}=n_{MgCl_2}=a\left(mol\right)\\n_{Fe}=n_{FeCl_2}=b\left(mol\right)\end{matrix}\right.\) \(\Rightarrow24a+56b=5,12\) (1)
Ta có: \(n_{H_2}=\dfrac{2,688}{22,4}=0,12\left(mol\right)\)
Bảo toàn electron: \(2a+2b=0,24\) (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}a=n_{MgCl_2}=0,05\left(mol\right)\\b=n_{FeCl_2}=0,07\left(mol\right)\end{matrix}\right.\)
Bảo toàn nguyên tố: \(n_{HCl\left(p/ứ\right)}=2n_{MgCl_2}+2n_{FeCl_2}=0,24\left(mol\right)\)
PTHH: \(NaOH+HCl\rightarrow NaCl+H_2O\)
Theo PTHH: \(n_{HCl\left(dư\right)}=n_{NaOH}=0,06\left(mol\right)\)
\(\Rightarrow\Sigma n_{HCl}=0,3\left(mol\right)\) \(\Rightarrow m_{ddHCl}=\dfrac{0,3\cdot36,5}{36,5\%}=30\left(g\right)\)
Mặt khác: \(m_{H_2}=0,12\cdot2=0,24\left(g\right)\)
\(\Rightarrow m_{dd}=m_{KL}+m_{ddHCl}-m_{H_2}=34,88\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{FeCl_2}=\dfrac{0,07\cdot127}{34,88}\cdot100\%\approx25,49\%\\C\%_{MgCl_2}=\dfrac{0,05\cdot95}{34,88}\cdot100\%\approx13,62\%\\C\%_{HCl\left(dư\right)}=\dfrac{0,04\cdot36,5}{34,88}\cdot100\%\approx4,19\%\end{matrix}\right.\)
Đúng 0
Bình luận (0)
Chia m gam hỗn hợp X gồm Al, Ba thành 2 phần bằng nhau - Phần 1: tác dụng với nước (dư) được 0,04 mol H2. - Phần 2: tác dụng với 50ml dung dịch NaOH 1M (dư) được 0,07 mol H2 và dung dịch Y. Cho V ml dung dịch HCl 1M vào Y được 1,56 gam kết tủa. Giá trị của V lớn nhất để thu được lượng kết tủa trên là A. 20 B. 50 C. 100 D. 130
Đọc tiếp
Chia m gam hỗn hợp X gồm Al, Ba thành 2 phần bằng nhau
- Phần 1: tác dụng với nước (dư) được 0,04 mol H2.
- Phần 2: tác dụng với 50ml dung dịch NaOH 1M (dư) được 0,07 mol H2 và dung dịch Y.
Cho V ml dung dịch HCl 1M vào Y được 1,56 gam kết tủa. Giá trị của V lớn nhất để thu được lượng kết tủa trên là
A. 20
B. 50
C. 100
D. 130
Số mol H2 thu được ở phần 2 lớn hơn phần 1, nên trong phản ứng với H2O của hỗn hợp X thì vẫn còn Al chưa phản ứng
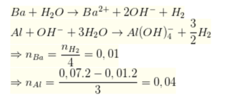
Lượng HCl lớn nhất cần dùng
n H C l = 0 , 03 + 0 , 02 + 4 ( 0 , 04 - 0 , 02 ) = 0 , 13 ⇒ v = 130 m l
Đúng 0
Bình luận (0)
Hòa tan 12,1 g hỗn hợp gồm Fe và Zn trong 500 ml dung dịch HCl 1M được dung dịch A .Để trung hòa hết lượng axit còn dư trong A cần 50ml dung dịch NaOH 2M .Tính thành phần phần trăm theo khối lượng mỗi kim loại
$NaOH + HCl \to NaCl + H_2O$
$n_{HCl\ dư} = n_{NaOH} = 0,05.2 = 0,1(mol)$
Gọi $n_{Fe} = a ; n_{Zn} = b \Rightarrow 56a + 65b = 12,1(1)$
$Fe + 2HCl \to FeCl_2 + H_2$
$Zn + 2HCl \to ZnCl_2 + H_2$
$n_{HCl} = 2a + 2b = 0,5 -0,1 = 0,4(2)$
Từ (1)(2) suy ra a = b = 0,1
$\%m_{Fe} = \dfrac{0,1.56}{12,1}.100\% = 46,28\%$
$\%m_{Zn} = 100\% -46,28\% = 53,72\%$
Đúng 2
Bình luận (0)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(HCl_{dư}+NaOH\rightarrow NaCl+H_2O\)
Gọi x, y lần lượt là số mol Fe, Zn, theo đề ta có:
\(\left\{{}\begin{matrix}56x+65y=12,1\\2x+2y=0,5.1-0,05.2\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\)
=> \(\%m_{Fe}=\dfrac{0,1.56}{12,1}=46,28\%\)
=> \(\%m_{Zn}=100-46,28=53,72\%\)
Đúng 3
Bình luận (0)
Dung dịch X chứa axit HCl a mol/l và HNO3 b mol/lít. Để trung hòa 20ml dung dịch X cần dùng 300ml dung dịch NaOH 0,1M. Mặt khác, lấy 20ml dung dịch X cho tác dụng với dung dịch AgNO3 dư thấy tạo thành 2,87 gam kết tủa. Giá trị của a và b lần lượt là: A. 1,0 và 0,5 B. 0,5 và 1,7 C. 1,0 và 1,5 D. 2,0 và 1,0
Đọc tiếp
Dung dịch X chứa axit HCl a mol/l và HNO3 b mol/lít. Để trung hòa 20ml dung dịch X cần dùng 300ml dung dịch NaOH 0,1M. Mặt khác, lấy 20ml dung dịch X cho tác dụng với dung dịch AgNO3 dư thấy tạo thành 2,87 gam kết tủa. Giá trị của a và b lần lượt là:
A. 1,0 và 0,5
B. 0,5 và 1,7
C. 1,0 và 1,5
D. 2,0 và 1,0
Đáp án A
nOH-= nH+ nên 0,02.a+ 0,02.b = 0,3.0,1
nCl-= nAgCl = 0,02 mol = 0,02a suy ra a = 1M suy ra b = 0,5
Đúng 0
Bình luận (0)






















