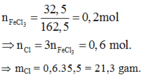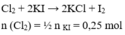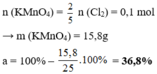Bao nhiêu gam Cu tác dụng vừa đủ với clo tạo ra 27 gam CuCl2?

Những câu hỏi liên quan
bao nhiu gam cu tác dụng vừa đủ vs kl clo tạo ta 27 gam CuCl2
Xem chi tiết
\(Cu + Cl_2 \xrightarrow{t^o} CuCl_2\\ n_{Cu} = n_{CuCl_2}= \dfrac{27}{135} = 0,2(mol)\\ \Rightarrow m_{Cu} = 0,2.64 = 12,8(gam)\)
Đúng 2
Bình luận (0)
Bao nhiêu gam clo tác dụng vừa đủ kim loại nhôm tạo ra 26,7 gam AlCl3?
A. 21,3 gam
B. 12,3 gam
C. 13,2 gam
D. 23,1 gam
Bao nhiêu gam clo tác dụng vừa đủ kim loại sắt tạo ra 32,5 gam FeCl3?
A. 21,3 gam
B. 14,2 gam.
C. 13,2 gam.
D. 23,1 gam.
Bao nhiêu gam clo tác dụng vừa đủ kim loại nhôm tạo ra 26,7 gam AlCl3 ?
đáp án a bạn nhé
vì nhôm pư với clo thep pthh:
2Al+3Cl2\(\rightarrow\)2AlCl3(1)
theo pthh(1) và đề bài ta có:nAlCl3=26,7:133,5=0,2(mol)
nCl2 =0,2:2\(\times\)3=0,3(mol)
mCl2=71\(\times\)0,3=21,3(g)
vậ số gam clo cần dùng là 21,3(g)
Đúng 0
Bình luận (0)
Khối lượng khí clo tác dụng vừa đủ với kim loại nhôm tạo ra 26,7 gam AlCl3 là:
A. 12,3 gam.
B. 13,2 gam.
C. 21,3 gam
D. 23,1 gam.
Đáp án C
nAlCl3 = 26,7: 133,5 = 0,2 mol
Bảo toàn nguyên tố Cl: 2nCl2 = 3nAlCl3
=> nCl2 = 1,5nAlCl3 = 1,5.0,2 = 0,3 mol
Đúng 0
Bình luận (0)
Bao nhiu gam clo tác dụng vừa đủ vs kl Al tạo ta 26,7 gam AlCl3
Xem chi tiết
vì nhôm pư với clo thep pthh:
2Al+3Cl22AlCl3(1)
theo pthh(1) và đề bài ta có:nAlCl3=26,7:133,5=0,2(mol)
nCl2 =0,2:23=0,3(mol)
mCl2=710,3=21,3(g)
vậy số gam clo cần dùng là 21,3(g)
Đúng 2
Bình luận (0)
PT: \(2Al+3Cl_2\underrightarrow{t^o}2AlCl_3\)
Ta có: \(n_{AlCl_3}=\dfrac{26,7}{133,5}=0,2\left(mol\right)\)
Theo PT: \(n_{Cl_2}=\dfrac{3}{2}n_{AlCl_3}=0,3\left(mol\right)\)
\(\Rightarrow m_{Cl_2}=0,3.71=21,3\left(g\right)\)
Bạn tham khảo nhé!
Đúng 3
Bình luận (0)
\(2Al + 3Cl_2 \xrightarrow{t^o} 2AlCl_3\\ n_{Cl_2} = \dfrac{3}{2}n_{AlCl_3} = \dfrac{3}{2}.\dfrac{26,7}{133,5} = 0,3(mol)\\ \Rightarrow m_{Cl_2} = 0,3.71 = 21,3(gam)\)
Đúng 3
Bình luận (0)
Cho 25 gam K M n O 4 (có a% tạp chất) tác dụng với dung dịch HCl dư thu được khí clo. Để khí clo sinh ra phản ứng vừa đủ với dung dịch chứa 83 gam KI tạo I 2 , giá trị của a là
A. 20
B. 59,25
C. 36,8
D. 26
Cần bao nhiêu gam KMnO4 và bao nhiêu ml dung dịch HCl 1M để điều chế đủ khí Clo tác dụng với Fe tạo nên 16,25 gam FeCl3 ?
Xem chi tiết
\(n_{FeCl_3}=\dfrac{16.25}{162.5}=0.1\left(mol\right)\)
\(Fe+\dfrac{3}{2}Cl_2\underrightarrow{t^0}FeCl_3\)
\(......0.15......0.1\)
\(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
\(0.06...............0.48........................................0.15\)
\(m_{KMnO_4}=0.06\cdot158=9.48\left(g\right)\)
\(V_{dd_{HCl}}=\dfrac{0.48}{1}=0.48\left(l\right)=480\left(ml\right)\)
Đúng 3
Bình luận (2)
\(2Fe+ 3Cl_2 \xrightarrow{t^o} 2FeCl_3\\ n_{Cl_2} = \dfrac{3}{2}n_{FeCl_3} = \dfrac{3}{2}.\dfrac{16,25}{162,5} = 0,15(mol)\\ 2KMnO_4 + 16HCl \to 2KCl + 2MnCl_2 + 5Cl_2 + 8H_2O\\ n_{KMnO_4} = \dfrac{2}{5}n_{Cl_2} = 0,06(mol)\\ \Rightarrow m_{KMnO_4} = 0,06.158 = 9,48(gam)\\ n_{HCl} = \dfrac{16}{4}n_{Cl_2} = 0,48(mol)\\ \Rightarrow V_{dd\ HCl} = \dfrac{0,48}{1} = 0,48(lít) = 480(ml)\)
Đúng 1
Bình luận (0)