Hòa tan hoàn toàn 10,2g hỗn hợp gồm 2 kim loại A và B có hóa trị lần lượt là II và III cần dùng vừa đủ 500 ml HCl, sau phản ứng thu được 45,7g muối HCl và V lít H2. Tìm V và CM của dung dịch HCl

Những câu hỏi liên quan
Để hòa tan hoàn toàn 1,65g hỗn hợp kim loại gồm một kim loại vừa hóa trị II, III và một kim loại hóa trị III cần 200ml dung dịch HCl 0,6Ma) Cô cạn dung dịch sau phản ứng thu được bao nhiêu (g) muối khan?b) Tính thể tích khí H2 ở ĐKTCc) Nếu biết kim loại hóa trị III là Al và có số mol gấp 2 lần số mol kim loại mang 2 hóa trị. Xác định tên kim loại đó.Mình đang cần gấp !!!
Đọc tiếp
Để hòa tan hoàn toàn 1,65g hỗn hợp kim loại gồm một kim loại vừa hóa trị II, III và một kim loại hóa trị III cần 200ml dung dịch HCl 0,6M
a) Cô cạn dung dịch sau phản ứng thu được bao nhiêu (g) muối khan?
b) Tính thể tích khí H2 ở ĐKTC
c) Nếu biết kim loại hóa trị III là Al và có số mol gấp 2 lần số mol kim loại mang 2 hóa trị. Xác định tên kim loại đó.
Mình đang cần gấp !!!
Hòa tan hoàn toàn 9,2g hỗn hợp gồm một kim loại có hoá trị II và một kim loại có hoá trị III vào dung dịch HCl 2M thu được 5,6 lít H2 ở đktc.
a) Nếu cô cạn dd sau phản ứng sẽ thu được bao nhiêu gam hh muối?
b) Tính thể tích dd HCl 2M đã dùng?
Em cần bài gắp, mong mọi người giải hộ!
a)
$R + 2HCl \to RCl_2 + H_2$
$2B + 6HCl \to 2BCl_3 + 3H_2$
$n_{H_2} = \dfrac{5,6}{22,4} = 0,25(mol)$
$n_{HCl} = 2n_{H_2} = 0,5(mol)$
Bảo toàn khối lượng : $m_{muối} = m_{kl} + m_{HCl} - m_{H_2}$
$= 9,2 + 0,5.36,5 - 0,25.2 = 26,95(gam)$
b) $V_{dd\ HCl} = \dfrac{0,5}{2} = 0,25(lít)$
Đúng 2
Bình luận (0)
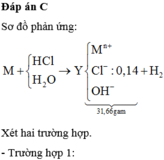
Hòa tan hoàn toàn a gam kim loại M (có hóa trị không đồi) vào 140 ml dung dịch HCl 1M, thu được dung dịch Y và V lít H2 (đktc). Cô cạn Y, thu được 31,66 gam hỗn hợp chất rắn khan. Mặt khác, Y phản ứng vừa đủ với dung dịch chứa 0,17 mol H2SO4 (loãng). Giá trị của V là A. 4,480. B. 5,376. C. 3,808. D. 3,360.
Đọc tiếp
Hòa tan hoàn toàn a gam kim loại M (có hóa trị không đồi) vào 140 ml dung dịch HCl 1M, thu được dung dịch Y và V lít H2 (đktc). Cô cạn Y, thu được 31,66 gam hỗn hợp chất rắn khan. Mặt khác, Y phản ứng vừa đủ với dung dịch chứa 0,17 mol H2SO4 (loãng). Giá trị của V là
A. 4,480.
B. 5,376.
C. 3,808.
D. 3,360.
Hoà tan hoàn toàn 4g hỗn hợp gồm 1 kim loại hoá trị II và một kim loại hoá trị III cần dùng hết 170 ml HCl 2M.
a) Cô cạn dung dịch thu được bao nhiêu gam muối?
b) Vính V H2 thoá ra ở dktc
c) Nếu biết kim loại hoá trị III là Al và số mol bằng 5 lần số mol kim loại hoá trị II thì kim loại hoá trị II là kim loại nào?
a) Gọi kim loại hóa trị II là A, kim loại hóa trị III là B
\(n_{HCl}=0,17.2=0,34\left(mol\right)\)
PTHH: A + 2HCl --> ACl2 + H2
2B + 6HCl --> 2BCl3 + 3H2
=> \(n_{H_2}=\dfrac{1}{2}n_{HCl}=0,17\left(mol\right)\)
Theo ĐLBTKL: mkim loại + mHCl = mmuối + mH2
=> mmuối = 4 + 0,34.36,5 - 0,17.2 = 16,07 (g)
b) \(V_{H_2}=0,17.22,4=3,808\left(l\right)\)
c) Có: \(\left\{{}\begin{matrix}n_A=a\left(mol\right)\\n_{Al}=5a\left(mol\right)\end{matrix}\right.\)
=> a.MA + 135a = 4 (1)
PTHH: A + 2HCl --> ACl2 + H2
a-------------------->a
2Al + 6HCl --> 2AlCl3 + 3H2
5a------------------------>7,5a
=> a + 7,5a = 0,17
=> a = 0,02 (mol) (2)
(1)(2) => MA = 65 (g/mol)
=> A là Zn
Đúng 4
Bình luận (0)
\(n_{HCl}=0,17.2=0,34\left(mol\right)\\ \rightarrow m_{HCl}=0,34.36,5=12,41\left(g\right)\)
Gọi kim loại hoá trị II là A, kim loại hoá trị III là B
PTHH:
A + 2HCl ---> ACl2 + H2
2B + 6HCl ---> 2BCl3 + 3H2
Theo pthh: \(n_{H_2}=\dfrac{1}{2}n_{HCl}=\dfrac{1}{2}.0,34=0,17\left(mol\right)\)
\(\rightarrow\left\{{}\begin{matrix}m_{H_2}=0,17.2=0,34\left(g\right)\\V_{H_2}=0,17.22,4=3,808\left(l\right)\end{matrix}\right.\)
Theo ĐLBTKL:
\(m_{kl}+m_{HCl}=m_{muối}+m_{H_2}\)
=> mmuối = 4 + 12,41 - 0,34 = 16,07 (g)
Gọi \(n_B=a\left(mol\right)\)
\(\rightarrow n_{Al}=5a\left(mol\right)\)
Theo pthh: \(n_{HCl}=2n_B+3n_{Al}=2a+13.5b=17a=0,34\left(mol\right)\)
\(\rightarrow a=0,02\left(mol\right)\\ \rightarrow m_{Al}=5.0,02.27=2,7\left(g\right)\\ \rightarrow m_B=4-2,7=1,3\left(g\right)\\ \rightarrow M_B=\dfrac{1,3}{0,02}=65\left(\dfrac{g}{mol}\right)\)
=> B là Zn
Đúng 3
Bình luận (0)
Hòa tan hoàn toàn 4gam hỗn hợp gồm 1 kim loại hóa trị II vào 1 kim loại hóa trị III. Cần dùng hết 170ml dung dịch HCl 2M.
a) Tính thể tích H2 sinh ra ở đktc.
b) Cô cạn dung dịch thu được bao nhiêu gam muối khan.
c) Nếu biết kim loại hóa trị III là Al và số mol = 5 lần số mol kim loại hóa trị II thì kim loại hóa trị II là nguyên tố nào?
PTHH: \(2R+6HCl\rightarrow2RCl_3+3H_2\uparrow\) (1)
\(X+2HCl\rightarrow XCl_2+H_2\uparrow\) (2)
a) Ta có: \(n_{HCl}=0,17\cdot2=0,34\left(mol\right)\)
Theo các PTHH: \(n_{HCl}:n_{H_2}=2:1\) \(\Rightarrow n_{H_2}=0,17\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,17\cdot22,4=3,808\left(l\right)\)
b) Ta có: \(\left\{{}\begin{matrix}m_{HCl}=0,34\cdot36,5=12,41\left(g\right)\\m_{H_2}=0,17\cdot2=0,34\left(g\right)\end{matrix}\right.\)
Bảo toàn khối lượng: \(m_{muối}=m_{KL}+m_{HCl}-m_{H_2}=16,07\left(g\right)\)
c) Đặt \(n_{Al}=5a\left(mol\right)\) \(\Rightarrow n_X=a\left(mol\right)\)
Theo các PTHH: \(\left\{{}\begin{matrix}n_{HCl\left(1\right)}=15a\left(mol\right)\\n_{HCl\left(2\right)}=2a\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow15a+2a=0,34\left(mol\right)=\Sigma n_{HCl}\) \(\Rightarrow a=n_X=0,02\left(mol\right)\)
Mặt khác: \(m_X=m_{KL}-m_{Al}=4-0,02\cdot5\cdot27=1,3\left(g\right)\)
\(\Rightarrow M_X=\dfrac{1,3}{0,02}=65\left(đvC\right)\)
\(\Rightarrow\) Nguyên tố Zn (Kẽm)
Đúng 2
Bình luận (0)
a, nHCl=0,17.2=0,34 mol
Ta có tỉ lệ HCl/H2=1/2 (vì HCl có 1 hiđro và H2 có 2 hiđro)
=> H2=0,34.1/2=0,17 mol
Nên VH2=0,17.22,4=3,808 l
b, ta có mmuoi khan=mhon hop+mCl (nCl=nHCl)
=> mmuoi khan=4+0,34.35,5=16,07 g
c, Gọi nA là a mol => nAl= 5a mol
PTPƯ: 2Al + 6HCl ---> 2AlCl3 + 3H2
5a mol Al ---> 15a mol HCl
AII + 2HCl ---> ACl2 + H2
a mol A ---> 2a mol HCl
Ta có: 15a+2a=0,34 => 17a=0,34 => a=0,02 mol
Ta có: 27.5.0,02+MA.0,02=4
=> 2,7+MA.0,02=4 => MA.0,02=1,3 => MA=65 (là nguyên tố kẽm hay Zn)
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 11,4 gam hỗn hợp gồm Fe và Fe3O4, cần vừa đủ V lít dung dịch HCl 1,25 M. Sau phản ứng thu được 2,24 lít khí H2 (đktc). Tính giá trị của V?
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ Fe+2HCl\rightarrow FeCl_2+H_2\\ n_{Fe}=n_{H_2}=0,1\left(mol\right)\\ m_{Fe_3O_4}=11,4-0,1.56=5,8\left(g\right)\\ n_{Fe_3O_4}=\dfrac{5,8}{232}=0,025\left(mol\right)\\ Fe_3O_4+8HCl\rightarrow2FeCl_3+FeCl_2+4H_2O\\ n_{HCl\left(tổng\right)}=2.n_{Fe}+8.n_{Fe_3O_4}=2.0,1+8.0,025=0,4\left(mol\right)\\ V_{ddHCl}=\dfrac{0,4}{1,25}=0,32\left(l\right)\)
Đúng 2
Bình luận (1)
hòa tan hoàn toàn 19,2g hh gồm Al,Mg,Fe cần vừa đủ V ml dung dịch hỗn hợp X chứa HCL 1M và h2SO4 2M, sau khi phản ứng xong thu đc 11.2l H2 và a(g) hh muối. Giá trị của a là ??
số mol H+ trong axit :nH+=nHCl+2nH2SO4+=V+4V=5V
số mol H+=2nh22.0,5=5V suy ra V=0,2mHCl=0,2.36,5mH2SO4=2.0,2.98ap dung dinh luat bao toan khoi luong tim ra muoi
Đúng 0
Bình luận (0)
vi khi cho hh kim loai vao can vua du V(lit) HCl va H2SO4 nên số mol nH2=nH+(trong HCl)+nH+(trong H2SO4) tim duoc V
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Hoà tan hoàn toàn 5,5 gam hỗn hợp X gồm 2 kim loại Al và Fe cần vừa đủ V lít dung dịch HCl 1M, sau phản ứng thu được 4,48 lít khí H2 ( ở đktc) và dung dịch Y, cô cnaj Y thu được m gam muối khan.a) TÍnh % theo khối lượn các kim loại có trong Xb) Tính các giá trị V và mc) Lấy 1/5 dung dịch Y cho tác dụng với lượng AgNO3 dư thu được bao nhiêu gam chất kết tủa? Biết cá phản ứng đều xảy ra hoàn toàn
Đọc tiếp
Hoà tan hoàn toàn 5,5 gam hỗn hợp X gồm 2 kim loại Al và Fe cần vừa đủ V lít dung dịch HCl 1M, sau phản ứng thu được 4,48 lít khí H2 ( ở đktc) và dung dịch Y, cô cnaj Y thu được m gam muối khan.
a) TÍnh % theo khối lượn các kim loại có trong X
b) Tính các giá trị V và m
c) Lấy 1/5 dung dịch Y cho tác dụng với lượng AgNO3 dư thu được bao nhiêu gam chất kết tủa? Biết cá phản ứng đều xảy ra hoàn toàn
Hòa tan 9,1 gam hỗn hợp X gồm hai kim loại Al và Cu vài 300 ml dung dịch HCl 1M vừa đủ đến khi phản ứng xảy ra hoàn toàn thu được V lít khí H2 do ở đktc. a. Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu b. Tính V
\(n_{HCl}=0,3.1=0,3mol\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,1 0,3 0,15 ( mol )
\(m_{Al}=0,1.27=2,7g\)
\(\Rightarrow m_{Al}=9,1.2,7=6,4g\)
\(V_{H_2}=0,15.22,4=3,36l\)
Đúng 3
Bình luận (2)
nHCl = 0,3 . 1 = 0,3 (mol)
PTHH: 2Al + 6HCl -> 2AlCl3 + 3H2
Mol: 0,1 <--- 0,3 ---> 0,1 ---> 0,15
mAl = 0,1 . 27 = 2,7 (g(
mCu = 9,1 - 2,7 = 6,4 (g)
VH2 = 0,15 . 22,4 = 3,36 (l)
Đúng 2
Bình luận (1)