Cho 46g Na t/d với o2.Sau phản ứng thu được oxit kim loại. Sau đó cho oxit kim loại đó vào 400ml nước dư. Thu được dung dịch A.(DH2O=1g/ml)
=a Tính C% dung dịch A
b Tính CM dung dịch A
Cho 46g Na t/d với o2.Sau phản ứng thu được oxit kim loại. Sau đó cho oxit kim loại đó vào 400ml nước dư. Thu được dung dịch A.
a Tính C% dung dịch A
b Tính CM dung dịch A
nNa=46/23=2 mol
2Na +1/2 O2 =>Na2O
2 mol =>0,5 mol=>1 mol
Na2O + H2O =>2NaOH
1 mol =>2 mol
mdd A=mNa2O+mH2O=1.62+400=462g
nNaOH=2 mol
=>mNaOH=2.40=80g
=>C% dd NaOH=80/462.100%=17,32%
CM dd NaOH=CM dd A=2/0,4=5M
Cho 20,2 gam hỗn hợp gồm Al và một oxit của kim loại kiềm vào nước dư, sau đó thấy khối lượng dung dịch tăng so với trước 14,2 gam. Cho 650 ml dung dịch HCl 1M vào dung dịch sau phản ứng thu được 3,9 gam kết tủa. Công thức của oxit kim loại kiềm là
A. K2O
B. Na2O
C. Li2O
D. Rb2O
Cho 20,2g hỗn hợp gồm Al và một oxit của kim loại kiềm vào nước dư, sau đó thấy khối lượng dung dịch tăng so với trước 14,2g. Cho 650ml dung dịch HCl 1M vào dung dịch sau phản ứng thu được 3,9g kết tủa . Công thức của oxit kim loại kiềm là :
A. K2O
B. Na2O
C. Li2O
D. Rb2O
Đáp án : A
Gọi CT oxit là : R2O
Giả sử có x mol Al và y mol R2O
, nHCl = 0,65 mol ; nAl(OH)3 = 0,05mol
Nếu Al dư => Trong dung dịch chỉ có 2y mol RAlO2
Do nHCl > nAl(OH)3 => kết tủa tan 1 phần
=> nH+= 4nAlO2 – 3nAl(OH)3 => nAlO2 = 2y = 0,2 => y = 0,1 mol
=> nH2 = 0,3 mol và nAl pứ = 0,2 mol
=> mtăng = mR2O + mAl pứ - mH2
=> mR2O = 9,4g và nR2O = 0,1 mol
=> M oxit = 94 => R = 39 (Kali)
TH : Al hết sẽ không thỏa mãn
Cho 6,2 gam oxit của kim loại hóa trị I tác dụng với nước dư thu được dung dịch A có tính kiềm. Chia A thành 2 phần bằng nhau:
Phần 1 tác dụng với 95ml dung dịch HCl 1M thấy dung dịch sau phản ứng làm xanh quỳ tím.
Phần 2 tác dụng với 55ml dung dịch HCl 2M thấy dung dịch sau phản ứng làm đỏ quỳ tím.
Công thức oxit kim loại đã dùng là:
A.Li2O.
B. Na2O.
C.K2O.
D.Rb2O.
Gọi n M 2 O = a thì nMOH = 2a, mỗi phần có nMOH = a
Khi nHCl = 0,095 thì dung dịch sau phản ứng làm quỳ tím hóa xanh nên MOH dư => a > 0,095
Khi nHCl = 0,11 thì dung dịch sau phản ứng làm quỳ tím hóa đỏ nên HCl dư => a < 0,11
Có 0,095 < a < 0,11
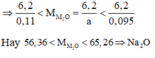
Đáp án B
A là dung dịch AgNO3 nồng độ a M . cho 13.8 g hỗn hợp sắt và đồng vào 750 ml dung dịch A , sau phản ứng kết thúc thu được dung dịch B và 37.2 g chất rắn E . Cho NaOH dư vào dung dịch B thu được kết tủa . Lấy kết tủa nung đến trong không khí đến khối lượng không đổi thu được 12g hỗn hợp 2 oxit của 2 kim loại .
a) Tính % theo khối lượng mỗi kim loạib) Tính a=?Oxit hóa hoàn toàn 6,5475 gam kim loại T bằng Cl2. Sản phẩm sau phản ứng đem hòa tan vào nước thu được dung dịch X. Cho từ từ dung dịch NaOH vào dung dịch X thấy có kết tủa tạo ra, sau đó kết tủa tan vừa hết thì ngừng, thấy đã dùng hết 970 ml dung dịch NaOH 1M. Xác định kim loại T
A. Al
B. Cr
C. Zn
D. Be
Cho các phát biểu sau:
(a) Điện phân NaCl nóng chảy, ở anot xảy ra sự khử anion clorua.
(b) Các oxit của kim loại kiềm thổ đều phản ứng với CO tạo thành kim loại.
(c) Cho mẩu kim loại Na vào dung dịch AlCl3, thu được kết tủa Al.
(d) Cho kim loại Mg vào dung dịch FeCl3 dư, không thu được Fe.
(e) Hỗn hợp Al và BaO (tỉ lệ mol tương ứng là 1 : 1) tan hoàn toàn trong nước dư.
Số phát biểu đúng là
A. 4.
B. 1.
C.2.
D.3.
Cho 11,2g canxi oxit vào 1 lít H2O (D=1g/ml)
a) Tính C%,CM của dung dịch thu được
b) Người ta dùng HCl 14,6% (D=1,2g/ml) để trung hòa dung dịch trên. Tính V dung dịch axit cần dùng
c) Tính CM,C% của dung dịch thu được sau phản ứng
nCaO=0,4 mol
mH2O=1g=>nH2O=1/18mol
PTHH: CaO+H2O=> Ca(OH)2
0,4:1/18 => nCaO dư theo nH2O
Cm=1/18:1=1/18M
Cho X là hỗn hợp của 3 chất gồm kim loại M, oxit và muối sunfat của kim loại M. Biết M có hóa trị II không đổi trong các hợp chất. Chia 29,6 gam X thành hai phần bằng nhau:
– Phần 1: đem hòa tan tỏng dung dịch H2SO4loãng dư thu được dung dịch A, khí B. Lượng khí B này vừa đủ để khử hết 16 gam CuO. Sau đó cho dung dịch A tác dụng với dung dịch KOH dư, đến khi kết thúc phản ứng thu được kết tủa C. Nung C đến khối lượng không đổi thì thu được 14 gam chất rắn.
– Phần 2: cho tác dụng với 200 ml dung dịch CuSO4 1,5M. Sau khi kết thúc phản ứng tách bỏ chất rắn, cô cạn phần dung dịch thì thu được 46 gam muối khan.
a) Viết phương trình phản ứng xảy ra và xác định kim loại M.
b) Tính phần trăm khối lượng các chất trong X.

Bảo toàn nguyên tố M: nMSO4 = 0,25mol
Bảo toàn nguyên tố Cu: nCuSO4 dư = 0,1 mol
=> M = 24 (Mg)
b.
