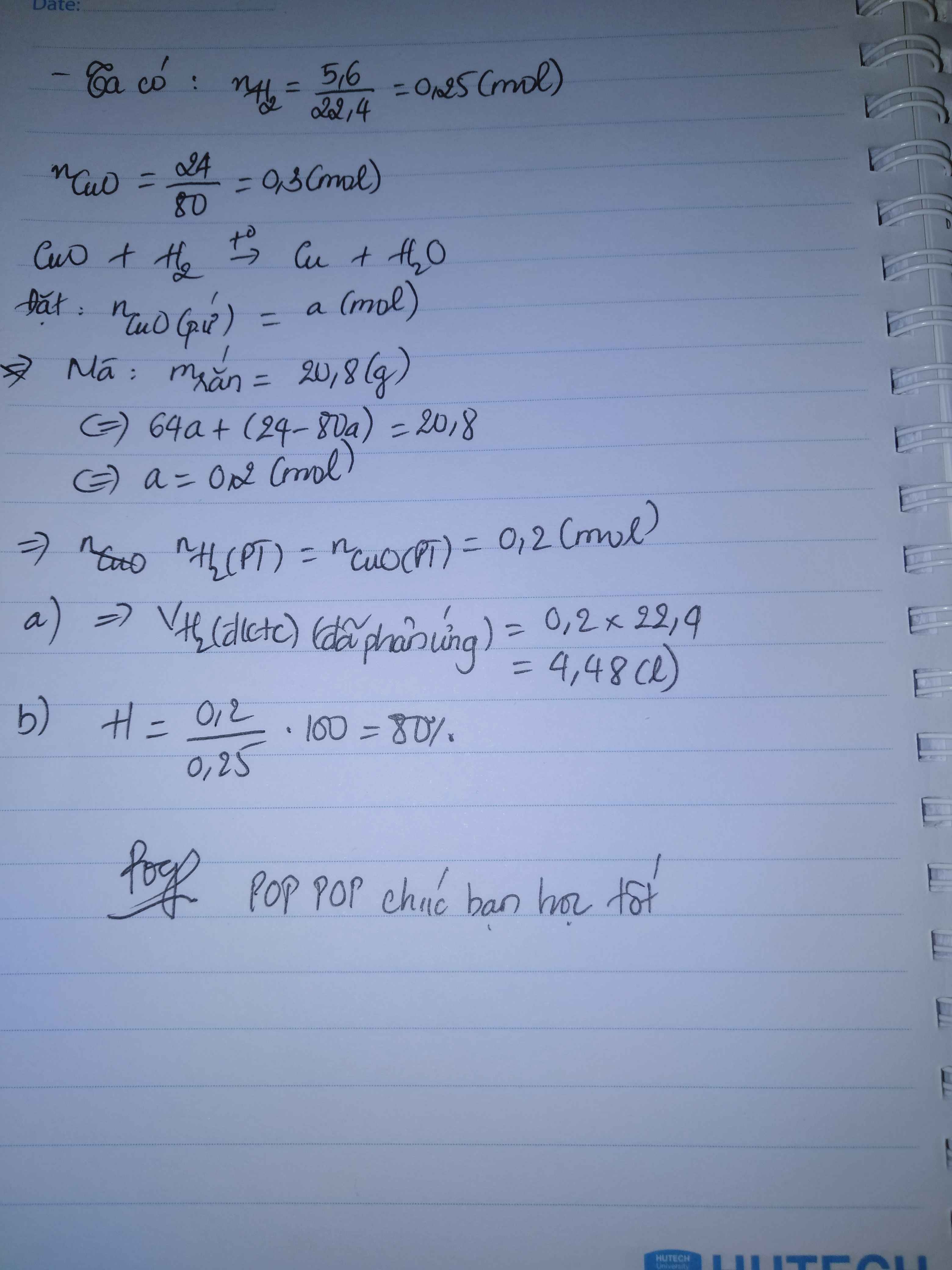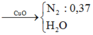Dẫn hỗn hợp khí CO và H2 qua 10 gam bột CuO ở nhiệt độ cao, sau một thời gian thấy còn lại 8,4 gam chất rắn. Hiệu suất chuyển hóa CuO thành Cu bằng

Những câu hỏi liên quan
Câu 1: Cho luồng khí H2 đi qua ống thủy tinh chứa 20 gam bột CuO ở nhiệt độ cao. Sau phản ứng thu được 16,8 gam chất rắn. Hiệu suất của phản ứng là
Biết phương trình hóa học của phản ứng như sau:
CuO + H2 Cu + H2O
Câu 1: Cho luồng khí H2 đi qua ống thủy tinh chứa 20 gam bột CuO ở nhiệt độ cao. Sau phản ứng thu được 16,8 gam chất rắn. Hiệu suất của phản ứng là
Biết phương trình hóa học của phản ứng như sau:
CuO + H2 Cu + H2O
Gọi số mol CuO pư là a (mol)
\(n_{CuO\left(bđ\right)}=\dfrac{20}{80}=0,25\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
a-------------->a
Rắn sau pư gồm \(\left\{{}\begin{matrix}CuO:0,25-a\left(mol\right)\\Cu:a\left(mol\right)\end{matrix}\right.\)
=> 80(0,25-a) + 64a = 16,8
=> a = 0,2 (mol)
=> \(H\%=\dfrac{0,2}{0,25}.100\%=80\%\)
Đúng 3
Bình luận (0)
Dẫn 5,6 lít H2 (đktc) qua ống sứ đựng 24 gam bột CuO ở nhiệt độ cao, sau một thời gian thu được 20,8 gam chất rắn.
a/ Tính thể tích H2 (đkc) đã phản ứng.
b/ Tính hiệu suất phản ứng.
a)
\(n_{CuO}=\dfrac{24}{80}=0,3\left(mol\right)\)
\(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
Xét tỉ lệ \(\dfrac{0,3}{1}>\dfrac{0,25}{1}\)=> Hiệu suất tính theo H2
Gọi số mol CuO phản ứng là a
=> nCu = a (mol)
Có: (0,3-a).80 + 64a = 20,8
=> a = 0,2 (mol)
\(n_{H_2}=n_{CuO}=0,2\left(mol\right)\)
=> \(V_{H_2}=0,2.22,4=4,48\left(l\right)\)
b) \(H\%=\dfrac{0,2}{0,25}.100\%=80\%\)
Đúng 4
Bình luận (0)
Số mol CuO bài ra là:
\(n_{CuObr}=\dfrac{24}{80}=0,3\left(mol\right)\)
Số mol hidro bài ra là:
\(n_{H_2br}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH
\(CuO+H_2\rightarrow Cu+H_2O\)
\(\dfrac{n_{CuObr}}{n_{CuOpt}}>\dfrac{n_{H_2br}}{n_{H_2pt}}\)
=> CuO dư sau phản ứng, bài toán tính theo hidro
Vậy thể tích hidro đã p/ứ là 5,6(lít)
b, Theo pt: \(n_{H_2}=n_{Cu}=0,25\left(mol\right)\)
Khối lượng Cu sản phẩm là:
\(m_{Cu}=0,25.64=16\left(g\right)\)
Hiệu suất của phản ứng là:
\(H=\dfrac{m_{Cu}}{m_{chat.ran}}.100\%=\dfrac{16}{20,8}.100\%\approx76,92\%\)
Đúng 0
Bình luận (0)
Câu 1: Cho luồng khí H2 đi qua ống thủy tinh chứa 20 gam bột CuO ở nhiệt độ cao. Sau phản ứng thu được 16,8 gam chất rắn. Hiệu suất của phản ứng làBiết phương trình hóa học của phản ứng như sau:CuO + H2 Cu + H2OCâu 2: Trộn 10,8 g bột nhôm với bột lưu huỳnh dư. Cho hỗn hợp vào ống nghiệm và đun nóng để phản ứng xảy ra thu được 25,5 g Al2S3. Tính hiệu suất phản ứng ?Câu 3: Một cơ sở sản xuất vôi tiến hành nung 4 tấn đá vôi (CaCO3) thì thu được 1,68 tấn vôi sống(CaO) và một lượng khí CO2. Tính hi...
Đọc tiếp
Câu 1: Cho luồng khí H2 đi qua ống thủy tinh chứa 20 gam bột CuO ở nhiệt độ cao. Sau phản ứng thu được 16,8 gam chất rắn. Hiệu suất của phản ứng là
Biết phương trình hóa học của phản ứng như sau:
CuO + H2 Cu + H2O
Câu 2: Trộn 10,8 g bột nhôm với bột lưu huỳnh dư. Cho hỗn hợp vào ống nghiệm và đun nóng để phản ứng xảy ra thu được 25,5 g Al2S3. Tính hiệu suất phản ứng ?
Câu 3: Một cơ sở sản xuất vôi tiến hành nung 4 tấn đá vôi (CaCO3) thì thu được 1,68 tấn vôi sống(CaO) và một lượng khí CO2. Tính hiệu suất của quá trình nung vôi.
Khử m gam hỗn hợp X gồm CuO, Fe2O3, FeO, Fe3O4 bằng khí CO ở nhiệt độ cao. Sau một thời gian người ta thu được 40 gam chất rắn Y và hỗn hợp khí Z. Dẫn Z vào dung dịch nước vôi trong dư thu được 40 gam kết tủa. Tính giá trị của m
PTHH: \(CuO+CO\xrightarrow[]{t^o}Cu+CO_2\)
\(Fe_2O_3+3CO\xrightarrow[]{t^o}2Fe+3CO_2\)
\(FeO+CO\xrightarrow[]{t^o}Fe+CO_2\)
\(Fe_3O_4+4CO\xrightarrow[]{t^o}3Fe+4CO_2\)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3\downarrow+H_2O\)
Theo các PTHH: \(n_{CaCO_3}=\dfrac{40}{100}=0,4\left(mol\right)=n_{CO_2}=n_{CO}\) \(\Rightarrow\left\{{}\begin{matrix}m_{CO}=0,4\cdot28=11,2\left(g\right)\\m_{CO_2}=0,4\cdot44=17,6\left(g\right)\end{matrix}\right.\)
Bảo toàn khối lượng: \(m_{Oxit}+m_{CO}=m_{KL}+m_{CO_2}\)
\(\Rightarrow m_{Oxit}=m_{KL}+m_{CO_2}-m_{CO}=40+17,6-11,2=46,4\left(g\right)\)
Đúng 2
Bình luận (0)
Nếu bạn không muốn viết nhiều phương trình thì bạn có thể dùng bảo toàn nguyên tố (Nếu đã được học)
Đúng 0
Bình luận (0)
Cho luồng khí H2 dư đi qua ống thủy tinh chứa 20 gam bột CuO ở nhiệt độ cao theo phương trình phản ứng như sau: CuO + H2 Cu + H2O. Sau phản ứng thu được 12 gam chất rắn. Hiệu suất của phản ứng là:A. 75%.B. 85%.C. 90%.D. 95%.Mọi người giúp mình với!
Đọc tiếp
Cho luồng khí H2 dư đi qua ống thủy tinh chứa 20 gam bột CuO ở nhiệt độ cao theo phương trình phản ứng như sau: CuO + H2 Cu + H2O. Sau phản ứng thu được 12 gam chất rắn. Hiệu suất của phản ứng là:
A. 75%.
B. 85%.
C. 90%.
D. 95%.
Mọi người giúp mình với!![]()
Ta có: \(n_{CuO}=\dfrac{20}{80}=0,25\left(mol\right)\)
Gọi: nCuO (pư) = x (mol) ⇒ nCuO (dư) = 0,25 - x (mol)
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Theo PT: \(n_{Cu}=n_{CuO\left(pư\right)}=x\left(mol\right)\)
Chất rắn gồm: Cu và CuO dư.
⇒ 64x + 80.(0,25 - x) = 12 ⇒ x = 0,5 > nCuO ban đầu
→ vô lý
Bạn xem lại đề nhé.
Đúng 1
Bình luận (2)
\(n_{CuO}=\dfrac{20}{80}=0,25mol\\ CuO+H_2\xrightarrow[]{t^0}Cu+H_2O\\ n_{Cu\left(LT\right)}=n_{CuO}=0,25mol\\ m_{Cu\left(LT\right)}=0,25.64=16g\\ H=\dfrac{12}{16}\cdot100\%=70\%\\ \Rightarrow A\)
Đúng 0
Bình luận (2)
Khử hoàn toàn 28 gam hỗn hợp gồm CuO và một oxit của sắt bằng khí H2 dư ở nhiệt độ cao. Sau phản ứng thu được hỗn hợp chất rắn, cho hỗn hợp rắn này tác dụng hoàn toàn với axit H2SO4 loãng thấy thoát ra 3,36 lít khí (ở đktc) và 12,8 gam chất rắn.
a. Tìm công thức oxit của sắt
b. Tính thành phần phần trăm theo khối lượng của mỗi oxit trong hỗn hợp ban đầu.
Hoà tan hoàn toàn 28 gam hỗn hợp trên vào dung dịch HCl 8%. Tính khối lượng dung dịch HCl cần dùng, biết rằng người ta đã dùng axit d...
Đọc tiếp
Khử hoàn toàn 28 gam hỗn hợp gồm CuO và một oxit của sắt bằng khí H2 dư ở nhiệt độ cao. Sau phản ứng thu được hỗn hợp chất rắn, cho hỗn hợp rắn này tác dụng hoàn toàn với axit H2SO4 loãng thấy thoát ra 3,36 lít khí (ở đktc) và 12,8 gam chất rắn.
a. Tìm công thức oxit của sắt
b. Tính thành phần phần trăm theo khối lượng của mỗi oxit trong hỗn hợp ban đầu.
Hoà tan hoàn toàn 28 gam hỗn hợp trên vào dung dịch HCl 8%. Tính khối lượng dung dịch HCl cần dùng, biết rằng người ta đã dùng axit dư 15% so với lí thuyết
dẫn luồng khí h2 đi qua ống có chứa m gam hỗn hợp chất rắn X gồm cuo;fe3o4 và fe2o3 nung nóng, sau một thời gian trong ống sứ còn lại 113,6 gam hỗn hợp chất rắn Y. cho toàn bộ khí và hơi thoát ra hấp thụ vào bình đựng 100g dung dịch h2so4 96,48% ( dư ) , sau thí nghiệm thấy nồng độ dung dịhj h2so4 ở trong bình là 90%. tính m
\(m_{H_2SO_4}=\dfrac{100.96,48}{100}=96,48\left(g\right)\)
\(m_{dd.sau.thí.nghiệm}=\dfrac{96,48.100}{90}=107,2\left(g\right)\)
=> \(m_{H_2O\left(thêm\right)}=107,2-100=7,2\left(g\right)\Rightarrow n_{H_2O}=\dfrac{7,2}{18}=0,4\left(mol\right)\)
=> nO(mất đi) = 0,4 (mol)
Có: mX = mY + mO(mất đi) = 113,6 + 0,4.16 = 120 (g)
Đúng 3
Bình luận (0)
Nung hỗn hợp khí X gồm H2 và N2 trong bình kín với xúc tác thích hợp, sau một thời gian thu được hỗn hợp khí Y có tỉ khối so với He là 2,965. Dẫn toàn bộ Y qua bột CuO (dư) nung nóng, sau khi các phản ứng xảy ra hoàn toàn thấy khối lượng chất rắn giảm 12 gam, đồng thời thu được 8,288 lít (đktc) khí duy nhất. Hiệu suất phản ứng tổng hợp NH3 là : A. 22% B. 23% C. 24% D. 25%
Đọc tiếp
Nung hỗn hợp khí X gồm H2 và N2 trong bình kín với xúc tác thích hợp, sau một thời gian thu được hỗn hợp khí Y có tỉ khối so với He là 2,965. Dẫn toàn bộ Y qua bột CuO (dư) nung nóng, sau khi các phản ứng xảy ra hoàn toàn thấy khối lượng chất rắn giảm 12 gam, đồng thời thu được 8,288 lít (đktc) khí duy nhất. Hiệu suất phản ứng tổng hợp NH3 là :
A. 22%
B. 23%
C. 24%
D. 25%