BT2. Áp suất hơi bão hòa của axit xyanhydric (HCN) phụ thuộc vào nhiệt độ theo pt: lgP (mmHg) = 7,04 - 1237/T.
Xác định nhiệt độ sôi và nhiệt hóa hơi của nó ở điều kiện thường.
Áp suất hơi bão hòa của axit xyanhydric HCN phụ thuộc vào nhiệt độ theo phương trình:
lgP(mmHg) = 7,04 - 1237/T
Xác định nhiệt độ sôi và nhiệt hóa hơi của nó ở điều kiện thường.
pt chuyển pha HCN=HCN
a/s hơi bão hòa Phbh phụ thuộc vào nhiệt độ T theo pt
lgP(mmHg) = 7,04 - 1237/T
\(\Rightarrow\) lnP(mmHg)=lgP(mmHg)/ln(10)=16,21-2848,3/T (1)
xét trong khoảng nhiệt độ tương đối hẹp ta có pt:
lnP=\(\frac{-\lambda}{RT}\)+j (2)
từ (1),(2) suy ra: \(\lambda\) =2848,3. 1,987=5659 ( cal/mol)
ở đk thường, P=1atm= 760mmHg\(\Rightarrow\)lg(760)=7,04-1237/T\(\Rightarrow\)T=297,4K=24,4oC
TTrong khoảng nhiệt độ tương đối hẹp nên: lnP = - \(\frac{\lambda}{RT}\) + C
Ta có : lgP = 7.04 - \(\frac{1237}{T}\) => lnP = (7.04 - \(\frac{1237}{T}\)) ln10
=> \(\frac{-\lambda}{R}\) = - 1237 . ln10 => nhiệt hóa hơi: \(\lambda\) = 1237 . ln10 . R = 1237 . ln10 . 1.987 = 5659,57 (cal/mol)
nhiệt độ sôi của chất lỏng là nhiệt độ tại P = 1atm = 760 mmHg
=> nhiệt độ sôi: \(T_s\) = \(\frac{1237}{7.04-lgP}\) = \(\frac{1237}{7.04-lg760}\) = 297.41 K
Từ pt: logP = 7,04 - \(\frac{1237}{T}\),
Ta có:
lnP = ln10.( 7,04 - \(\frac{1237}{T}\) )
Từ pt clapeyron-clausius II, ta có:
\(\frac{dlnP}{dT}=\frac{\lambda}{R.T^2}\)
\(\Rightarrow\)\(lnP=-\frac{\lambda}{R.T}+j\) \(=-\frac{1237.ln10}{T}+ln10.7,04\)
\(\Rightarrow\)\(\lambda=ln10.1237.R=ln10.1237.1,987=5659,57\)(cal/mol)
Vậy nhiệt hóa hơi của HCN ở dk thường là: 5659,57(cal/mol).
Ta có:
\(logP=7,04-\frac{1237}{T}\)
\(\)ở điều kiện thường p = 1atm= 760 (mmHg ).
\(\Rightarrow log760=7,04-\frac{1237}{T}\)
\(\Leftrightarrow T=297,41\)
Vậy nhiệt độ sôi ở dk thường là: 297,41K
BT5. Ở 46 độ C, áp suất hơi bão hòa của chất A dạng lỏng là 50 mmHg, chất A dạng rắn là 49,5 mmHg. Ở 45 độ C, áp suất hơi bão hòa của A lỏng lớn hơn của A rắn là 1 mmHg. Tính nhiệt nóng chảy, nhiệt thăng hoa và nhiệt độ nóng chảy của chất A. Biết nhiệt hóa hơi của nó là 9 kcal/mol và xem thể tích riêng của A lỏng và A rắn xấp xỉ nhau.
Clorofooc(CHCl3) sôi ở 60,2oC dưới áp suất khí quyển 1 atm . Áp suất hơi của nó tại nhiệt độ này bằng 781 mmHg
Xác định áp suât hơi và nhiệt độ sôi của dd chứa 0,2mol chất tan không bay hơi trong 1 kg clorofooc
Nhiệt bay hơi của clorofooc là 31,64 kJ/mol
Xác định áp suất riêng phần p (theo đơn vị mmHg) của hơi nước trong không khí ẩm ở 28 ° C. Cho biết độ ẩm tỉ đối của không khí là 80% và áp suất nước bão hoà ở nhiệt độ này gần đúng bằng 28,35 mmHg.
A. p = 226,8 mmHg. B. p ≈ 35,44 mmHg.
C. p = 22,68 mmHg. D. p ≈ 354,4 mmHg.
Chọn đáp án C
Độ ẩm tỉ đối của không khí tính bằng:
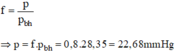
chọn phát biểu sai:
A sự bay hơi là quá trình hóa hơi xảy ra ở bề mặt thoáng của chất lỏng
B sự sôi là quá trình hóa hơi xảy ra cả ở bề mặt thoáng áp suât và trong lòng khối chất lỏng
C sự bay hơi phụ thuộc vào nhiệt độ diện tích mặt thoáng áp suất và bản chất của chất lỏng
D sự sôi phụ thuộc vào nhiệt độ diện tích mặt thoáng áp suất và bàn chất của chất lỏng
Nhiệt độ sôi của clorbenzen ở áp suất thường bằng 405.4 k và ở áp suất 4 mmhg là 383.2 k. Khi áp suất 2 mmhg clorbenzen sẽ sôi ở nhiệt độ bao nhiêu ?
Phân biệt hơi bão hòa với hơi khôi. So sánh áp suất hơi bão hòa với áp suất hơi khô của chất lỏng ở cùng nhiệt độ.
+ Hơi bão hòa là hơi ở trạng thái cân bằng động với chất lỏng của nó: tốc độ bay hơi bằng tốc độ ngưng tụ xảy ra ở bề mặt chất lỏng. Hơi bão hòa có áp suất đạt giá trị cực đại gọi là áp suất hơi bão hòa. Áp suất hơi bão hòa không phụ thuộc thể tích và không tuân theo định luật Bôilơ – Mariốt, nó chỉ phụ thuộc vào bản chất và nhiệt độ của chất lỏng bay hơi.
+ Hơi khô là hơi có tốc độ bay hơi lớn hơn tốc độ ngưng tụ. Hơi khô có áp suất đạt giá trị cực đại. Hơi khô và hơi bão hòa đều gây ra áp suất lên thành bình.
+ Ở cùng nhiệt độ, áp suất hơi khô có giá trị nhỏ hơn, áp suất hơi khô phụ thuộc thể tích và tuân theo định luật Bôilơ – Mariốt.
BT3. Ở áp suất thường, nhiệt độ sôi của nước và cloroform lần lượt là 100 và 60 độ C, nhiệt hóa hơi tương ứng là 12 và 7 kcal/mol. Tính nhiệt độ tại đó 2 chất lỏng trên có cùng áp suất.
Phân biệt hơi bão hòa với hơi khô. So sánh áp suất hơi bão hòa với áp suất hơi khô của chất lỏng ở cùng nhiệt độ?