Một loại quặng photphat có chứa 35% Ca3(PO4)2. Hãy tính hàm lượng phần trăm P2O5 có trong quặng trên.

Những câu hỏi liên quan
Một loại quặng photphat có chứa 35% Ca3(PO4)2. Hãy tính hàm lượng phần trăm P2O5 có trong quặng trên.
Trong 1000g quặng có: 1000. 35% = 350g Ca3(PO4)2
Bảo toàn nguyên tố P ⇒ trong 1 mol Ca3(PO4)2 có 1mol P2O5 nghĩa là trong 310g Ca3(PO4)2 tương ứng có 142g P2O5.
⇒350g Ca3(PO4)2 có lượng P2O5 là:
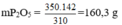
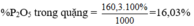
Đúng 0
Bình luận (0)
Khối lượng P2O5 có trong 5 tấn quặng photphat chứa 35% Ca3(PO4)2 là
A. 0,5 tấn B. 0,8 tấn C. 0,7 tấn D. 0,85 tấn
\(m_{Ca_3\left(PO_4\right)_2}=5.35\%=1,75\left(tấn\right)\)
Trong 1 mol Ca3(PO4)2 có 1 mol P2O5
=> Trong 310 tấn Ca3(PO4)2 tương ứng có 142 tấn P2O5
=> Trong 1,75 tấn Ca3(PO4)2 tương ứng có x tấn P2O5
=> x=\(\dfrac{1,75.142}{310}=0,8\left(tấn\right)\)
=> Chọn B
Đúng 2
Bình luận (0)
1 loại quặng photphat chứa 60% là tạp chất, còn lại là ca3(po4)2. Nếu dùng 20 tấn quặng này thì lượng p2o5 điều chế được là bao nhiêu
\(m_{Ca_3\left(PO_4\right)_2}=20\cdot40\%=8\left(tấn\right)=8000\left(kg\right)\)
\(n_{Ca_3\left(PO_4\right)_2}=\dfrac{8000}{310}=\dfrac{800}{31}\left(kmol\right)\)
Bảo toàn nguyên tố P :
\(n_{P_2O_5}=n_{Ca_3\left(PO_4\right)_2}=\dfrac{800}{31}\left(kmol\right)\)
\(m_{P_2O_5}=\dfrac{800}{31}\cdot142=3664.5\left(kg\right)\)
Đúng 2
Bình luận (0)
$m_{Ca_3(PO_4)_2} = 20.(100\%-60\%) = 8(tấn) = 8000(kg)$
Bảo toàn P
$n_{P_2O_5} = n_{Ca_3(PO_4)_2} = \dfrac{8000}{310}(kmol)$
$m_{P_2O_5} = \dfrac{8000}{310}.142 = 3664,5(kg)$
Đúng 0
Bình luận (0)
Một loại quặng photphat dùng để làm phân bón có chứa 35% Ca3(PO4) về khối lượng, còn lại là các chất không chứa photphat. Độ dinh dưỡng của loại phân lân này là: A. 7%. B. 16,03%. C. 25% D. 35%
Đọc tiếp
Một loại quặng photphat dùng để làm phân bón có chứa 35% Ca3(PO4) về khối lượng, còn lại là các chất không chứa photphat. Độ dinh dưỡng của loại phân lân này là:
A. 7%.
B. 16,03%.
C. 25%
D. 35%
Đáp án B
Độ dinh dưỡng của phân lân được đánh giá bằng hàm lượng P2O5 có trong loại phân đó
Lấy 100 gam quặng => mCa3(PO4)2 = 35 (g) => nCa3(PO4)2 = 0,1129 (mol)
BTNT P: => nP2O5 = nCa3(PO4)2 = 0,1129 (mol)
=> Độ dinh dưỡng =% P2O5 = [( 0,1129. 142) :100].100% = 16,03%
Đúng 0
Bình luận (0)
Một loại quặng photphat dùng để làm phân bón có chứa 35% Ca3(PO4)2 về khối lượng, còn lại là các chất không chứa photpho. Độ dinh dưỡng của loại phân lân này là A. 7%. B. 16,03%. C. 25%. D. 35%.
Đọc tiếp
Một loại quặng photphat dùng để làm phân bón có chứa 35% Ca3(PO4)2 về khối lượng, còn lại là các chất không chứa photpho. Độ dinh dưỡng của loại phân lân này là
A. 7%.
B. 16,03%.
C. 25%.
D. 35%.
Đáp án B
Giả sử khối lượng phân là 100g
⇒ mCa3(PO4)3 = 35 gam.
Bảo toàn nguyên tố ta có:
Ca3(PO4)2 → P2O5.
⇒ mP2O5 = 35 × 142/310 = 16,03 gam.
⇒ Độ dinh dưỡng của phân bón đã cho = ![]() = 16,03%.
= 16,03%.
Đúng 0
Bình luận (0)
Một loại quặng photphat dùng để làm phân bón có chứa 35% Ca3(PO4)2 về khối lượng, còn lại là các chất không chứa photpho. Độ dinh dưỡng của loại phân lân này là A. 7%. B. 16,03%. C. 25%. D. 35%.
Đọc tiếp
Một loại quặng photphat dùng để làm phân bón có chứa 35% Ca3(PO4)2 về khối lượng, còn lại là các chất không chứa photpho. Độ dinh dưỡng của loại phân lân này là
A. 7%.
B. 16,03%.
C. 25%.
D. 35%.
Đáp án B
Giả sử khối lượng phân là 100g ⇒ mCa3(PO4)3 = 35 gam.
Bảo toàn nguyên tố ta có: Ca3(PO4)2 → P2O5.
⇒ mP2O5 = 35 × 142/310 = 16,03 gam.
⇒ Độ dinh dưỡng của phân bón đã cho = 16,03×100/100 = 16,03%.
Đúng 0
Bình luận (0)
một quặng photphat có 35% Ca3(PO4)2 . Hãy tính hàm lượng phần trăm P2O5 có trong quặng trên .
Có thể tính như sau: Trong 310 gam Ca3(PO4)2(3CaO.P2O5) có chứa x gam P2O5.
Từ đó ta tính được khối lượng P2O5: x = 142 x (35 : 310) = 16 (g)
Hàm lượng P2O5 là 16%.
Đúng 0
Bình luận (0)
một quặng photphat có 35% Ca3(PO4)2 . Hãy tính hàm lượng phần trăm P2O5 có trong quặng trên .
Có thể tính như sau: Trong 310 gam Ca3(PO4)2(3CaO.P2O5) có chứa x gam P2O5.
Từ đó ta tính được khối lượng P2O5: x = 142 x (35 : 310) = 16 (g)
Hàm lượng P2O5 là 6%.
Đúng 0
Bình luận (0)
Một loại quặng photphat có chứa 35% Ca3(PO4)2. Hãy tính hàm lượng phần trăm P2O5 có trong quặng trên.
Có thể tính như sau: Trong 310 gam Ca3(PO4)2(3CaO.P2O5) có chứa x gam P2O5.
Từ đó ta tính được khối lượng P2O5: x = 142 x (35 : 310) = 16 (g)
Hàm lượng P2O5 là 6%.
Đúng 0
Bình luận (0)

















