
Những câu hỏi liên quan
Đốt cháy hoàn toàn một hidrocacbon X thu được 8,96 lít khí CO2 (đktc) và 9 gam nước. Xác định CTPT của X.
A
.
C
4
H
10
B
.
C
5
H
12
C
.
C
4
H...
Đọc tiếp
Đốt cháy hoàn toàn một hidrocacbon X thu được 8,96 lít khí CO2 (đktc) và 9 gam nước. Xác định CTPT của X.
A . C 4 H 10
B . C 5 H 12
C . C 4 H 8
D . C 5 H 10
nCO2 = 0,4 mol => nC = 0,4 mol
nH2O = 0,5 mol => nH = 0,5 . 2 = 1 mol
C : H = 0,4 : 1 = 4 : 10
X là C4H10
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 784ml khí (đktc) một hidrocacbon X thu được 3,08 gam
C
O
2
và 0,63 gam nước. Công thức phân tử của X là A.
C
2
H
4
B.
C
2
H
2
C.
C
H
4
D.
C
6
H
6
Đọc tiếp
Đốt cháy hoàn toàn 784ml khí (đktc) một hidrocacbon X thu được 3,08 gam C O 2 và 0,63 gam nước. Công thức phân tử của X là
A. C 2 H 4
B. C 2 H 2
C. C H 4
D. C 6 H 6
Đốt cháy hoàn toàn một hidrocacbon X ở thể khí thu được 0,14 mol CO2 và 1,89g H2O. Tìm CTPT và CTCT của X biết X có thể trùng hợp tạo thành cao su?
Một hỗn hợp gồm 2 hidrocacbon A, B có cùng công thức tổng quát là CnH2n+2. X chiếm cùng thể tích với 10,24g O2 ở cùng điều kiện nhiệt độ và áp suất. Đốt cháy hết hỗn hợp X ta thu được 21,504l CO2 (đktc).a) Tính n trung bình và xác định các công thức có thể có của A,B biết rằng x4b)Tính thể tích O2 ở đktc cần dùng để đốt cháy hỗn hợp X và khối lượng nước thu được
Đọc tiếp
Một hỗn hợp gồm 2 hidrocacbon A, B có cùng công thức tổng quát là CnH2n+2. X chiếm cùng thể tích với 10,24g O2 ở cùng điều kiện nhiệt độ và áp suất. Đốt cháy hết hỗn hợp X ta thu được 21,504l CO2 (đktc).
a) Tính n trung bình và xác định các công thức có thể có của A,B biết rằng x<=4
b)Tính thể tích O2 ở đktc cần dùng để đốt cháy hỗn hợp X và khối lượng nước thu được
Đốt cháy hoàn toàn 4,4 gam một hợp chất hữu cơ X có dạng tổng quát là C_nH_{2n}O_2, thu được V lít khí CO_2 (đktc) và 3,6 gam H_2O.1. Xác định công thức phân tử của X.2. Hấp thụ hoàn toàn V lít khí CO_2 thu được ở trên vào 150ml dung dịch Baleft(OHright)_2 1M, thu được m gam kết tủa. Viết phương trình hóa học của các phản ứng xảy ra và tính giá trị của m.3. Cho 4,4 gam X tác dụng vừa đủ với dung dịch NaOH, thu được 4,1 gam muối. Xác định công thức cấu tạo của X.
Đọc tiếp
Đốt cháy hoàn toàn 4,4 gam một hợp chất hữu cơ \(X\) có dạng tổng quát là \(C_nH_{2n}O_2\), thu được \(V\) lít khí \(CO_2\) (đktc) và 3,6 gam \(H_2O\).
1. Xác định công thức phân tử của \(X\).
2. Hấp thụ hoàn toàn \(V\) lít khí \(CO_2\) thu được ở trên vào 150ml dung dịch \(Ba\left(OH\right)_2\) 1M, thu được \(m\) gam kết tủa. Viết phương trình hóa học của các phản ứng xảy ra và tính giá trị của \(m\).
3. Cho 4,4 gam \(X\) tác dụng vừa đủ với dung dịch \(NaOH\), thu được 4,1 gam muối. Xác định công thức cấu tạo của \(X\).
1)
$n_{H_2O} = \dfrac{3,6}{18}= 0,2(mol)$
Bảo toàn nguyên tố C,H :
$C_nH_{2n}O_2 \to nCO_2 + nH_2O$
$\Rightarrow n_{CO_2} = n_{H_2O} = 0,2(mol)$
$\Rightarrow n_C = 0,2(mol) ; n_H = 0,4(mol)$
$\Rightarrow n_O = \dfrac{4,4 - 0,2.12-0,4.1}{16} = 0,1(mol)$
$n_X = \dfrac{1}{2}n_O = 0,05(mol)$
$\Rightarrow M_X = 12n + 2n + 32 = \dfrac{4,4}{0,06} = 88$
$\Rightarrow n = 4$
Vậy CTPT của X là $C_4H_8O_2$
2)
$n_{Ba(OH)_2} = 0,15(mol) < n_{CO_2} = 0,2(mol)$
\(Ba\left(OH\right)_2+CO_2\rightarrow BaCO_3+H_2O\)
0,15 0,15 0,15 (mol)
\(BaCO_3+CO_2+H_2O\rightarrow Ba\left(HCO_3\right)_2\)
0,05 0,05 (mol)
$\Rightarrow n_{BaCO_3} = 0,15 - 0,05 = 0,1(mol)$
$\Rightarrow m = 0,1.197 = 19,7(gam)$
3)
CTTQ của muối : $RCOONa$
$n_{muối} = n_X = 0,05(mol) \Rightarrow M_{muối} = R + 67 = \dfrac{4,1}{0,05} = 82$
$\Rightarrow R = 15(-CH_3)$
Vậy CTCT của X là $CH_3COOC_2H_5$
Đúng 3
Bình luận (0)
Đốt cháy hoàn toàn hh X gồm 2 hidrocacbon A (CnH2n-2) và B (CmH2m) thu được 15,68 lít CO2 ở đktc và 14,4 gam H2O. Biết X chiếm thể tích là 6,72 lít ở đktc. Xác định tp % thể tích của hỗn hợp X, xác định CTPT của A,B
Đốt cháy hoàn toàn một hidrocacbon X, sau phản ứng thu được 3 lít CO2 và 4 lít hơi nước (thể tích khí và hơi đo ở cùng điều kiện nhiệt độ và áp suất). Công thức phân tử của X là: A. C3H4. B. C3H8. C. C4H6. D. C4H8
Đọc tiếp
Đốt cháy hoàn toàn một hidrocacbon X, sau phản ứng thu được 3 lít CO2 và 4 lít hơi nước (thể tích khí và hơi đo ở cùng điều kiện nhiệt độ và áp suất). Công thức phân tử của X là:
A. C3H4.
B. C3H8.
C. C4H6.
D. C4H8
Đáp án B
C : H = nC:nH = VCO2/2VH2O = 3/8
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn một hidrocacbon X, sau phản ứng thu được 3 lít CO2 và 4 lít hơi nước (thể tích khí và hơi đo ở cùng điều kiện nhiệt độ và áp suất). Công thức phân tử của X là: A. C3H4 B C3H8 C. C4H6 D C4H8
Đọc tiếp
Đốt cháy hoàn toàn một hidrocacbon X, sau phản ứng thu được 3 lít CO2 và 4 lít hơi nước (thể tích khí và hơi đo ở cùng điều kiện nhiệt độ và áp suất). Công thức phân tử của X là:
A. C3H4
B C3H8
C. C4H6
D C4H8
Đáp án B
C : H = nC:nH = VCO2/2VH2O = 3/8
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn một hidrocacbon X, sau phản ứng thu được 3 lít CO2 và 4 lít hơi nước (thể tích khí và hơi đo ở cùng điều kiện nhiệt độ và áp suất). Công thức phân tử của X là: A. C3H4. B C3H8. C. C4H6. D C4H8.
Đọc tiếp
Đốt cháy hoàn toàn một hidrocacbon X, sau phản ứng thu được 3 lít CO2 và 4 lít hơi nước (thể tích khí và hơi đo ở cùng điều kiện nhiệt độ và áp suất). Công thức phân tử của X là:
A. C3H4.
B C3H8.
C. C4H6.
D C4H8.
Đáp án B
C : H = nC:nH = VCO2/2VH2O = 3/8
Đúng 0
Bình luận (0)







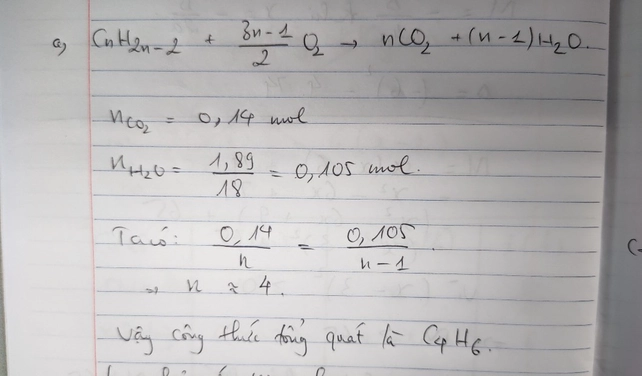
 Bạn tham khảo nhé!
Bạn tham khảo nhé!







