1. Trình bày phương pháp điều chế oxi trong phòng thí nghiệm từ KMno4.
2. Trình bày phương pháp điều chế hiđro trong phòng thí nghiệm từ Zn và dung dịch HCl.
3. Có mấy cách thu khí hiđro và oxi? Giải thích.
Hãy trình bày các phương pháp điều chế khí oxi trong phòng thí nghiệm và trong công nghiệp. Tại sao không áp dụng phương pháp điều chế khí trong phòng thí nghiệm, và ngược lại?
Điều chế oxi:
- Trong phòng thí nghiệm, oxi được điều chế bằng cách phân hủy những hợp chất giàu Oxi và ít bên với nhiệt như KMnO4, KClO3, ...
2KMnO4 → K2MnO4 + MnO2 + O2
2KClO3 → 2KCl + 3O2
- Trong công nghiệp:
a) Từ không khí: Không khí sau khi đã loại bỏ hết hơi nước, khí CO2, được hóa lỏng dưới áp suất 200 atm đồng thời hạ thấp nhiệt độ. Chưng cất phân đoạn không khí lỏng, thu được oxi lỏng. Oxi lỏng được vận chuyển trong những bình thép có thể tích 100 lít dưới áp suất 150atm.
b) Từ nước. Điện phân nước: 2H2O
Người ta không áp dụng phương pháp phòng thí nghiệm cho phòng thí nghiệm vì trong phòng thí nghiệm chỉ điều chế lượng nhỏ oxi, còn công nghiệp cần một lượng lớn giá thảnh rẻ.
1. phương pháp thu khí hidro và oxi? giải thích tại sao?
2. nêu cách tiến hành thí nghiệm điều chế hidro và oxi trong phòng thí nghiệm
Cách thu khí ôxi : Bằng cách đẩy nước và đẩy không khí .
Cách thu khí hiđrô : Giống ôxi .
Cách tiến hành :
- Cho một lượng nhỏ (bằng hạt ngô) KMnO4 vào đáy ống nghiệm. Đặt một ít bồng gần miệng ống nghiệm.
- Dùng nút cao su có ống dẫn khí xuyên qua đậy kín ống nghiệm. Đặt ống nghiệm vào giá đỡ hoặc kẹp gỗ sao cho đáy ống nghiệm cao hơn miệng ống nghiệm chút ít.
- Nhánh dài của ống dẫn khí sâu gần sát đáy ống nghiệm (hoặc lọ thu).
- Dùng đèn cồn đun nóng cả ống nghiệm chứa KMnO4, sau đó tập trung đốt nóng phần có hóa chất. Kali pemanganat bị phân hủy tạo ra khí oxi. Nhận ra khí trong ống nghiệm (2) bằng que đóm còn hồng.
- Sau khi kiểm tra độ kín của các nút, đốt nóng ống nghiệm chứa KMnO4. Khí oxi sinh ra sẽ đẩy không khí hoặc đẩy nước và chứa trong ống nghiệm thu. Dùng nút cao su đậy kín ống nghiệm đã chứa đẩy bình oxi để dùng cho thí nghiệm sau.
1) Đẩy nước và đẩy không khí do tính không tan trong nước của hai khi và tính nặng hơn không khí của oxi và tính nhẹ hơn không khí của hidro
2)
- Điều chế H2 : Cho viên kẽm vào dung dịch HCl lấy dư
$Zn + 2HCl \to ZnCl_2 + H_2$
- Điều chế O2 :Nung KMnO4 trên ngọn lửa đèn cồn
$2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2$
trình bày phương pháp hoá học nhận biết khí oxi cách điều chế khí oxi trong phòng thí nhiệm
refer
Điều chế, sản xuất Oxi (O2) trong phòng thí nghiệm và trong công nghiệp - hoá 8 bài 27
bấm vào ^
nhận biết khí Oxi bằng cách cho que đóm đang cháy vào lọ chứa khí Oxi
chúng sẽ cháy to
điều chế oxi bằng cách phân hủy cách chất giàu oxi và dễ phân hủy
điều chế Oxi bằng 2 phương pháp : đẩy nước và đẩy không khí
lưu ý : khi đẩy không khí ta phải để bình đựng khí ở trạng thái ngửa vì Oxi nặng hơn không khí
Các chất khí điều chế trong phòng thí nghiệm thường được thu theo phương pháp đẩy không khí (cách 1, cách 2) hoặc đẩy nước (cách 3, cách 4) như các hình vẽ dưới đây:
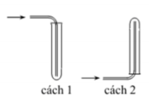
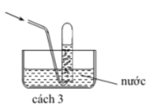
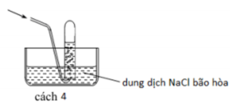
Trong phòng thí nghiệm, có thể điều chế khí hiđro clorua bằng cách cho tinh thể NaCl tác dụng với axit H 2 S O 4 đậm đặc và đun nóng:
![]()
![]()
Dùng cách nào trong bốn cách trên để thu khí HCl?
A. Cách 1
B. Cách 2
C. Cách 3
D. Cách 4
Các chất khí điều chế trong phòng thí nghiệm thường được thu theo phương pháp đẩy không khí (cách 1, cách 2) hoặc đẩy nước (cách 3, cách 4) như các hình vẽ dưới đây:
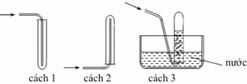
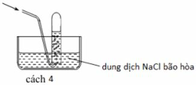
Trong phòng thí nghiệm, có thể điều chế khí hiđro clorua bằng cách cho tinh thể NaCl tác dụng với axit H 2 S O 4 đậm đặc và đun nóng:
NaOH+ H 2 S O 4 đ ặ c → t ∘ N a H S O 4 +HCl
Dùng cách nào trong bốn cách trên để thu khí HCl?
A. Cách 1
B. Cách 2
C. Cách 3
D. Cách 4
Hãy nêu phương pháp điều chế và thu khí hidro trong phòng thí nghiệm. Cách đặt ống nghiệm có gì khác so với cách thu khí oxi?
- Phương pháp điều chế: cho các kim loại (Al, Mg, Fe, Zn,...) tác dụng với dd axit (HCl, H2SO4 loãng,...)
- Cách thu: ngửa bình
- Khác với cách thu oxi: Thu oxi thì phải úp bình
1. Tính chất vật lí , hoá học của oxi 2. Định nghĩa oxit , công thức của oxit , phân loại và cách gọi tên oxit 3. Điều chế khí oxi trong phòng thí nghiệm 4. Tính chất vật lí , hoá hợp của hiđro 5. Điều chế khí hiđro trong phòng thí nghiệm
Nêu phương pháp điều chế hidro, oxi trong phòng thí nghiệm? Cách thu khí hidro, oxi?
Cách điều chế oxi:dùng KMnO4,KClO3
Cách điều chế hidro:dùng kẽm và axit clohidric hay điện phân nước
Cách thu khí oxi:bằng cách đẩy nước và đẩy không khí
Cách thu khí hiđrô : giống oxi
điều chế O2 dùng KClO3 , KMnO4
điều chế H2 cho kim loại (Zn,Mg,...)vào axit(HCl,H2SO4,...)
cách thu H2,O2 : đẩy nước và đẩy kk
theo dõi mình nhé ♥♥♥
Trong phòng thí nghiệm hóa học có các kim loại kẽm và sắt, dung dịch HCl và axit H2SO4.
a) Viết các phương trình hóa học có thể điều chế hiđro;
b) Phải dùng bao nhiêu gam kẽm, bao nhiêu gam sắt để điều chế được 2,24 lít khí hiđro (đktc)?
Phương trình hóa học của phản ứng:
Fe + H2SO4 → FeSO4 + H2.
Zn + H2SO4 → ZnSO4 + H2.
Fe + 2HCl → FeCl2 + H2.
Zn + 2HCl → ZnCl2 + H2.
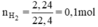
Theo phương trình (3) mFe cần dùng: 56.0,1 = 5,6g.
Theo phương trình (4) mZn cần dùng: 65.0,1 = 6,5g.