Cho 0,53g muối cacbonat hóa trị I tác dụng vừa hết với dung dịch HCl 3,65% thấy thoát ra 1,12ml khí (đktc) và thu được dung dịch A.
a. Xác định CTHH của muối cacbonat.
b. Tính nồng độ phần trăm dung dịch A
Cho 19,5 Zn tác dụng hết với 300g dung dịch HCl
a. Tính nồng độ phần trăm của dung dịch HCl đã dùng
b. Tính thể tích khí thoát ra (ở đktc)
c. Tính nồng độ phần trăm của dung dịch muối thu được sau phản ứng
n Zn= 19,5/65=0,3 (mol).
PTPƯ: Zn(0.3) + HCl(0.6) ----> ZnCl2(0.3) + H2(0,3)
mHCl=0,6.36.5=21.9(g)
a) C%HCl= 21.9/300.100%=7,3%
b) VH2=0,3.22,4=6,72(lít)
c) mH2=0,3.2=0,6(g)
mZnCl2=0,3.136=40,8(g)
mddZnCl2 =(19,5+300)-0,6=318,9(g)
C%=mZnCl2/mddZnCl2.100= 40,8/318,9.100=12,793%
Cho 1,06 gam muối cacbonat kim loại hoá trị I tác dụng hết với dung dịch HCl thấy thoát ra 224 mi khí cacbonic (ở đktc). Xác định công thức phân tử muối cacbonat.
Gọi M là kí hiệu nguyên tử khối của kim loại hoá trị I. Công thức muối là M 2 CO 3 . Phương trình hoá học của phản ứng :
M 2 CO 3 + 2HCl → 2 MCl 2 + H 2 O + CO 2
(2M + 60)g 22400ml
1,06g 224ml
Theo phương trình hóa học trên ta có:
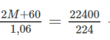
→ M = 23. Đó là muối Na 2 CO 3
Giải giúp em bài này với ạ!
Hòa tan 2g muối cacbonat của kim loại hóa trị II bằng dung dịch HCl 10% vừa đủ thu được 448cm3 chất khí ở đktc
a/ Tính mddHCl
b/ xác định CTHH của muối
c/ tính nồng độ phần trăm của chất tan trong dung dịch
gọi công thức muối là ACO3
n CO2=0,448:22,4=0,02mol
PTHH: ACO3+2HCl=>ACl2+CO2+H2O
0,02<--0,04<-0,02<-0,02->0,02
=> mHCl=0,04.36,5=1,46g
=> mddHCl=\(\frac{1,46}{10}.100=14,6g\)
ta có MACO3=2:0,02=100g/mol
=> M A=100-12-16.3=40
=> A là Ca
=> công thức muois là CACO3
ta có m CaCl2=0,02.111=2,22g
=> mddCaCl2=2+14,6-0,02.44-0,02.18=15,36g
=> C% CaCl2=2,22:15,36.100=14,45%
448 cm3 = 0,448 l
Gọi CTHH của muối cacbonat cần tìm là MCO3
MCO3 + 2HCl = MCl2 + CO2 + H2O
=> Khí thu được là CO2
Số mol CO2 là : 4,48 : 22,4 = 0,2 (mol)
Khối lượng CO2 là: 0,2 x 44 = 8,8 (g)
Theo PTHH: nHCl = 2 nCO2 = 0,2 x 2= 0,4 (mol)
Khối lượng HCl là: 0,4 x 36,5 = 14,6 (g)
Khối lượng dd HCl là : 14,6 : 10 x 100 = 146 (g)
Theo PTHH: nMCO3 = nCO2 = 0,2 (mol)
Khối lượng mol của MCO3 là: 20 : 0,2 = 100 (g)
Khối lượng mol của M: 100- 60 = 40 (g)
=> M là kim loại Ca
=> Muối cần tìm là CaCO3
Chất tan trong dung dịch là CaCl2
Theo PTHH: nCaCl2 = nCO2 = 0,2 (mol)
Khối lượng CaCl2 là : 111 x 0,2 = 22,2 (g)
Khối lượng dd mới là: 20 + 146 - 8,8 = 157,2 (g)
C% dd CaCl2 là: 22,2 :157,2 x 100 = 14,122%
Bạn ơi hình như bạn ghi sai đề, mk nghĩ muối cacbonat là 20g, không thể 2g được, bạn tham khảo nha
Cho 21,2 g muối cacbonate của kim loại R có hóa trị 1 tác dụng hết với dung dịch HCl thấy thoát ra 4,958 lít khí CO2 ở điều kiện chuẩn xác định công thức muối cacbonat và tính phần trăm theo khối lượng của mỗi nguyên tố có trong mỗi cacbonate
\(n_{CO_2}=\dfrac{V}{24,79}=0,2\left(mol\right)\)
PTHH: \(R_2CO_3+2HCl\rightarrow2RCl+CO_2+H_2O\)
Mol: 0,2 0,2
\(\Rightarrow n_{R_2CO_3}=0,2\left(mol\right)\)
Mặt khác: \(n_{R_2CO_3}=\dfrac{m}{M}\Rightarrow\dfrac{m}{M}=0,2\)
\(\Rightarrow M=\dfrac{m}{0,2}\Leftrightarrow2R+12+3\cdot16=\dfrac{21,2}{0,2}\)
\(\Rightarrow R=23=Na\)
\(\Rightarrow\left\{{}\begin{matrix}\%Na=\dfrac{2M_{Na}}{M}\cdot100\%=\dfrac{2\cdot23}{23\cdot2+12+16\cdot3}\cdot100\%\approx43,4\%\\\%O=\dfrac{3M_O}{M}\cdot100\%=\dfrac{3\cdot16}{23\cdot2+12+16\cdot3}\cdot100\%\approx45,3\%\\\%C=100\%-\%Na-\%O\approx11,3\%\end{matrix}\right.\)
Cho 7,0 gam hỗn hợp hai muối cacbonat của kim loại hóa trị II tác dụng hết với dung dịch HCl thấy thoát ra V lít khí ở đktc. Cô cạn dung dịch sau phản ứng thu được 9,2 gam muối khan. Giá trị của V là:
A. 1,12 lít
B. 2,24 lít
C. 3,36 lít
D. 4,48 lít
Đáp án D
Đặt công thức của hai muối là RCO3: x mol
RCO3+ 2HCl → RCl2+ CO2+ H2O
x 2x x x mol
Theo định luật bảo toàn khối lượng:
mmuối cacbonat+ mHCl= m muối clorua+ mCO2+ mH2O
→ 7,0 + 2x. 36,5=9,2+ 44x+18x → x= 0,2 mol→ VCO2= 0,2.22,4= 4,48 lít
7: Cho 15,9 gam muối cacbonat của kim loại M (có hóa trị (I) trong hợp chất) tác dụng vừa đủ
với V ml dung dịch HCl 075M tạo ra 3,36 lít khí (đktc) và dung dịch X.
a) Xác định tên kim loai M.
b) Tính V và nồng độ mol của chất có trong dung dịch X.
\(a,n_{CO_2}=\dfrac{3,36}{22,4}=0,15(mol)\\ PTHH:M_2CO_3+2HCl\to 2MCl+H_2O+CO_2\uparrow\\ \Rightarrow n_{M_2CO_3}=n_{CO_2}=0,15(mol)\\ \Rightarrow M_{M_2CO_3}=\dfrac{15,9}{0,15}=106(g/mol)\\ \Rightarrow M_{M}=\dfrac{106-12-16.3}{2}=23(g/mol)\)
Vậy M là natri (Na)
\(b,n_{HCl}=2n_{CO_2}=0,3(mol)\\ \Rightarrow V_{dd_{HCl}}=\dfrac{0,3}{0,75}=0,4(l)\\ X:NaCl\\ n_{NaCl}=n_{HCl}=0,3(mol)\\ \Rightarrow C_{M_{NaCl}}=\dfrac{0,3}{0,4}=0,75M\)
Một cốc đựng dung dịch muối cacbonat của một kim loại hóa trị II .Rót từ từ dung dịch H2SO4 có nồng độ 20% vào cốc cho đến khi khí thoát ra vừa hết thì thu được dung dịch muối có nồng độ 24,91%.Hãy xác định muối cacbonat của kim loại gì ?
gọi dd muối CO3 là ACO3
ACO3 +H2SO4 -->ASO4 +CO2+H2O
giả sử có 1 mol ACO3
=>mACO3= MA +60(g)
theo PTHH : nH2SO4=nACO3=1(mol)
=>mdd H2SO4=1.98.100/20=490(g)
nASO4=nACO3=1(mol)
=>mASO4=MA +96(g)
nCO2=nACO3=1(mol)
=>mCO2=44(g)
=>\(\dfrac{MA+96}{MA+60+490-44}\).100=24,91
giải ra ta được MA=40(g/mol0
=>ACO3:CaCO3
ta có pthh: ACO3 +H2SO4--ASO4+H2O+CO2
(A+60)g......98g.......(A+96)g..........44g
mdd H2SO4=(98.100):20=490g
mdd muối sau phản ứng=(A+60)+490-44= (A+506)g
theo đê bài ta có:C% ASO4=(A+96).100:A+506
suy ra A=40 CÓ: CTHH :CACO3
mdd muối sau phản ứng=(A+60)+490-44: (A+506)g=24,91%
Hòa tan hoàn toàn 13 gam Zn cần dùng vừa đủ dung dịch axit HCl 7,3% thu được dung dịch muối X và thấy thoát ra V lít khí H2 (ở đktc) a. Tính giá trị của V? b. Tính khối lượng dung dịch axit HCl đã phản ứng? c. Tính nồng độ phần trăm của muối trong X?
a)
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
0,2-->0,4----->0,2--->0,2
=> VH2 = 0,2.22,4 = 4,48 (l)
b) mHCl = 0,4.36,5 = 14,6 (g)
=> \(m_{dd.HCl}=\dfrac{14,6.100}{7,3}=200\left(g\right)\)
c)
mdd sau pư = 13 + 200 - 0,2.2 = 212,6 (g)
mZnCl2 = 0,2.136 = 27,2 (g)
=> \(C\%=\dfrac{27,2}{212,6}.100\%=12,8\%\)
Hòa tan hoàn toàn 13 gam Zn cần dùng vừa đủ dung dịch HCl 7,3 % thu được dung dịch X và thấy thoát ra V lít khí H2 (ở đktc)
a. Viết phương trình phản ứng hóa học?
b. Tính giá trị của V?
c. Tính khối lượng muối thu được?
d. Tính nồng độ phần trăm muối trong X?
a, \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
b, \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Zn}=0,2\left(mol\right)\Rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)\)
c, \(n_{ZnCl_2}=n_{Zn}=0,2\left(mol\right)\Rightarrow m_{ZnCl_2}=0,2.136=27,2\left(g\right)\)
d, \(n_{HCl}=2n_{Zn}=0,4\left(mol\right)\Rightarrow m_{HCl}=0,4.36,5=14,6\left(g\right)\)
\(\Rightarrow m_{ddHCl}=\dfrac{14,6}{7,3\%}=200\left(g\right)\)
⇒ m dd sau pư = 13 + 200 - 0,2.2 = 212,6 (g)
\(\Rightarrow C\%_{ZnCl_2}=\dfrac{27,2}{212,6}.100\%\approx12,79\%\)