Đốt cháy 1,2 g Mg trong 3,36 lít oxi (đktc)
a)Viết PTPƯ
b)Chất nào dự tính khối lượng chất dư
c)Tính khối lượng của chất sản phẩm
Để đốt cháy hoàn toàn 2,50 g chất A phải dùng vừa hết 3,36 lít O 2 (đktc). Sản phẩm cháy chỉ có C O 2 và H 2 O , trong đó khối lượng C O 2 hơn khối lượng H 2 O là 3,70 g. Tính phần trăm khối lượng của từng nguyên tố trong chất A.
Khi A tác dụng với O 2 chỉ sinh ra, và H 2 O , vậy A có chứa cacbon, hiđro, có thể có hoặc không có oxi.
Theo định luật bảo toàn khối lượng :
m C O 2 + m H 2 O = m A + m O 2 = 7,30 (g) (1)
Theo đầu bài: m C O 2 + m H 2 O = 3,70(g). (2)
Từ hệ (1) và (2), tìm được m C O 2 = 5,50 g; m H 2 O = 1,80 g.
Khối lượng C trong 5,50 g
C
O
2
: 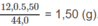
Khối lượng H trong 1,8 g
H
2
: 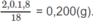
Đó cũng là khối lượng c và H trong 2,50 g chất A. Vậy chất A phải chứa O.
Khối lượng O trong 2,50 g A: 2,50 - 1,50 - 0,200 = 0,80 (g)
Phần trăm khối lượng của C: 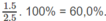
Phần trăm khối lương của H: 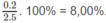
Phần trăm khối lương của O: 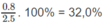
3. Đốt cháy 4,8 gam magie trong 3,36 lít khí Oxi ở điều kiện tiêu chuẩn.a. Chất nào còn dư sau phản ứng và dư bao nhiêu gam (lit - đktc)?b. Tính khối lượng sản phẩm thu được
a)
\(n_{Mg} = \dfrac{4,8}{24} = 0,2(mol)\\ n_{O_2} = \dfrac{3,36}{22,4}= 0,15(mol)\\ 2Mg + O_2 \xrightarrow{t^o} 2MgO\)
Ta thấy :
\( \dfrac{n_{Mg}}{2} = 0,1 < n_{O_2} = 0,15 \) nên O2 dư.
\(n_{O_2\ pư} = \dfrac{n_{Mg}}{2} = 0,1(mol)\\ m_{O_2\ dư} = (0,15-0,1).32 = 1,6(gam)\\ V_{O_2\ dư} = (0,15-0,1).22,4 = 1,12(lít)\)
b)
\(n_{MgO} = n_{Mg} = 0,2\ mol\\ \Rightarrow m_{MgO} = 0,2.40 = 8\ gam\)
1.cho 31(g) Natri oxit vào 27(g)H2O.
a,viết phương trình phản ứng
b,tính khối lượng sản phẩm thu được
c,tính khối lượng chất còn dư sau phản ứng
2.Đốt cháy 2,24 lít khí metan(CH4) bằng 3,36 lít khí O2(đktc)
a,viết phương trình phản ứng và tính số mol các chất trước phản ứng
b,sau phản ứng chất nào dư?tính V khí dư
c,tính tổng khối lướng sản phẩm thu được
mình cần gấp.giúp mình với
Bài 1:
a, PT: \(Na_2O+H_2O\rightarrow2NaOH\)
b, Ta có: \(n_{Na_2O}=\dfrac{31}{62}=0,5\left(mol\right)\)
\(n_{H_2O}=\dfrac{27}{18}=1,5\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,5}{1}< \dfrac{1,5}{1}\), ta được H2O dư.
Theo PT: \(n_{NaOH}=2n_{Na_2O}=1\left(mol\right)\)
\(\Rightarrow m_{NaOH}=1.40=40\left(g\right)\)
b, Theo PT: \(n_{H_2O\left(pư\right)}=n_{Na_2O}=0,5\left(mol\right)\)
\(\Rightarrow n_{H_2O\left(dư\right)}=1,5-0,5=1\left(mol\right)\)
\(\Rightarrow m_{H_2O\left(dư\right)}=1.18=18\left(g\right)\)
Bài 2:
a, PT: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
Ta có: \(n_{CH_4}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(n_{O_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
b, Xét tỉ lệ: \(\dfrac{0,1}{1}>\dfrac{0,15}{2}\), ta được CH4 dư.
Theo PT: \(n_{CH_4\left(pư\right)}=\dfrac{1}{2}n_{O_2}=0,075\left(mol\right)\)
\(\Rightarrow n_{CH_4\left(dư\right)}=0,1-0,075=0,025\left(mol\right)\)
\(\Rightarrow V_{CH_4\left(dư\right)}=0,025.22,4=0,56\left(l\right)\)
c, Theo PT: \(\left\{{}\begin{matrix}n_{CO_2}=\dfrac{1}{2}n_{O_2}=0,075\left(mol\right)\\n_{H_2O}=n_{O_2}=0,15\left(mol\right)\end{matrix}\right.\)
⇒ m sản phẩm = mCO2 + mH2O = 0,075.44 + 0,15.18 = 6 (g)
1.cho 31(g) Natri oxit vào 27(g)H2O.
a,viết phương trình phản ứng
b,tính khối lượng sản phẩm thu được
c,tính khối lượng chất còn dư sau phản ứng
2.Đốt cháy 2,24 lít khí metan(CH4) bằng 3,36 lít khí O2(đktc)
a,viết phương trình phản ứng và tính số mol các chất trước phản ứng
b,sau phản ứng chất nào dư?tính V khí dư
c,tính tổng khối lướng sản phẩm thu được
mình cần gấp.giúp mình với
đốt cháy hoàn toàn 15.4 g hỗn hợp chất a gồm zn và mg cần 3,36 lít ( đktc) a, tính khối lượng mỗi kim loại trong a . b, tính khối lượng mỗi oxit thu đc
\(n_{H2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Pt : \(2Zn+O_2\underrightarrow{t^o}2ZnO|\)
2 1 2
a 0,5b 0,2
\(2Mg+O_2\underrightarrow{t^o}2MgO|\)
2 1 2
b 0,5b 0,1
a) Gọi a là số mol của Zn
b là số mol của Mg
\(m_{Zn}+m_{Mg}=15,4\left(g\right)\)
⇒ \(n_{Zn}.M_{Zn}+n_{Mg}.M_{Mg}=15,4g\)
⇒ 65a + 24b = 15,4g (1)
Theo phương trình : 0,5a + 0,5b = 0,15 (2)
65a + 24b = 15,4g
0,5a + 0,5b = 0,15
⇒ \(\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\)
\(m_{Zn}=0,2.65=13\left(g\right)\)
\(m_{Mg}=01.24=2,4\left(g\right)\)
b) Có : \(n_{ZnO}=\dfrac{0,2.2}{2}=0,2\left(mol\right)\)
⇒ \(m_{ZnO}=0,2.81=16,2\left(g\right)\)
\(n_{MgO}=\dfrac{0,1.2}{2}=0,1\left(mol\right)\)
⇒ \(m_{MgO}=0,1.40=4\left(g\right)\)
Chúc bạn học tốt
\(n_{O_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\ Đặt:n_{Zn}=a\left(mol\right);n_{Mg}=b\left(mol\right)\left(a,b>0\right)\\ 2Zn+O_2\underrightarrow{^{to}}2ZnO\\a.........0,5a..........a\left(mol\right)\\ 2Mg+O_2\underrightarrow{^{to}}2MgO\\b..........0,5b...........b\left(mol\right)\\ \Rightarrow\left\{{}\begin{matrix}65a+24b=15,4\\0,5a+0,5b=0,15\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\\ \Rightarrow m_{Zn}=0,2.65=13\left(g\right);m_{Mg}=0,1.24=2,4\left(g\right)\\ b.m_{ZnO}=81.0,2=16,2\left(g\right)\\ m_{MgO}=0,1.40=4\left(g\right)\)
Câu 5. Đốt cháy 16,8 g sắt trong bình chứa 6,72 lít oxi (đktc) thu được oxit sắt từ (Fe3O4). Hỏi a) Viết phương trình hóa học của phản ứng ? b) Sau khi cháy chất nào dư, dư bao nhiêu gam? c) Tính khối lượng sản phẩm thu được ?
nFe = 16.8/56 = 0.3 (mol)
nO2 = 6.72/22.4 = 0.3 (mol)
2Fe + 3O2 -to-> Fe3O4
0.2___0.3________0.1
mFe dư = ( 0.3 - 0.2 ) * 56 = 5.6 (g)
mFe3O4 = 0.1*232 = 23.2 (g)
a)
3Fe+2O2→Fe3O4
b)
nO2=6,72/22,4=0,3mol
Ta có: nFe3O4=0,3/3=0,1
mFe3O4=0,1.232=23,2g
1). Đốt 6,4 g kim loại đồng trong bình chứa 1,12 lít khí O2 (đktc).
a) Viết PTHH của phản ứng.
b) Sau phản ứng chất nào hết, chất nào dư và dư bao nhiêu mol?
c) Tính khối lượng chất sản phẩm thu được.
2). Đốt cháy 13,5 g Al trong bình chứa 6,67 lít khí oxi (đktc) cho đến khi phản ứng xảy ra hoàn toàn. Tính khối lượng sản phẩm thu được.
Bài 1:
\(a,2Cu+O_2\underrightarrow{t^o}2CuO\)
b, \(n_{O_2}=\dfrac{1,12}{32}=0,035mol\)
\(n_{Cu}=\dfrac{6,4}{64}=0,1mol\)
\(\dfrac{0,1}{2}>\dfrac{0,035}{1}\) => Cu dư, O2 đủ
\(n_{Cu}\left(dư\right)=0,1-0,07=0,039\left(mol\right)\)
c, \(m_{CuO}=0,07.80=5,6g\)
Bài 2:
\(n_{Al}=\dfrac{13,5}{27}=0,5mol\)
\(n_{O_2}=\dfrac{6,67}{32}=0,21\left(mol\right)\)
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
\(\dfrac{0,5}{4}>\dfrac{0,21}{3}\) => Al dư, O2 đủ
\(n_{Al_2O_3}=\dfrac{2}{3}.0,21=0,14\left(mol\right)\)
\(m_{Al_2O_3}=0,14.102=14,28g\)
Bài 1: Đốt cháy hoàn toàn 10,8 gam nhôm trong bình có chứa 16 gam khí oxi.
a. Viết PTHH xảy ra
b. Sau phản ứng, chất nào dư? Tính khối lượng chất dư.
c. Tính khối lượng sản phẩm thu được.
Bài 2: Điền vào chỗ trống khối lượng, thể tích (ở đktc) của các chất phản ứng và sản phẩm và tỉ khối của chất khí so với hidro có ở những thời điểm khác nhau.
Cho sơ đồ phản ứng như sau: Fe2O3 + CO Fe + CO2
Các thời điểm | Các chất tham gia | Sản phẩm | d khí/H2 | ||
Fe2O3 (gam) | CO (lít) | Fe (gam) | CO2 (lít) | ||
Thời điểm to | 16 g | 8,96 l |
|
|
|
Thời điểm t1 |
|
|
| 1,344 l |
|
Thời điểm t2 |
| 3,584 l |
|
|
|
Thời điểm t3 |
|
| 11,2 g |
|
|
Bài 1 :
a. \(n_{Al}=\dfrac{10,8}{27}=0,4\left(mol\right)\)
\(n_{O_2}=\dfrac{16}{32}=0,5\left(mol\right)\)
b. PTHH : 4Al + 3O2 -to> 2Al2O3
0,4 0,3 0,2
Xét tỉ lệ : \(\dfrac{0,4}{4}< \dfrac{0,5}{3}\) => Al đủ , O2 dư
\(m_{O_2\left(dư\right)}=\left(0,5-0,3\right).32=6,4\left(g\right)\)
c. \(m_{Al_2O_3}=0,2.102=20,4\left(g\right)\)
Bài 2:
| Các thời điểm | Fe2O3 (gam) | CO (lít) | Fe(gam) | CO2(lít) | dkhí/H2 |
| Thời điểm t0 | 16 | 8,96 | 11,2 | 6,72 | 20 |
| Thời điểm t1 | 3,2 | 1,344 | 2,24 | 1,344 | 22 |
| Thời điểm t2 | 128/15 | 3,584 | 448/75 | 3,584 | 22 |
| Thời điểm t3 | 16 | 6,72 | 11,2 | 6,72 | 22 |
Đốt cháy 6,32(g) Photpho trong 6,16(lít) oxi(đktc)
a,Sau phản ứng chất nào còn dư,dư bao nhiu(g)
b,Tính khối lượng sản phẩm
P/S; giúp mik né thanks nhìu...
4P + 5O2 ---> 2P2O5
Số mol P = 6,32/31 = 0,2 mol; số mol O2 = 6,16/22,4 = 0,275 mol.
Theo pt p.ư số mol P = 4/5 số mol O2 = 0,8.0,275 = 0,22 mol > 0,2 mol. Như vậy, O2 còn dư và P đã hết.
O2 còn dư = 0,275 - 0,2.5/4 = 0,025 mol hay 32.0,025 = 0,8 gam.
Sản phẩm P2O5 có số mol = 1/2 số mol P = 0,1 mol. Do đó, có khối lượng = 0,1.142 = 14,2 g.