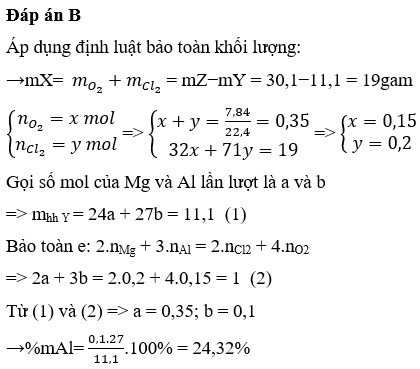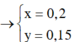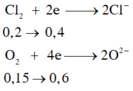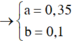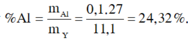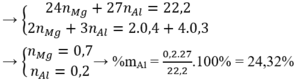Cho 7,84 lít hỗn hợp khí X ( đktc ) gồm Cl2 và O2 phản ứng vừa đủ với 11,1 gam hỗn hợp Y gồm Mg và AI , thu được 30,1 gam hỗn hợp Z. Tính phần trăm khối lượng của Al , Mg trong Y.

Những câu hỏi liên quan
Cho 7,84 lít hỗn hợp khí X (đktc) gồm
C
l
2
,
O
2
phản ứng vừa đủ với 11,1 gam hỗn hợp Y gồm Mg và Al, thu được 30,1 gam hỗn hợp Z. Phần trăm khối lượng của Al trong Y là A. 75,68% B. 24,32% C. 51,35% D. 48,65%
Đọc tiếp
Cho 7,84 lít hỗn hợp khí X (đktc) gồm C l 2 , O 2 phản ứng vừa đủ với 11,1 gam hỗn hợp Y gồm Mg và Al, thu được 30,1 gam hỗn hợp Z. Phần trăm khối lượng của Al trong Y là
A. 75,68%
B. 24,32%
C. 51,35%
D. 48,65%
Cho 7,84 lít hỗn hợp khí X (đktc) gồm
C
l
2
v
à
O
2
phản ứng vừa đủ với 11,1 gam hỗn hợp Y gồm Mg và Al, thu được 30,1 gam hỗn hợp Z. Phần trăm khối lượng của Al trong Y là A. 75,68%. B. 24,32%. C. 51,35%. D. 48,65%.
Đọc tiếp
Cho 7,84 lít hỗn hợp khí X (đktc) gồm C l 2 v à O 2 phản ứng vừa đủ với 11,1 gam hỗn hợp Y gồm Mg và Al, thu được 30,1 gam hỗn hợp Z. Phần trăm khối lượng của Al trong Y là
A. 75,68%.
B. 24,32%.
C. 51,35%.
D. 48,65%.
Chọn đáp án B
n C l 2 = x mol; n O 2 = y mol
⇒ x + y = 0,35 mol (1)
Áp dụng định luật bảo toàn khối lượng: m C l 2 + m O 2 = m Z – m Y = 19g
⇒ 71x + 32y = 19 (2)
Từ (1)(2) => x = 0,2; y = 0,15
Đặt n M g = a mol; n A l = b mol
⇒ 24a + 27b = 11,1g (3)
Bảo toàn e: 2 n M g + 3 n A l = 2 n C l 2 + 4 n O 2
⇒ 2a +3b = 1 (4)
Từ (3)(4) ⇒ a = 0,35; b = 0,1
⇒% m A l = 0 , 1 . 27 11 , 1 . 100 % = 23 , 32 %
Đúng 0
Bình luận (0)
Cho 7,84 lít hỗn hợp khí X (đktc) gồm Cl2 và O2 phản ứng vừa đủ với 11,1 gam hỗn hợp Y gồm Mg và Al, thu được 30,1 gam hỗn hợp Z. Phần trăm khối lượng của Al trong Y là A. 75,68%. B. 24,32%. C. 51,35%. D. 48,65%.
Đọc tiếp
Cho 7,84 lít hỗn hợp khí X (đktc) gồm Cl2 và O2 phản ứng vừa đủ với 11,1 gam hỗn hợp Y gồm Mg và Al, thu được 30,1 gam hỗn hợp Z. Phần trăm khối lượng của Al trong Y là
A. 75,68%.
B. 24,32%.
C. 51,35%.
D. 48,65%.
Cho 7,84 lít hỗn hợp khí X (đktc) gồm Cl2 và O2 phản ứng vừa đủ với 11,1 gam hỗn hợp Y gồm Mg và Al, thu được 30,1 gam hỗn hợp Z. Phần trăm khối lượng của Al trong Y là
A. 75,68%.
B. 24,32%.
C. 51,35%.
D. 48,65%.
Đáp án B.
Áp dụng định luật bảo toàn khối lượng:
![]()
= 30,1 - 11,1 = 19 gam
Đặt
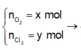
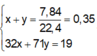
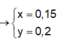
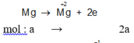
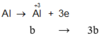
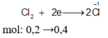
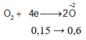
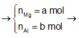
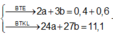
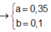
![]()
Đúng 0
Bình luận (0)
Cho 7,84 lít hỗn hợp khí X (đktc) gồm Cl2 và O2 phản ứng vừa đủ với 11,1 gam hỗn hợp Y gồm Mg và Al, thu được 30,1 gam hỗn hợp Z. Phần trăm khối lượng của Al trong Y là A. 75,68%. B. 24,32% C. 51,35% D. 48,65%
Đọc tiếp
Cho 7,84 lít hỗn hợp khí X (đktc) gồm Cl2 và O2 phản ứng vừa đủ với 11,1 gam hỗn hợp Y gồm Mg và Al, thu được 30,1 gam hỗn hợp Z. Phần trăm khối lượng của Al trong Y là
A. 75,68%.
B. 24,32%
C. 51,35%
D. 48,65%
Cho 7,84 lít hỗn hợp khí X (đktc) gồm
C
l
2
v
à
O
2
phản ứng vừa đủ với 11,1 gam hỗn hợp Y gồm Mg và Al, thu được 30,1 gam hỗn hợp Z. Thành phần phần trăm khối lượng của Al trong Y là A. 75,68% B. 24,32% C. 51,35% D. 48,65%
Đọc tiếp
Cho 7,84 lít hỗn hợp khí X (đktc) gồm C l 2 v à O 2 phản ứng vừa đủ với 11,1 gam hỗn hợp Y gồm Mg và Al, thu được 30,1 gam hỗn hợp Z. Thành phần phần trăm khối lượng của Al trong Y là
A. 75,68%
B. 24,32%
C. 51,35%
D. 48,65%
Chọn đáp án B
n X = 7 , 84 22 , 4 = 0,35 (mol)
Bảo toàn khối lượng: m C l 2 + m O 2 = 30,1 – 11,1 = 19 (gam)
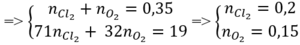

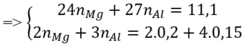
=> n M g = 0 , 35 n A l = 0 , 1 => %mAl = 0 , 1 . 27 11 , 1 .100% = 24,32%
Đúng 0
Bình luận (0)
Cho 8,4 lít hỗn hợp khí X (đktc) gồm
C
l
2
,
O
2
phản ứng vừa đủ với 10,2 gam hỗn hợp Y gồm Mg và Al, thu được 31,95 gam hỗn hợp Z. Phần trăm khối lượng của Mg trong Y là A. 47,06% B. 23,52% C. 52,94% D. 48,65%
Đọc tiếp
Cho 8,4 lít hỗn hợp khí X (đktc) gồm C l 2 , O 2 phản ứng vừa đủ với 10,2 gam hỗn hợp Y gồm Mg và Al, thu được 31,95 gam hỗn hợp Z. Phần trăm khối lượng của Mg trong Y là
A. 47,06%
B. 23,52%
C. 52,94%
D. 48,65%
Cho 15,68 lít hỗn hợp khí X (đktc) gồm
C
l
2
và
O
2
phản ứng vừa đủ với 22,2 gam hỗn hợp Y gồm Mg và Al, thu được 60,2 gam hỗn hợp Z. Phần trăm khối lượng của Al trong Y là A. 75,68% B. 24,32% C. 51,35% D. 48,65%
Đọc tiếp
Cho 15,68 lít hỗn hợp khí X (đktc) gồm C l 2 và O 2 phản ứng vừa đủ với 22,2 gam hỗn hợp Y gồm Mg và Al, thu được 60,2 gam hỗn hợp Z. Phần trăm khối lượng của Al trong Y là
A. 75,68%
B. 24,32%
C. 51,35%
D. 48,65%
Cho 7,84 lít hỗn hợp khí X(đktc) gồm Cl2 và O2 phản ứng vừa đủ với 11,1 gam hỗn hợp Y gồm Mg và Al, thu được 30,1 gam hỗn hợp Z.Tính % khối lượng của mỗi kim loại trong Y
X + Y → Z
Bảo toàn khối lượng → mX + mY = mZ
→ mX + 11,1 = 30,1
→ mX = 19 gam
Giả sử X chứa a mol Cl2 và b mol O2
Ta có hệ pt:
\(\left\{{}\begin{matrix}n_X=a+b=\frac{7,84}{22,4}=0,35\\m_X=71a+32b=19\end{matrix}\right.\rightarrow\left\{{}\begin{matrix}a=0,2\\b=0,15\end{matrix}\right.\)
Giả sử Y chứa u mol Mg và v mol Al
→ mY = 24u + 27v = 11,1 (1)
Quá trình cho - nhận e:
Mg0 → Mg+2 + 2e __________Cl2 + 2e → 2Cl-
Al0 → Al+3 + 3e_____________O2 + 4e → 2O-2
Áp dụng bảo toàn e: 2nMg + 3nAl = 2nCl2 + 4nO2
→ 2u + 3v = 2.0,2 + 4.0,15 (2)
Giải (1) (2) được u = 0,35 và v = 0,1
\(\%m_{Mg}=\frac{0,35.24}{11,1}.100\%=75,7\%\)
\(\%m_{Al}=100\%-75,7\%=24,3\%\)