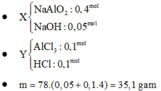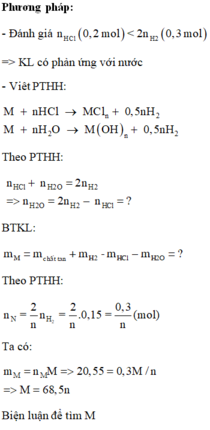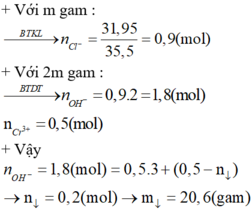Hòa tan hoàn toàn 4,6g kim loại kiềm M vào H2O thì thu được 2,24 lít H2 (đktc) và dung dịch X. Nhỏ từ từ đến hết V lít dung dịch HCl 1M vào dung dịch X thì thu được dung dịch Y chứa 10,96g chất tan. Tính V

Những câu hỏi liên quan
Hoà tan hết a gam Al vào 450 ml dung dịch NaOH 1M thu được 13,44 lít H2 (đktc) và dung dịch X. Hoà tan hết b gam Al vào 400 ml dung dịch HCl 1M thu được 3,36 lít H2 (đktc) và dung dịch Y. Trộn dung dịch X với dung dịch Y đến phản ứng hoàn toàn thì thu được m gam kết tủa. Giá trị m là?
A. 7,8.
B. 3,9.
C. 35,1.
D. 31,2.
Hòa tan kim loại M vào 200 ml dung dịch HCl 1M, sau khi các phản ứng xảy ra hoàn toàn, thu được 3,36 lít khí
H
2
(đktc) và dung dịch X chứa 29,35 gam chất tan. Kim loại M là A. Na B. Ba C. K D. Al
Đọc tiếp
Hòa tan kim loại M vào 200 ml dung dịch HCl 1M, sau khi các phản ứng xảy ra hoàn toàn, thu được 3,36 lít khí H 2 (đktc) và dung dịch X chứa 29,35 gam chất tan. Kim loại M là
A. Na
B. Ba
C. K
D. Al
Hỗn hợp D gồm Fe và một kim loại M có hóa trị II. Hòa tan 9,6g hỗn hợp D vào dung dịch HCL dư thì thu được 4,48 lít khí (đktc). Mặt khác khi hòa tan hoàn toàn 4,6g kim loại M vào dung dịch HCL dư thì thể tích H2 sinh ra chưa đến 5,6 lít (đktc). Xác định kim loại M và tính khối lượng mỗi kim loại có trong hỗn hợp D.
Hỗn hợp D gồm sắt và một kim loại M có hóa trị II. Hòa tan 9,6g hỗn hợp D vào dung dịch HCl dư thì thu được 4,48 lít khí (đktc). Mặt khác khi hòa tan hoàn toàn 4,6g kim loại M vào dung dịch HCl dư thì thế tích H2 sinh ra chưa đến 5,6 lít (đktc). Xác định kim loại M và tính khối lượng mỗi kim loại có trong hỗn hợp.
Gọi $n_{Fe} = a(mol) ; n_M = b(mol) \Rightarrow 56a + Mb = 9,6(1)$
$Fe + 2HCl \to FeCl_2 + H_2$
$M + 2HCl \to MCl_2 + H_2$
$n_{H_2} =a + b = 0,2 \Rightarrow a = 0,2 - b$
Ta có :
$56a + Mb = 9,6$
$⇔ 56(0,2 - b) + Mb = 9,6$
$⇔ Mb - 56b = -1,6$
$⇔ b(56 - M) = 1,6$
$⇔ b = \dfrac{1,6}{56 - M}$
Mà $0 < b < 0,2$
Suy ra : $0 < \dfrac{1,6}{56 - M} < 0,2$
$⇔ M < 48(1)$
$M + 2HCl \to MCl_2 + H_2$
$n_M = n_{H_2} < \dfrac{5,6}{22,4} = 0,25$
$\Rightarrow M_M > \dfrac{4,6}{0,25} = 18,4$
+) Nếu $M = 24(Mg)$
Ta có :
$56a + 24b = 9,6$
$a + b = 0,2$
Suy ra a = 0,15 ; b = 0,05
$m_{Fe} = 0,15.56 = 8,4(gam)$
$m_{Mg} = 0,05.24 = 1,2(gam)$
+) Nếu $M = 40(Ca)$
$56a + 40b = 9,6$
$a + b = 0,2$
Suy ra a = b = 0,1
$m_{Ca} = 0,1.40 = 4(gam)$
$m_{Fe} = 0,1.56 = 5,6(gam)$
Đúng 2
Bình luận (0)
Hỗn hợp D gồm sắt và một kim loại M có hóa trị II. Hòa tan 9,6g hỗn hợp D vào dung dịch HCl dư thì thu được 4,48 lít khí (đktc). Mặt khác khi hòa tan hoàn toàn 4,6g kim loại M vào dung dịch có chứa 18,25g HCl thu được dung dịch E. Cho quỳ tím vào dung dịch E thấy quỳ tím chuyển thành màu đỏ. XĐ kim loại M và tính m mỗi kim loại có trong hỗn hợp
Thí nghiệm 2 : n HCl = 18,25/36,5 = 0,5(mol)
$M + 2HCl \to MCl_2 + H_2$
Vì HCl dư nên : 2n M < 0,5
<=> n M < 0,25
<=> M > 4,6/0,25 = 18,4 (1)
Thí nghiệm 1: n H2 = 4,48/22,4 = 0,2(mol)
n M = a(mol)
$Fe + 2HCl \to FeCl_2 + H_2$
=> n Fe = 0,2 - a(mol)
Ta có : 0 < a < 0,2
M,a + 56.(0,2 - a) = 9,6
<=> M = (56a - 1,6)/a
<=> M < 48 (2)
Từ (1)(2) suy ra 18,4 < M < 48
- Nếu M = 40(Ca)
Ta có : 40a + 56(0,2 -a) = 9,6 => a = 0,1
m Ca = 0,1.40 = 4(gam)
m Fe = 9,6 -4 = 5,6(gam)
- Nếu M = 24(Mg)
Ta có : 24a + 56(0,2 -a) = 9,6 => a = 0,05
m Mg = 0,05.24 = 1,2(gam)
m Fe = 9,6 -1,2 = 8,4(gam)
Đúng 2
Bình luận (0)
Hòa tan hoàn toàn m gam hỗn hợp X gồm Na và K vào dung dịch HCl dư thu được dung dịch Y. Cô cạn dung dịch Y thu được (m+31,95) gam hỗn hợp chất rắn khan. Hòa tan hoàn toàn 2m gam hỗn hợp X vào nước thu được dung dịch Z. Cho từ từ đến hết dung dịch Z vào 0,5 lít dung dịch CrCl3 1M đến phản ứng hoàn toàn thu được kết tủa có khối lượng là A. 54,0 gam. B. 20,6 gam. C. 30,9 gam. D. 51,5 gam.
Đọc tiếp
Hòa tan hoàn toàn m gam hỗn hợp X gồm Na và K vào dung dịch HCl dư thu được dung dịch Y. Cô cạn dung dịch Y thu được (m+31,95) gam hỗn hợp chất rắn khan. Hòa tan hoàn toàn 2m gam hỗn hợp X vào nước thu được dung dịch Z. Cho từ từ đến hết dung dịch Z vào 0,5 lít dung dịch CrCl3 1M đến phản ứng hoàn toàn thu được kết tủa có khối lượng là
A. 54,0 gam.
B. 20,6 gam.
C. 30,9 gam.
D. 51,5 gam.
Đáp án B
DVới m (g) X: nX= nCl= 31,95:35,5= 0,9 mol
Với 2m (g) X:

Đúng 0
Bình luận (0)
Hòa tan hoàn toàn m gam hỗn hợp X gồm Na và K vào dung dịch HCl dư thu được dung dịch Y, cô cạn dung dịch Y thu được (m+31,95) gam hỗn hợp chất rắn khan. Hòa tan hoàn toàn 2m gam hỗn hợp X thu được dung dịch Z. Cho từ từ đến hết dung dịch Z vào 0.5 lít dung dịch CrCl3 1M đến phản ứng hoàn toàn thu được kết tủa có khối lượng là: A.54,0 gam B.20,6 gam C. 30,9 gam D.51,5 gam
Đọc tiếp
Hòa tan hoàn toàn m gam hỗn hợp X gồm Na và K vào dung dịch HCl dư thu được dung dịch Y, cô cạn dung dịch Y thu được (m+31,95) gam hỗn hợp chất rắn khan. Hòa tan hoàn toàn 2m gam hỗn hợp X thu được dung dịch Z. Cho từ từ đến hết dung dịch Z vào 0.5 lít dung dịch CrCl3 1M đến phản ứng hoàn toàn thu được kết tủa có khối lượng là:
A.54,0 gam
B.20,6 gam
C. 30,9 gam
D.51,5 gam
Hòa tan hoàn toàn 29,68 gam hỗn hợp X gồm Cu, Fe và Fe3O4 bằng lượng vừa đủ dung dịch chứa hỗn hợp gồm HCl 1M và H2SO4 0,5M thu được 0,896 lít khí H2 (ở đktc) và dung dịch Y chứa m gam chất tan. Cho từ từ dung dịch BaCl2 vào dung dịch Y đến khi kết tủa cực đại thì dừng lại, cho tiếp tục dung dịch AgNO3 dư vào, sau phản ứng thu được 211,02 gam kết tủa. Mặt khác cho cùng lượng hỗn hợp X trên tác dụng với dung dịch HNO3 đặc, nóng lấy dư thu được 8,736 lít NO2 (ở đktc). Giá trị của m là A. 60,02. B...
Đọc tiếp
Hòa tan hoàn toàn 29,68 gam hỗn hợp X gồm Cu, Fe và Fe3O4 bằng lượng vừa đủ dung dịch chứa hỗn hợp gồm HCl 1M và H2SO4 0,5M thu được 0,896 lít khí H2 (ở đktc) và dung dịch Y chứa m gam chất tan. Cho từ từ dung dịch BaCl2 vào dung dịch Y đến khi kết tủa cực đại thì dừng lại, cho tiếp tục dung dịch AgNO3 dư vào, sau phản ứng thu được 211,02 gam kết tủa. Mặt khác cho cùng lượng hỗn hợp X trên tác dụng với dung dịch HNO3 đặc, nóng lấy dư thu được 8,736 lít NO2 (ở đktc). Giá trị của m là
A. 60,02.
B. 62,22.
C. 55,04.
D. 52,21.
Đáp án A
Nhận thấy, nFe2+(dd Y) = nNO2 – 2nH2 = 0,39 – 2.0,04 = 0,31 mol
Giả sử nHCl = 2a; nH2SO4 = a
nBaSO4 = a, nAgCl = 4a, nAg = nFe2+ = 0,31 => 233a + 143,5.4a + 0,31.108 = 211,02 => a = 0,22
BTNT H => nHCl + 2nH2SO4 = 2nH2 + 2nH2O => nH2O = (0,44 + 2.0,22 – 2.0,04)/2 = 0,4 mol
BTKL: m = mX + mHCl + mH2SO4 – mH2 – mH2O = 29,68 + 0,44.36,5 + 0,22.98 – 0,04.2 – 0,4.18 = 60,02 gam
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 29,68 gam hỗn hợp X gồm Cu, Fe và Fe3O4 bằng lượng vừa đủ dung dịch chứa hỗn hợp gồm HCl 1M và H2SO4 0,5M thu được 0,896 lít khí H2 (ở đktc) và dung dịch Y chứa m gam chất tan. Cho từ từ dung dịch BaCl2 vào dung dịch Y đến khi kết tủa cực đại thì dừng lại, cho tiếp tục dung dịch AgNO3 dư vào, sau phản ứng thu được 211,02 gam kết tủa. Mặt khác cho cùng lượng hỗn hợp X trên tác dụng với dung dịch HNO3 đặc, nóng lấy dư thu được 8,736 lít NO2 (ở đktc). Giá trị của m là A. 60,02. B...
Đọc tiếp
Hòa tan hoàn toàn 29,68 gam hỗn hợp X gồm Cu, Fe và Fe3O4 bằng lượng vừa đủ dung dịch chứa hỗn hợp gồm HCl 1M và H2SO4 0,5M thu được 0,896 lít khí H2 (ở đktc) và dung dịch Y chứa m gam chất tan. Cho từ từ dung dịch BaCl2 vào dung dịch Y đến khi kết tủa cực đại thì dừng lại, cho tiếp tục dung dịch AgNO3 dư vào, sau phản ứng thu được 211,02 gam kết tủa. Mặt khác cho cùng lượng hỗn hợp X trên tác dụng với dung dịch HNO3 đặc, nóng lấy dư thu được 8,736 lít NO2 (ở đktc). Giá trị của m là
A. 60,02.
B. 62,22.
C. 55,04.
D. 52,21.
Đáp án A
Nhận thấy, nFe2+(dd Y) = nNO2 – 2nH2 = 0,39 – 2.0,04 = 0,31 mol
Giả sử nHCl = 2a; nH2SO4 = a
nBaSO4 = a, nAgCl = 4a, nAg = nFe2+ = 0,31 => 233a + 143,5.4a + 0,31.108 = 211,02 => a = 0,22
BTNT H => nHCl + 2nH2SO4 = 2nH2 + 2nH2O => nH2O = (0,44 + 2.0,22 – 2.0,04)/2 = 0,4 mol
BTKL: m = mX + mHCl + mH2SO4 – mH2 – mH2O = 29,68 + 0,44.36,5 + 0,22.98 – 0,04.2 – 0,4.18 = 60,02 gam
Đúng 0
Bình luận (0)