10. Cho 28,4g điphotpho pentaoxit P2O5 vào cốc chứa 90g nước để tạo thành axit photphoric. Tinh khối lượng axit H3PO4 được tạo thành ?

Những câu hỏi liên quan
Cho 28,4g điphotpho penoxit
P
2
O
5
vào cốc có chứa 90g
H
2
O
để tạo thành axit photphoric
H
3
P
O
4
. Khôi lượng axit
H
3
P
O
4
tạo thành là: A. 19.6g B. 58,8g C.39,2g...
Đọc tiếp
Cho 28,4g điphotpho penoxit P 2 O 5 vào cốc có chứa 90g H 2 O để tạo thành axit photphoric H 3 P O 4 . Khôi lượng axit H 3 P O 4 tạo thành là:
A. 19.6g B. 58,8g C.39,2g D.40g
Hãy chọn đáp số đúng.
Phương trình phản ứng:
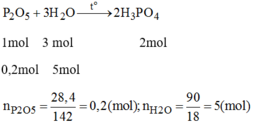
Tỉ lệ mol:
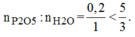
Vậy H 2 O dư và P 2 O 5 hết.
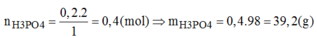
→ Chọn C.
Đúng 0
Bình luận (0)
Cho 5,68 gam P 2 O 5 vào cốc chứa 2,7 gam H 2 O thu được dung dịch axit photphoric H 3 P O 4 . Tính khối lượng axit tạo thành.
1) Khi cho 2g khí hidro tác dụng vói 1,12 lít khí oxi . Khối lượng nước thu được
2) Đốt cháy 3,2g lưu huỳnh trong một bình chứa 1,12l khí O2 (dktc). Thể tích khí SO2 thu được
3) Cho 28,4g diphotpho pentaoxit vào cốc chứa 90g nước để tạo thành axit . Khối lượng axit tạo thành là
4)Đốt cháy hoàn toàn m gam Mg cần dùng vừa đủ 125,776 l không khí (dktc) . Giá trị m
1)
nH2 = 2/2 = 1 (mol)
nO2 = 1.12/22.4 = 0.05 (mol)
2H2 + O2 -to-> 2H2O
0.1_____0.05____0.1
mH2O = 0.1*18 = 1.8 (g)
2)
nS = 3.2/32 = 0.1 (mol)
nO2 = 1.12/22.4 = 0.05 mol
S + O2 -to-> SO2
0.05_0.05____0.05
VSO2 = 0.05*22.4 = 1.12 (l)
Đúng 3
Bình luận (1)
3)
nP2O5 = 28.4/142 = 0.2 (mol)
nH2O = 90/18 = 5 (mol)
P2O5 + 3H2O => 2H3PO4
0.2_____0.6________0.4
mH3PO4 = 0.4*98 = 39.2 (g)
4)
nkk = 125.776/22.4 = 5.615 (mol)
nO2 = 5.615/5 = 1.123 (mol)
Mg + 1/2O2 -to-> MgO
2.246___1.123
mMg = 2.246*24 = 53.904 (g)
Chúc bạn học tốt !!
Đúng 2
Bình luận (1)
Cho 1,42gg P2O5 vào nước để tạo thành dung dịch A tính khối lượng axit photphoric thu được
Ta có: \(n_{P_2O_5}=\dfrac{1,42}{142}=0,01\left(mol\right)\)
PT: \(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
___0,01_____________0,02 (mol)
\(\Rightarrow m_{H_3PO_4}=0,02.98=1,96\left(g\right)\)
Bạn tham khảo nhé!
Đúng 2
Bình luận (0)
\(n_{P_2O_5}=\dfrac{1.42}{142}=0.01\left(mol\right)\)
\(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
\(0.01......................0.02\)
\(m_{H_3PO_4}=0.02\cdot98=1.96\left(g\right)\)
Đúng 1
Bình luận (0)
Đốt cháy 6,2 gam photpho trong bình chứa 6,72 lít khí oxi (đktc) tạo thành điphotpho pentaoxit(P2O5) . Tính khối lượng P2O5 tạo thành
\(n_P=\dfrac{6,2}{31}=0,2mol\)
\(n_{O_2}=\dfrac{6,72}{22,4}=0,3mol\)
\(4P+5O_2\rightarrow\left(t^o\right)2P_2O_5\)
Xét: \(\dfrac{0,2}{4}\) < \(\dfrac{0,3}{5}\) ( mol )
0,2 0,1 ( mol )
\(m_{P_2O_5}=0,1.142=14,2g\)
Đúng 3
Bình luận (0)
`PTHH: 4P + 5O_2` $\xrightarrow[]{t^o}$ `2P_2 O_5`
`n_P = [ 6,2 ] / 31 = 0,2 (mol)`
`n_[O_2] = [ 6,72 ] / [ 22,4 ] = 0,3 (mol)`
Ta có: `[ 0,2 ] / 4 < [ 0,3 ] / 5`
`->P` hết ; `O_2` dư
Theo `PTHH` có: `n_[P_2 O_5] = 1 / 2 n_P = 1 / 2 . 0,2 = 0,1 (mol)`
`-> m_[P_2 O_5] = 0,1 . 142 = 14,2 (g)`
Đúng 2
Bình luận (0)
trong số các tính chất sau của nước [H2O] đâu là tính chất vật lí ? đâu là tính chất hóa học ?a/ nước là chất duy nhất có trên trái đất có thể đồng thời tồn tại ở cả ba trạng thái rắn , lỏng và khíb/ nước cất [nước tinh khiết] sôi ở nhiệt độC trong điều kiện áp suất là 1atmc/ nước có tác dụng với vôi sống [CaO] tạo thành vôi tôi [Ca[OH]2]d/ nước có thể hòa tan được nhiều chấte/ nước tác dụng với điphotpho pentaoxit [P2O5] tạo thành axit photphoric [H3PO4]
Đọc tiếp
trong số các tính chất sau của nước [H2O] đâu là tính chất vật lí ? đâu là tính chất hóa học ?
a/ nước là chất duy nhất có trên trái đất có thể đồng thời tồn tại ở cả ba trạng thái rắn , lỏng và khí
b/ nước cất [nước tinh khiết] sôi ở nhiệt độC trong điều kiện áp suất là 1atm
c/ nước có tác dụng với vôi sống [CaO] tạo thành vôi tôi [Ca[OH]2]
d/ nước có thể hòa tan được nhiều chất
e/ nước tác dụng với điphotpho pentaoxit [P2O5] tạo thành axit photphoric [H3PO4]
Tính chất vật lí: a, b
Tính chất hóa học: c, d, e
Đúng 0
Bình luận (0)
Lập phương trình hóa học cho phản ứng sau:
Điphotpho pentaoxit + nước → axit photphoric H 3 P O 4
đốt cháy 12,4g photpho(P) trong bình chứa khí oxi(O2), sau p.ứng tạo ra 28,4g điphotpho pentaoxit(P2O5). Tính khối lượng khí oxi(O2) đã phản ứng?
Khối lượng khí Oxi đã phản ứng là:
mP2O5 = mP + mO2
28,4 = 12,4 + mO2
mO2 = 28,4 - 12,4
mO2 = 16 g
Đúng 0
Bình luận (0)
cho 28,4(g) điphotpho penta oxit vào cốc chứa 2,7(g) H2O để tạp thành axit photphiric (H3PO4) tính khối lượng H3PO4 tạo thành
PTHH:P2O5+3H2O\(\underrightarrow{t^0}\)2H3PO4
Theo PTHH:142 gam P2O5 cần 54 gam H2O
Vậy:7,1 gam P2O5 cần 2,7 gam H2O
Do đó:P2O5 thừa:28,4-7,1=21,3(gam)
Vì P2O5 thừa nên ta tính SP theo chất thiếu là:H2O
Theo PTHH:54 gam H2O tạo ra 196 gam H3PO4
Vậy:2,7 gam H2O tạo ra 9,8 gam H3PO4
Vậy mH3PO4=9,8 gam
Đúng 0
Bình luận (0)
Ta có: \(n_{P_2O_5}=\frac{28,4}{142}=0,2\left(mol\right)\\ n_{H_2O}=\frac{2,7}{18}=0,15\left(mol\right)\)
PTHH: P2O5 + 3H2O -to-> 2H3PO4
Theo PTHH và đề bài, ta có:
\(\frac{0,2}{1}>\frac{0,15}{3}\)
=> P2O5 dư, H2O hết nên tính theo \(n_{H_2O}\)
Theo PTHH và đề bài, ta có:
\(n_{H_3PO_4}=\frac{2.0,15}{3}=0,1\left(mol\right)\)
Khối lượng H3PO4 tạo thành sau phản ứng:
\(m_{H_3PO_4}=0,1.98=9,8\left(g\right)\)
Đúng 0
Bình luận (0)
























