cho a gam na2co3 10,6% vào b gam dung dịch h2so4 9,8% thu được dung dịch Y có nồng độ h2so4 là 2%. tính tỉ lệ a/b

Những câu hỏi liên quan
Cho 250 gam dung dịch FeCl3 6,5% vào 150 gam dung dịch Na2CO3 10,6% thu được khí A, kết tủa B và dung dịch X. Thêm m gam dung dịch AgNO3 21,25% vào dung dịch X thu được dung dịch Y có nồng độ % cuả NaCl là 1,138%. Giá trị của m xấp xỉ bằng ? A. 176,0gam B. 113,2 gam C. 160 gam D. 140 gam
Đọc tiếp
Cho 250 gam dung dịch FeCl3 6,5% vào 150 gam dung dịch Na2CO3 10,6% thu được khí A, kết tủa B và dung dịch X. Thêm m gam dung dịch AgNO3 21,25% vào dung dịch X thu được dung dịch Y có nồng độ % cuả NaCl là 1,138%. Giá trị của m xấp xỉ bằng ?
A. 176,0gam
B. 113,2 gam
C. 160 gam
D. 140 gam
nFe3+ = 0,1 mol ; nCO32-= 0,15mol
2Fe3+ + 3 CO32- + 3H2O --> 3CO2 + 2Fe(OH)3
Dung dịch X chứa: NaCl (0,3mol)
=> mdd X = 400 - 0,15*44 - 0,1*107 = 382,7 gam
Ag+ + Cl- -> AgCl
x------x-------x
=> mdd Y = 382,7 + 800x - 143,5x = (382,7 + 656,5x) gam
=> 0,01138(382,7 + 656,5x) = 58,5(0,3 - x) => x = 0,2 => m = 160
=> Đáp án C
Đúng 0
Bình luận (0)
Bài 1: Cần thêm bao nhiêu gam SO3 vào dung dịch H2SO4 nồng độ 10% để được 100 gam H2SO4 phải thêm nước vào dung dịch H2SO4 50% để thu được dung dịch H2SO4 20%. Tính tỉ lệ về khối lượng nước và dung dịch axit phải dùng để thu được dung dịch 20%.
Hòa tan 2,7 gam nhôm trong dung dịch axit sunfuric H2SO4 9,8% thu được V (lít) khí và dung dịch A.
a) Tính V (đktc)?
b) Tính khối lượng dung dịch H2SO4 9,8% cần dùng.
c) Tính nồng độ % dung dịch thu được sau phản ứng.
\(n_{Al}=\dfrac{2,7}{27}=0,1mol\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
0,1 0,15 0 ,05 0,15
a)\(V=0,15\cdot22,4=3,36\left(l\right)\)
b)\(m_{H_2SO_4}=0,15\cdot98=14,7\left(g\right)\)
\(\Rightarrow m_{ddHCl}=\dfrac{14,7}{9,8}\cdot100=150\left(g\right)\)
c) \(m_{H_2}=0,15\cdot2=0,3\left(g\right)\)
\(m_{ddsau}=2,7+150-0,3=152,4\left(g\right)\)
\(m_{Al_2\left(SO_4\right)_3}=0,05\cdot342=17,1\left(g\right)\)
\(\Rightarrow C\%=\dfrac{17,1}{152,4}\cdot100=11,22\%\)
Đúng 1
Bình luận (0)
Cho 150g dung dịch H2SO4 9,8% tác dụng vừa đủ với dung dịch Na2CO3 10,6%. Tính khối lượng dung dịch Na2CO3 đã dùng và tính nồng độ % của dung dịch muối sau phản ứng
\(n_{H_2SO_4}=\dfrac{150.9,8\%}{98}=0,15\left(mol\right)\\ H_2SO_4+Na_2CO_3\rightarrow Na_2SO_4+H_2O+CO_2\\ n_{Na_2CO_3}=n_{H_2SO_4}=0,15\left(mol\right)\\ \Rightarrow m_{ddNa_2CO_3}=\dfrac{0,15.106}{10,6\%}=150\left(g\right)\\ n_{CO_2}=n_{H_2SO_4}=0,15\left(mol\right)\\ m_{ddsaupu}=150+150-0,15.44=293,4\left(g\right)\\ n_{Na_2SO_4}=n_{H_2SO_4}=0,15\left(mol\right)\\ C\%_{Na_2SO_4}=\dfrac{0,15.142}{293,4}.100=7,26\%\)
Đúng 4
Bình luận (4)
Cho 150g dung dịch H2SO4 9,8% tác dngj vừa đủ với dung dịch Na2CO3 10,6%. Tính khối lượng dung dịch Na2CO3 đã dùng và tính nồng độ % của dung dịch muối sau phản ứng
\(m_{H_2SO_4}=150.9,8\%=14,7\left(g\right)\\ n_{H_2SO_4}=\dfrac{14,7}{98}=0,3\left(mol\right)\\ PTHH:H_2SO_4+Na_2CO_3\rightarrow Na_2SO_4+CO_2\uparrow+H_2O\\ Mol:0,3\rightarrow0,3\rightarrow0,3\rightarrow0,3\)
\(m_{Na_2CO_3}=0,3.106=31,8\left(g\right)\\ m_{ddNa_2CO_3}=\dfrac{31,8}{10,6\%}=300\left(g\right)\\ m_{Na_2SO_4}=0,3.142=42,6\left(g\right)\\ m_{CO_2}=0,3.44=13,2\left(g\right)\\ m_{dd}=150+300-13,2=436,8\left(g\right)\\ C\%_{Na_2SO_4}=\dfrac{42,6}{436,8}=9,75\%\)
Đúng 4
Bình luận (3)
mH2SO4 =mdd H2SO4.C% : 100% = 400.9,8% :100% = 39,2 (g)
=> nH2SO4 = mH2SO4 : MH2SO4 = 39,2: 98 = 0,4 (mol)
PTHH: H2SO4 + Na2CO3 ---> Na2SO4 + CO2 + H2O
0,4 ---->0,4 -----------> 0,4 -------> 0,4 (mol)
a) Theo PTHH: nNa2CO3 = nH2SO4 = 0,4 (mol)
=> mNa2CO3 = nNa2CO3. MNa2CO3 = 0,4.106 = 42,4 (g)
=> mdd Na2CO3 = mNa2CO3. 100% : C% = 42,4.100% : 10% = 424 (g)
b) Theo PTHH: nCO2 = nH2SO4 = 0,4 (mol)
=> VCO2(đktc) = 0,4.22,4 = 8,96 (lít)
c) Theo PTHH: nNa2SO4 = nH2SO4 = 0,4 (mol)
=> mNa2SO4 = nNa2SO4. MNa2SO4 = 0,4.142 = 56,8 (g)
mdd A = mdd H2SO4 + mdd Na2CO3 = 400 + 424 = 824 (g)
dd A chứa Na2SO4
=> C% Na2SO4 = (mNa2SO4 : mddA).100% = (56,8 : 824).100% = 6,89%
Lấy vừa đủ a gam dung dịch H2SO4 40% để hòa tan b gam hỗn hợp Na, Na2O, NaOH, Na2CO3 thu được 8,96 lít khí(đktc) hỗn hợp khí có tỉ khối đối với h2 Bằng 16,75 và dung dịch Y có nồng độ 51,449%. Cô cạn dung dịch Y thu được 170,4 g muối trung hòa khan. Xác định giá trị a ,b
Cho m gam dung dịch Na2CO3 21,2% vào 120 gam dung dịch B gồm XCl2 và YCl3 (tỉ lệ mol 1:2, X và Y là hai kim loại nhóm A) thu được dung dịch D, khí E và 12 gam kết tủa. Tiếp tục cho 200 gam dung dịch AgNO3 40,5% vào dung dịch D thì thu được dung dịch G chỉ chứa muối nitrat, trong đó nồng độ của NaNO3 là 9,884%. (Dung dịch D chỉ chứa một chất tan duy nhất). Nồng độ % của XCl2 là A. 3,958%. B. 7,917%. C. 11,125%. D. 5,563%.
Đọc tiếp
Cho m gam dung dịch Na2CO3 21,2% vào 120 gam dung dịch B gồm XCl2 và YCl3 (tỉ lệ mol 1:2, X và Y là hai kim loại nhóm A) thu được dung dịch D, khí E và 12 gam kết tủa. Tiếp tục cho 200 gam dung dịch AgNO3 40,5% vào dung dịch D thì thu được dung dịch G chỉ chứa muối nitrat, trong đó nồng độ của NaNO3 là 9,884%. (Dung dịch D chỉ chứa một chất tan duy nhất). Nồng độ % của XCl2 là
A. 3,958%.
B. 7,917%.
C. 11,125%.
D. 5,563%.
Chọn đáp án A
Phản ứng tạo khí E và Y là kim loại nhóm A.
⇒ Y là Al. D chỉ chứa 1 chất tan ⇒ D chứa NaCl.
+ Từ tỷ lệ mol 1:2 ⇒ Đặt nXCl2 = a và nAlCl3 = 2a
⇒ Trong dung dịch D có ∑nCl– = 8a và nNa2CO3 = 4a mol.
+ G chỉ chứa muối nitrat ⇒ NaCl (D) pứ hết, tạo nAgCl↓ = 8a mol và nNaNO3 = 8a mol.
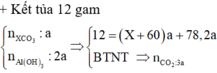
+ BTKL: mdd G = mdd Na2CO3 + mdd B + mdd AgNO3 – mkết tủa – mCO2.
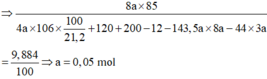
⇒ X = 24 ⇒ X là Mg ⇒ C% MgCl2 = 0 , 05 . 95 . 100 120 = 3,985%
⇒ Chọn A
Đúng 0
Bình luận (0)
Cho m gam dung dịch Na2CO3 21,2% vào 120 gam dung dịch B gồm XCl2 và YCl3 (tỉ lệ mol 1:2, X và Y là hai kim loại nhóm A) thu được dung dịch D, khí E và 12 gam kết tủa. Tiếp tục cho 200 gam dung dịch AgNO3 40,5% vào dung dịch D thì thu được dung dịch G chỉ chứa muối nitrat, trong đó nồng độ của NaNO3 là 9,884%. (Dung dịch D chỉ chứa một chất tan duy nhất). Nồng độ % của XCl2 là A. 3,958%. B. 7,917%. C. 11,125%. D. 5,563%.
Đọc tiếp
Cho m gam dung dịch Na2CO3 21,2% vào 120 gam dung dịch B gồm XCl2 và YCl3 (tỉ lệ mol 1:2, X và Y là hai kim loại nhóm A) thu được dung dịch D, khí E và 12 gam kết tủa. Tiếp tục cho 200 gam dung dịch AgNO3 40,5% vào dung dịch D thì thu được dung dịch G chỉ chứa muối nitrat, trong đó nồng độ của NaNO3 là 9,884%. (Dung dịch D chỉ chứa một chất tan duy nhất). Nồng độ % của XCl2 là
A. 3,958%.
B. 7,917%.
C. 11,125%.
D. 5,563%.
Chọn đáp án A
Phản ứng tạo khí E và Y là kim loại nhóm A.
⇒ Y là Al. D chỉ chứa 1 chất tan ⇒ D chứa NaCl.
+ Từ tỷ lệ mol 1:2 ⇒ Đặt nXCl2 = a và nAlCl3 = 2a
⇒ Trong dung dịch D có ∑nCl– = 8a và nNa2CO3 = 4a mol.
+ G chỉ chứa muối nitrat ⇒ NaCl (D) pứ hết, tạo nAgCl↓ = 8a mol và nNaNO3 = 8a mol.
+ Kết tủa 12 gam 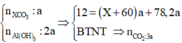
+ BTKL: mdd G = mdd Na2CO3 + mdd B + mdd AgNO3 – mkết tủa – mCO2.
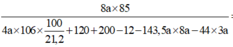
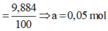
⇒ X = 24 ⇒ X là Mg ⇒ C% MgCl2 = 0 , 05 . 95 . 100 120 = 3,985%
Đúng 0
Bình luận (0)
Nhiệt phân hoàn toàn m gam Fe(OH)2 thu được 7,2 gam một chất rắn màu đen. a. Tính m. b. Hòa tan m gam Fe(OH)2 trên bằng 300g dung dịch H2SO4 9,8% thu được dung dịch X. Tính nồng độ phần trăm của các chất trong dung dịch X.















