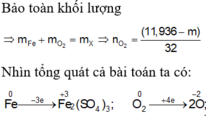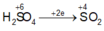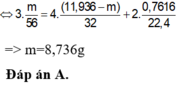Đốt cháy 11,2 gam Fe ngoài không khí một thời gian thu được 15,04 gam hỗn hợp X gồm Fe FeO Fe304 Fe2O3 cho toàn bộ X tác dụng với H2SO4 đặc nóng thu được V lít (điều kiện tiêu chuẩn )khí SO2 (sản phẩm khử duy nhất) .Tính V

Những câu hỏi liên quan
Nung nóng 12,6 gam Fe ngoài không khí sau một thời gian thu được m gam hỗn hợp X gồm Fe, FeO, Fe2O3 và Fe3O4 . Hỗn hợp này phản ứng hết với dung dịch H2SO4 đặc nóng (dư), thu được 4,2 lít khí SO2 (sản phẩm khử duy nhất, ở đktc). Tính m? A. 15g B. 9g C.18g D. 24g
Đọc tiếp
Nung nóng 12,6 gam Fe ngoài không khí sau một thời gian thu được m gam hỗn hợp X gồm Fe, FeO, Fe2O3 và Fe3O4 . Hỗn hợp này phản ứng hết với dung dịch H2SO4 đặc nóng (dư), thu được 4,2 lít khí SO2 (sản phẩm khử duy nhất, ở đktc). Tính m?
A. 15g
B. 9g
C.18g
D. 24g
Đáp án A
Ta có, nFe = 0,225 mol và nSO2 = 0,1875 mol
Quy hỗn hỗn hợp X về 2 nguyên tố Fe và O
Quá trình nhường: Fe0 → Fe+3 + 3e
Quá trình nhận e: O0 + 2e → O-2
S+6 + 2e → S+4
Áp dụng định luật bảo toàn electron ta có:
0,675 = 2x + 0,375 → x = 0,15
Mặt khác ta có: nên: m = 12,6 + 0,15.16 = 15 (gam).
Đúng 1
Bình luận (0)
Để m gam bột sắt ngoài không khí, sau một thời gian thu được 11,936 gam hỗn hợp X gồm Fe, FeO, Fe2O3, Fe3O4. Cho hỗn hợp X phản ứng hết với dung dịch H2SO4 đặc, nóng thu được 0,7616 lít khí SO2(đktc). Gía trị của m là: A. 8,736 gam B. 14,448 gam C. 5,712 gam D. 7,224 gam
Đọc tiếp
Để m gam bột sắt ngoài không khí, sau một thời gian thu được 11,936 gam hỗn hợp X gồm Fe, FeO, Fe2O3, Fe3O4. Cho hỗn hợp X phản ứng hết với dung dịch H2SO4 đặc, nóng thu được 0,7616 lít khí SO2(đktc). Gía trị của m là:
A. 8,736 gam
B. 14,448 gam
C. 5,712 gam
D. 7,224 gam
Nung 12,6 gam Fe trong không khí sau một thời gian thu được m gam hỗn hợp chất rắn X gồm Fe, FeO, Fe3O4, Fe2O3. Hòa tan m gam X trong dung dịch H2SO4 đặc nóng dư thu được 1,68 lít (đktc) khí SO2 (sản phẩm khử duy nhất). Tính m
Ta có: \(n_{Fe}=\dfrac{12,6}{56}=0,225\left(mol\right)\)
Coi X gồm Fe và O.
BTNT Fe: nFe (X) = 0,225 (mol)
Ta có: \(n_{SO_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\)
BT e, có: 3nFe = 2nO + 2nSO2 ⇒ nO = 0,2625 (mol)
⇒ m = mFe + mO = 0,225.56 + 0,2625.16 = 16,8 (g)
Đúng 2
Bình luận (0)
Để a gam phoi bào sắt ngoài không khí một thời gian thu được b gam hỗn hợp X gồm Fe, FeO, Fe3O4 và Fe2O3. Hòa tan hết hỗn hợp X trong dung dịch H2SO4 đặc, nóng, dư thu được 5,6 lít khí SO2 (đktc) và dung dịch Y. Cho dung dịch Y phản ứng với dung dịch NaOH dư thu được kết tủa Z. Đem nung Z trong không khí đến khối lượng không đổi thu được 24 gam chất rắn. Tìm a và b. Help me, please quick!Các bạn làm ơn help me nhanh nhé
Đọc tiếp
Để a gam phoi bào sắt ngoài không khí một thời gian thu được b gam hỗn hợp X gồm Fe, FeO, Fe3O4 và Fe2O3. Hòa tan hết hỗn hợp X trong dung dịch H2SO4 đặc, nóng, dư thu được 5,6 lít khí SO2 (đktc) và dung dịch Y. Cho dung dịch Y phản ứng với dung dịch NaOH dư thu được kết tủa Z. Đem nung Z trong không khí đến khối lượng không đổi thu được 24 gam chất rắn. Tìm a và b.
Help me, please quick!
Các bạn làm ơn help me nhanh nhé
Đem 11,2 gam Fe để ngoài không khí, sau một thời gian thu được một hỗn hợp X gồm Fe và các oxit. Hòa tan hoàn toàn hỗn hợp đó trong dung dịch H2SO4 đặc, nóng dư, thu được dung dịch Y và 3,36 lít khí SO2 (đktc). Số mol H2SO4 đã tham gia phản ứng là A. 0,4 B. 0,3 C. 0,5 D. 0,45
Đọc tiếp
Đem 11,2 gam Fe để ngoài không khí, sau một thời gian thu được một hỗn hợp X gồm Fe và các oxit. Hòa tan hoàn toàn hỗn hợp đó trong dung dịch H2SO4 đặc, nóng dư, thu được dung dịch Y và 3,36 lít khí SO2 (đktc). Số mol H2SO4 đã tham gia phản ứng là
A. 0,4
B. 0,3
C. 0,5
D. 0,45
Hòa tan m gam hỗn hợp X gồm Fe2O3, CuO, MgO, FeO, Fe3O4 trong H2SO4 đặc nóng, dư, thu được 3,36 lít SO2 (đktc, sản phẩm khử duy nhất). Mặt khác, nung m gam X với khí CO dư, thu được chất rắn Y và hỗn hợp khí Z. Cho Z vào dung dịch Ca(OH)2 dư, sau khi phản ứng xảy ra hoàn toàn thu được 35 gam kết tủa. Hòa tan Y trong dung dịch HNO3 đặc nóng, due thu được V lít khí NO2 (sản phẩm khử duy nhất ở điều kiện tiêu chuẩn). Giá trị của V là: A.33,6. B. 11,2. C. 44,8. D. 22,4.
Đọc tiếp
Hòa tan m gam hỗn hợp X gồm Fe2O3, CuO, MgO, FeO, Fe3O4 trong H2SO4 đặc nóng, dư, thu được 3,36 lít SO2 (đktc, sản phẩm khử duy nhất). Mặt khác, nung m gam X với khí CO dư, thu được chất rắn Y và hỗn hợp khí Z. Cho Z vào dung dịch Ca(OH)2 dư, sau khi phản ứng xảy ra hoàn toàn thu được 35 gam kết tủa. Hòa tan Y trong dung dịch HNO3 đặc nóng, due thu được V lít khí NO2 (sản phẩm khử duy nhất ở điều kiện tiêu chuẩn). Giá trị của V là:
A.33,6.
B. 11,2.
C. 44,8.
D. 22,4.
Nung hỗn hợp X gồm 13,44 gam Fe và 7,02 gam Al trong không khí một thời gian, thu được 28,46 gam chất rắn Y. Cho Y tác dụng với dd H2SO4 đặc, nóng dư thu được V lít khí SO2 (đktc). Tìm V
Để m gam bột sắt ngoài không khí, sau một thời gian sẽ chuyển thành hỗn hợp A có khối lượng 37,6 gam gồm Fe, FeO, Fe2O3, Fe3O4. Cho hỗn hợp A phản ứng hết với H2SO4 đặc, nóng, dư thu được 3,36 lít khí SO2 (đktc). Giá trị của m là A. 56,0. B. 28,0 C. 11,2. D. 8,4.
Đọc tiếp
Để m gam bột sắt ngoài không khí, sau một thời gian sẽ chuyển thành hỗn hợp A có khối lượng 37,6 gam gồm Fe, FeO, Fe2O3, Fe3O4. Cho hỗn hợp A phản ứng hết với H2SO4 đặc, nóng, dư thu được 3,36 lít khí SO2 (đktc). Giá trị của m là
A. 56,0.
B. 28,0
C. 11,2.
D. 8,4.
Đáp án B
Xét giai đoạn A tác dụng với H2SO4 đặc, nóng, dư:
Số mol SO2 thu được là: n SO 2 = 0 , 15 mol
Qui đổi hỗn hợp A thành Fe : a mol; O : b mol
![]()
Sơ đồ phản ứng :
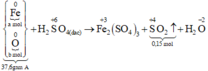
Các quá trình nhường, nhận electron:
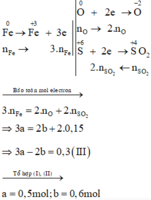
Xét giai đoạn để m gam Fe ngoài không khí:
Sơ đồ phản ứng :

Đúng 1
Bình luận (0)
Cho 12,8 gam hỗn hợp X gồm Fe và FeO vào dung dịch H2SO4 loãng dư thấy có 2,24 lít H2 thoát ra.a-Tính số mol Fe và FeO.Biết khí đo ở đktc .(1đ)b-Cho toàn bộ lượng hỗn hợp X trên tác dụng với H2SO4 đặc nóng dư thu được V lít khí SO2 ở đktc .Tính V
\(n_{Fe}=a\left(mol\right),n_{FeO}=b\left(mol\right)\)
\(m_X=56a+72b=12.8\left(g\right)\)
\(n_{H_2}=n_{Fe}=\dfrac{2.24}{22.4}=0.1\left(mol\right)\)
\(\Rightarrow a=0.1\)
\(b=\dfrac{12.8-56\cdot0.1}{72}=0.1\left(mol\right)\)
\(BTe:\)
\(3n_{Fe}+n_{FeO}=2n_{SO_2}\)
\(\Rightarrow n_{SO_2}=\dfrac{3\cdot0.1+0.1}{2}=0.2\left(mol\right)\)
\(V_{SO_2}=0.2\cdot22.4=4.48\left(l\right)\)
\(\)
Đúng 0
Bình luận (0)