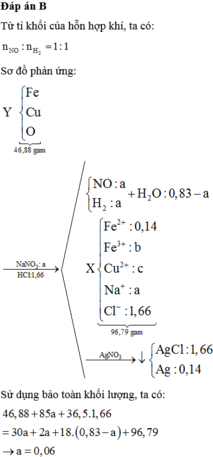
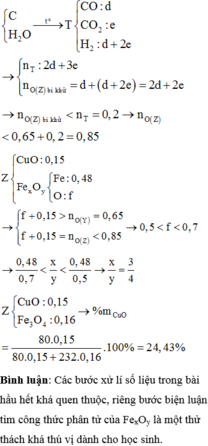Hòa tan 7,5 gam hỗn hợp X gồm 2 kim loại Al và Mg trong 425 ml dung dịch HCl 2M, sau khi phản ứng hoàn toàn thu được dung dịch Y và khí Z
a/ CM dung dịch Y vẫn có axit dư
b/ Dẫn khí sinh ra qua ống nghiệm đựng m(g) CuO nung nóng thì thấy khối lượng chất rắn thu được là (m-5,6) gam. Tính khối lượng mỗi kim loại trong hỗn hợp đầu!!!