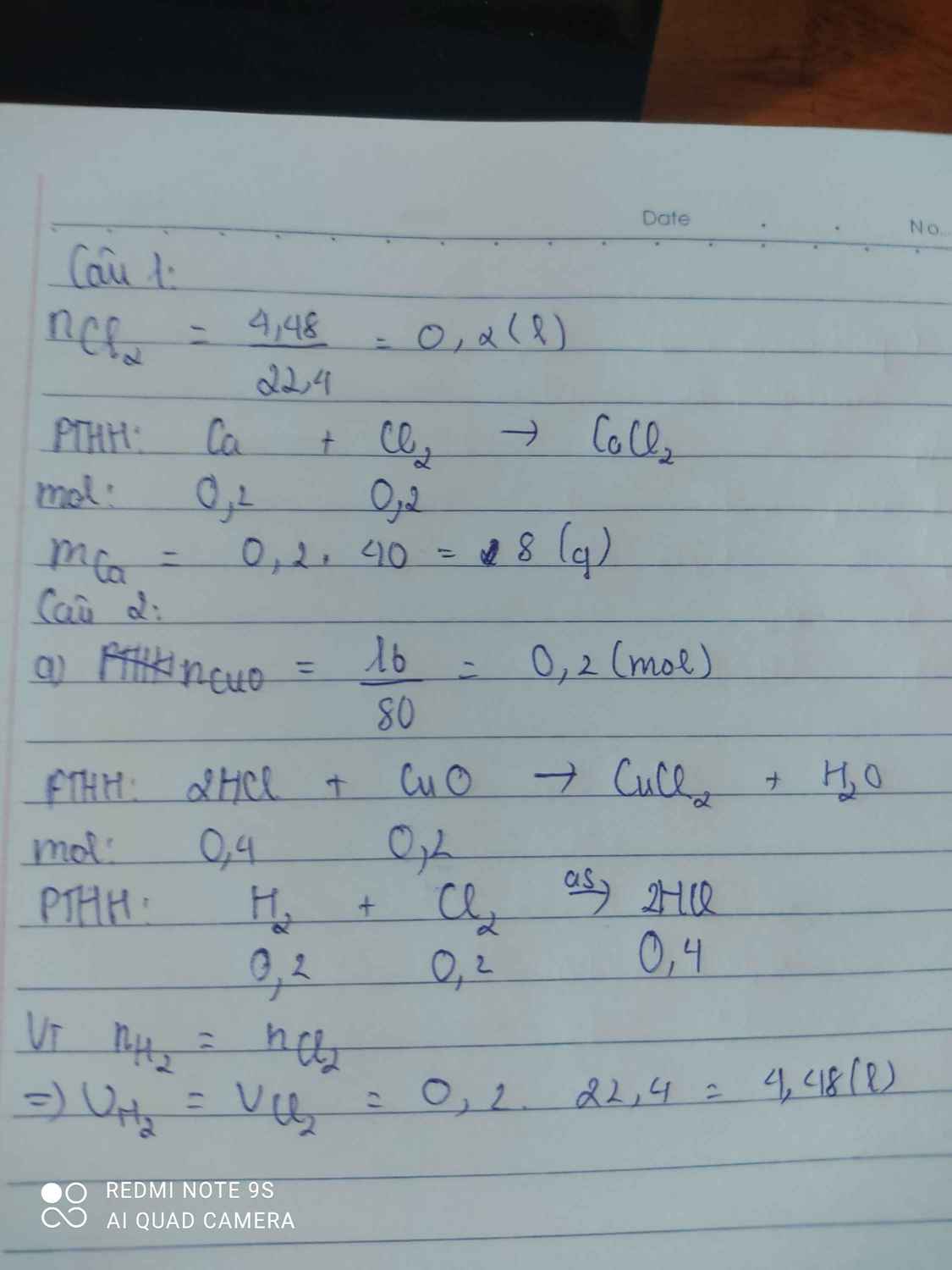Câu 5: Cho 5,6 gam canxi oxit tác dụng vừa đủ với axit clohidric 1M. Xác định m(g) khối lượng muối khan thu được?(Biết Cl = 35, 5 Ca = 40 ; O=16;H=1)

Những câu hỏi liên quan
Câu 5: Cho 5,6 gam canxi oxit tác dụng vừa đủ với axit clohidric 1M. Xác định m(g) khối lượng muối khan thu được?(Biết Cl = 35, 5 Ca = 40 ; O=16;H=1)
\(n_{CaO}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
PTHH: CaO + 2HCl → CaCl2 + H2O
Mol: 0,1 0,1
\(\Rightarrow m_{CaCl_2}=0,1.111=11,1\left(g\right)\)
Đúng 1
Bình luận (0)
Cho 11,2 gam canxi oxit tác dụng vừa đủ với dung dịch axit clohiđric 2M. a. Tính khối lượng muối khan thu được, đọc tên muối. b. Thể tích dung dịch axit clohiđric (ml) đã dùng.
\(a.CaO+2HCl\rightarrow CaCl_2+H_2O\\ n_{CaO}=\dfrac{11,2}{56}=0,2\left(mol\right)\\ n_{CaCl_2}=n_{CaO}=0,2\left(mol\right)\\ m_{CaCl_2}=111.0,2=22,2\left(g\right)\)
Tên muối: Canxi clorua
\(b.n_{HCl}=0,2.2=0,4\left(mol\right)\\ V_{ddHCl}=\dfrac{0,4}{2}=0,2\left(l\right)=200\left(ml\right)\)
Đúng 1
Bình luận (0)
1) Cho m gam đồng II oxit tác dụng vừa đủ với 98 gam dung dịch axit sunfuric 40% a. Tìm giá trị m = ? b. Tính C% của muối thu được? 2) Cho 16 gam sắt III oxit tác dụng với 146 gam dung dịch axit clohiđric 20%. Thu được dung dịch A a. Xác định khối lượng chất tan có trong A? b. Tính C% của chất trong A? Giúp mình với hôm nay mình nộp bài r ạ 😭
Câu 6. Cho 0,27 gam kim loại A (hóa trị III) tác dụng vừa đủ với dd axit clohiđric (H và Cl), sau phản ứng thu được m gam muối clorua (A và Cl) và 336(ml) khí hiđro (đktc).a. Xác định tên kim loại A.b. Tính khối lượng muối clorua thu được.Câu 7. Đốt cháy 3,1 gam photpho trong bình chứa 4,48 lít khí oxi (đktc), sau phản ứng thu được a gam chất rắn.a. Chất nào còn dư sau phản ứng và dư bao nhiêu gam?b. Tính khối lượng của hợp chất thu được.c. Nếu hòa tan hết a gam hợp chất trên vào nước thì sau ph...
Đọc tiếp
Câu 6. Cho 0,27 gam kim loại A (hóa trị III) tác dụng vừa đủ với dd axit clohiđric (H và Cl), sau phản ứng thu được m gam muối clorua (A và Cl) và 336(ml) khí hiđro (đktc).
a. Xác định tên kim loại A.
b. Tính khối lượng muối clorua thu được.
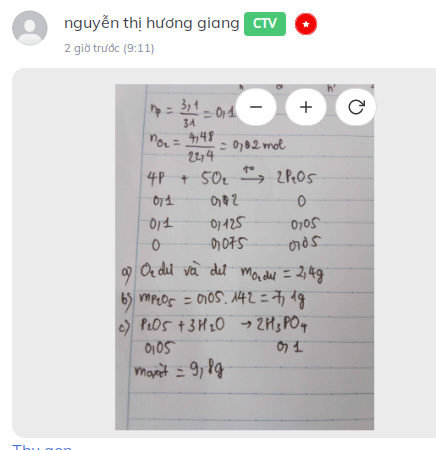
Câu 7. Đốt cháy 3,1 gam photpho trong bình chứa 4,48 lít khí oxi (đktc), sau phản ứng thu được a gam chất rắn.
a. Chất nào còn dư sau phản ứng và dư bao nhiêu gam?
b. Tính khối lượng của hợp chất thu được.
c. Nếu hòa tan hết a gam hợp chất trên vào nước thì sau phản ứng thu được sản phẩm là axit photphoric (H và PO4). Tính khối lượng axit có trong dung dịch thu được sau phản ứng?
Câu 8. Cho một lượng Mg tác dụng hết với dung dịch có chứa 19,6 gam H2SO4.
a. Tính khối lượng Mg đã phản ứng.
b. Tính khối lượng muối thu được sau phản ứng.
c. Dẫn toàn bộ lượng khí H2 thu được qua ống sứ chứa 24gam CuO nung nóng cho tới khi phản ứng xảy ra hoàn toàn. Tính khối lượng Cu thu được sau phản ứng.
Câu 6. Cho 0,27 gam kim loại A (hóa trị III) tác dụng vừa đủ với dd axit clohiđric (H và Cl), sau phản ứng thu được m gam muối clorua (A và Cl) và 336(ml) khí hiđro (đktc).a. Xác định tên kim loại A.b. Tính khối lượng muối clorua thu được.Câu 7. Đốt cháy 3,1 gam photpho trong bình chứa 4,48 lít khí oxi (đktc), sau phản ứng thu được a gam chất rắn.a. Chất nào còn dư sau phản ứng và dư bao nhiêu gam?b. Tính khối lượng của hợp chất thu được.c. Nếu hòa tan hết a gam hợp chất trên vào nước thì sau ph...
Đọc tiếp
Câu 6. Cho 0,27 gam kim loại A (hóa trị III) tác dụng vừa đủ với dd axit clohiđric (H và Cl), sau phản ứng thu được m gam muối clorua (A và Cl) và 336(ml) khí hiđro (đktc).
a. Xác định tên kim loại A.
b. Tính khối lượng muối clorua thu được.
Câu 7. Đốt cháy 3,1 gam photpho trong bình chứa 4,48 lít khí oxi (đktc), sau phản ứng thu được a gam chất rắn.
a. Chất nào còn dư sau phản ứng và dư bao nhiêu gam?
b. Tính khối lượng của hợp chất thu được.
c. Nếu hòa tan hết a gam hợp chất trên vào nước thì sau phản ứng thu được sản phẩm là axit photphoric (H và PO4). Tính khối lượng axit có trong dung dịch thu được sau phản ứng?
nH2 = 0,336/22,4 = 0,015 (mol)
PTHH: 2A + 6HCl -> 2ACl3 + 3H2
nACl3 = nA = 0,015 : 3 . 2 = 0,01 (mol)
M(A) = 0,27/0,01 = 27 (g/mol)
=> A là Al
mAlCl3 = 0,01 . 133,5 = 1,335 (g)
Đúng 2
Bình luận (1)
Câu 6.
\(n_{H_2}=\dfrac{0,336}{22,4}=0,015mol\)
\(2A+6HCl\rightarrow2ACl_3+3H_2\)
0,01 0,015
\(\overline{M_A}=\dfrac{0,27}{0,01}=27đvC\)
\(\Rightarrow A\) là Al nhôm.
\(m_{AlCl_3}=0,01\cdot133,5=1,335g\)
Đúng 2
Bình luận (0)
Cho 65 gam kẽm tác dụng vừa đủ với 73 gam axit clohidric (HCl) thu được muối kẽm clorua và 2 gam khí hidro.
a. Dấu hiệu xảy ra pư hh là gì?
b. Xác định CTHH của muối và viết PTHH
c. Tính khối lượng muối kẽm clorua thu được bằng cách nhanh nhất
a, Dấu hiệu xảy ra phản ứng là có khí thoát ra nè
b) CTHH của muối: ZnCl2
PTHH: Zn +2 HCl -> ZnCl2 + H2
c) Áp dụng ĐLBTKL, ta có:
\(m_{Zn}+m_{HCl}=m_{ZnCl_2}+m_{H_2}\\ \Leftrightarrow65+73=m_{ZnCl_2}+2\\ \Leftrightarrow m_{ZnCl_2}=136\left(g\right)\)
Đúng 1
Bình luận (2)
Lấy bột magie oxit tác dụng hoàn toàn và vừa đủ với 73 gam dd axit clohidric 4%. Tìm khối lượng magie oxit đã dùng. Tìm nồng độ phần trăm dd muối thu được
\(n_{HCl}=\dfrac{73.4\%}{36,5}=0,08\left(mol\right)\\ MgO+2HCl\rightarrow MgCl_2+H_2O\\ 0,04........0,08.......0,04......0,04\left(mol\right)\\ m_{MgO}=0,04.40=1,6\left(g\right)\\ C\%_{ddMgCl_2}=\dfrac{0,04.95}{1,6+73-0,04.2}.100\approx5,099\%\)
Đúng 1
Bình luận (0)
\(m_{ct}=\dfrac{4.73}{100}=2,92\left(g\right)\)
\(n_{HCl}=\dfrac{2,92}{36,5}=0,08\left(mol\right)\)
Pt : \(MgO+2HCl\rightarrow MgCl_2+H_2O|\)
1 2 1 1
0,04 0,08 0,04
\(n_{MgO}=\dfrac{0,08.1}{2}=0,04\left(mol\right)\)
⇒ \(m_{MgO}=0,04.40=1,6\left(g\right)\)
\(n_{MgCl2}=\dfrac{0,08.1}{2}=0,04\left(mol\right)\)
⇒ \(m_{MgCl2}=0,04.95=3,8\left(g\right)\)
\(m_{ddspu}=1,6+73=74,6\left(g\right)\)
\(C_{MgCl2}=\dfrac{3,8.100}{74,6}=5,09\)0/0
Chúc bạn học tốt
Đúng 0
Bình luận (0)
Câu 1:Cho m (g) Ca tác dụng hết với 4,48 lit Cl 2 (đktc).Tính m.Câu 2:Hỗn hợp khí Cl 2 và H 2 có chiếu sáng phản ứng hoàn toàn thì thu được khíhidroclorua,hòa tan khí vào nước được axit clohidric,lượng axit này tác dụng vừa đủ với16 g CuO.a- Viết ptpu ; b-Tính thể tích Cl 2 ,H 2 (biết pu vừa đủ)Câu 3:Cho 11 g hỗn hợp Fe,Al tác dụng hết với 20,16 lit khí Cl 2 (đktc),sau phản ứng thuđược hh muối clorua.a- viết pthu ; b-Tính thành phần trăm khối lượng từng kim loại tronghh.(Cho:Cu64;Fe56;Al27;Cl35,...
Đọc tiếp
Câu 1:Cho m (g) Ca tác dụng hết với 4,48 lit Cl 2 (đktc).Tính m.
Câu 2:Hỗn hợp khí Cl 2 và H 2 có chiếu sáng phản ứng hoàn toàn thì thu được khí
hidroclorua,hòa tan khí vào nước được axit clohidric,lượng axit này tác dụng vừa đủ với
16 g CuO.
a- Viết ptpu ; b-Tính thể tích Cl 2 ,H 2 (biết pu vừa đủ)
Câu 3:Cho 11 g hỗn hợp Fe,Al tác dụng hết với 20,16 lit khí Cl 2 (đktc),sau phản ứng thu
được hh muối clorua.
a- viết pthu ; b-Tính thành phần trăm khối lượng từng kim loại trong
hh.(Cho:Cu=64;Fe=56;Al=27;Cl=35,5;O=16;H=1)
Câu 1:
\(Ca+Cl_2\rightarrow CaCl_2\)
\(n_{Cl_2}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
=>nCa=0,4(mol)
\(m_{Ca}=0.4\cdot12=4.8\left(g\right)\)
Đúng 1
Bình luận (0)
1) Cho 15,3 gam nhôm oxit tác dụng vừa đủ với m gam dung dịch axit clohiđric 20% a. Tìm giá trị m =? b. Tính khối lượng dung dịch thu được sau phản ứng? c. Tính C% của muối thu được? 2) Cho m gam nhôm oxit tác dụng vừa đủ với 54,75 gam dung dịch axit clohiđric 20% a. Tìm giá trị m=? b. Tính C% của muối thu được?
1)
a, \(n_{Al}=\dfrac{15,3}{102}=0,15\left(mol\right)\)
PTHH: Al2O3 + 6HCl → 2AlCl3 + 3H2O
Mol: 0,15 0,9 0,3
\(m_{ddHCl}=\dfrac{0,9.36,5.100}{20}=164,25\left(g\right)\)
b, mdd sau pứ = 15,3 + 164,25 = 179,55 (g)
c, \(C\%_{ddAlCl_3}=\dfrac{0,3.133,5.100\%}{179,55}=22,31\%\)
Đúng 2
Bình luận (0)
2)
a, \(m_{HCl}=54,75.20\%=10,95\left(g\right)\Rightarrow n_{HCl}=\dfrac{10,95}{36,5}=0,3\left(mol\right)\)
PTHH: Al2O3 + 6HCl → 2AlCl3 + 3H2O
Mol: 0,05 0,3 0,1
\(m_{Al_2O_3}=0,05.102=5,1\left(g\right)\)
b, mdd sau pứ = 5,1 + 54,75 = 59,85 (g)
\(C\%_{ddAlCl_3}=\dfrac{0,1.133,5.100\%}{59,85}=22,31\%\)
Đúng 1
Bình luận (0)