Dạng 4: Kim loại tác dụng với dung dịch muối
Nội dung lý thuyết
KIM LOẠI TÁC DỤNG VỚI MUỐI
1.Cơ chế phản ứng
- Đối với dạng toán cho kim loại tác dụng với muối thì cơ chế phản ứng sẽ tuân theo quy tắc α
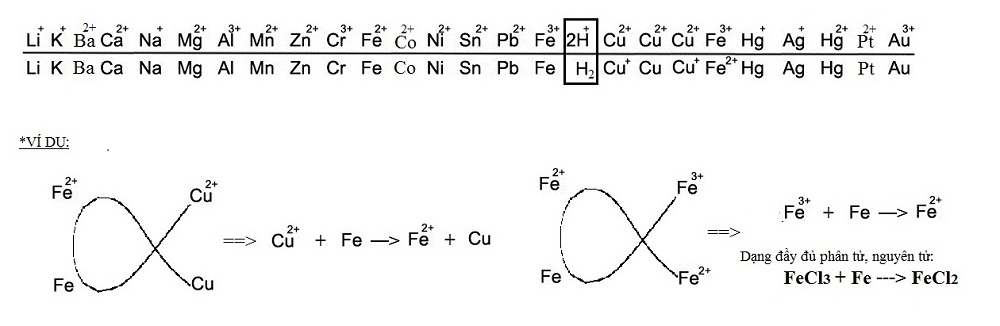
2. Phương pháp giải
-Bảo toàn electron.
3. Ví dụ
Bài 1: Cho a gam Mg vào 100 ml dung dịch Al2(SO4)3 1M và CuSO4 3M thu được 21,9 gam hỗn hợp chất rắn gồm hai kim loại. Giá trị của a là
A. 10,8 B. 14,4 C. 13,4 D. 21,6
Hướng dẫn giải
Thứ tự phản ứng sẽ là Mg phản ứng với Cu2+ trước rồi mới đến Al3+.
Hai kim loại thu được là Cu và Al. => Mg phản ứng hết.
Mg → Mg2+ + 2e Cu2+ + 2e → Cu
x 2x 0,3 0,6 0,3
Al3+ + 3e → Al
3y y
\(\Rightarrow m_{Mg}=10,8gam\)
Bài 2: Nhúng một thanh magie vào dung dịch có chứa 0,8 mol Fe(NO3)3 và 0,05 mol Cu(NO3)2. Sau một thời gian, lấy thanh kim loại ra, rửa sạch, cân lại thấy khối lượng tăng 11,6 gam so với thanh kim loại ban đầu. Khối lượng magie đã phản ứng là :
A. 6,96 gam B. 20,88 gam C. 25,2 gam D. 24 gam
Hướng dẫn giải:
TH1: Khối lượng thanh Mg tăng lên là do Cu bám vào
\(m_{Cu}=0,05\cdot64=3,2gam< 11,6gam\)
=> Giả thiết không đúng. Vậy khối lượng thanh Mg tăng lên là do 2 kim loại Cu và Fe bám vào.
TH2: Khối lượng thanh Mg tăng lên là do Cu và Fe bám vào
Mg → Mg2+ + 2e Fe3+ + 1e → Fe2+
x 2x 0,8 0,8
Cu2+ + 2e → Cu
0,05 0,1 0,05
Fe2+ + 2e → Fe
y 2y y
Áp dụng định luật báo toàn e ta có : \(2x=0,8+0,1+2y\left(1\right)\)
Dựa vào đề ra thì \(\Delta m=m_{KLbám}-m_{KLtan}\Leftrightarrow11,6=0,05\cdot64+56y-24x\left(2\right)\)
Giải hệ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=1,05\\y=0,6\end{matrix}\right.\)
\(\Rightarrow m_{Mg}=25,2gam\)