Bài 4: Phân tử, đơn chất, hợp chất
Nội dung lý thuyết
I. Phân tử
1. Khái niệm phân tử
- Phân tử là hạt đại diện cho chất, gồm một số nguyên tử gắn kết với nhau bằng liên kết hoá học và thể hiện đầy đủ tính chất hoá học của chất.
- Các phân tử của một chất giống nhau về thành phần và hình dạng.
Ví dụ 1: Nước được hợp thành từ các phân tử có hai nguyên tử H, một nguyên tử O và có dạng gấp khúc.
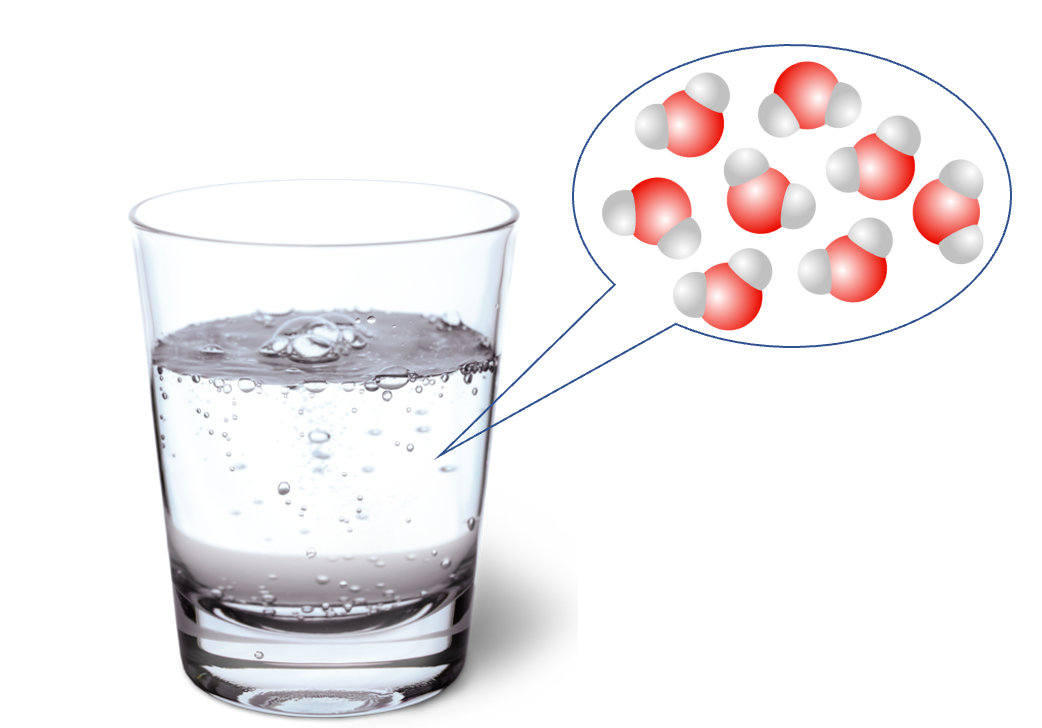
Hình 1: Mô hình phân tử của nước
- Mỗi phân tử gồm nhiều nguyên tử liên kết với nhau.
- Trong một phân tử, các nguyên tử có thể giống hoặc khác nhau.
Ví dụ 2:
- Phân tử đường ăn gồm 12 nguyên tử C, 22 nguyên tử H và 11 nguyên tử O liên kết với nhau.
- Phân tử iodine gồm hai nguyên tử I liên kết với nhau.
@2455615@
2. Khối lượng phân tử
- Khối lượng phân tử (kí hiệu là M) bằng tổng khối lượng các nguyên tử có trong phân tử. Đơn vị của khối lượng phân tử là amu.
Ví dụ 3: Cách xác định khối lượng phân tử nước.
Bước 1: Xác định số lượng nguyên tử của mỗi nguyên tố. Phân tử nước gồm 2 nguyên tử H và 1 nguyên tử O.
Bước 2: Có khối lượng của từng nguyên tử (H: 1 amu, O: 16 amu), khối lượng phân tử nước là:
M nước = 2 x 1 + 1 x 16 = 18 (amu)
@2455703@
II. Đơn chất
- Đơn chất là những chất được tạo thành từ một nguyên tố hoá học.
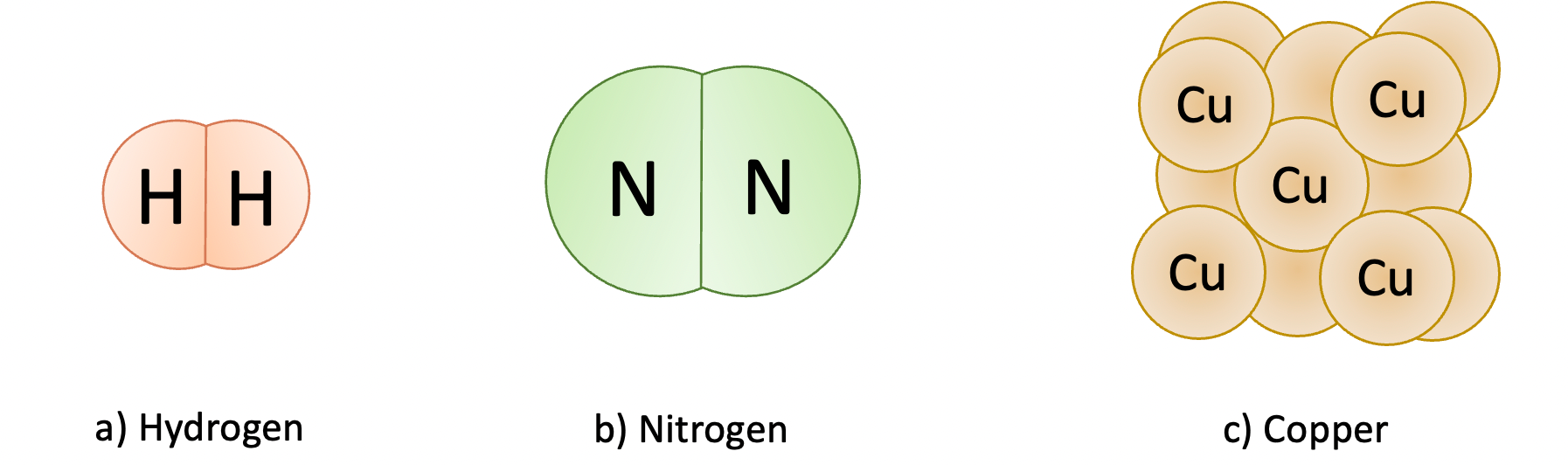
Hình 2: Mô hình phân tử một số đơn chất
Ví dụ 4: Mỗi chất trong hình 2 đều do một nguyên tố hoá học tạo nên, do đó khí hydrogen, khí nitrogen và kim loại copper đều là các đơn chất.
- Ở điều kiện thường, trừ mercury ở thể lỏng, các đơn chất kim loại khác đều ở thể rắn.
- Tên của các đơn chất thường trùng với tên của các nguyên tố tạo nên chất đó, trừ một số nguyên tố tạo ra được hai hay nhiều đơn chất.
Ví dụ 5:
- Than và kim cương là các đơn chất được tạo ra từ cùng một nguyên tố carbon.
- Khí oxygen và khí ozone là các đơn chất được tạo ra từ cùng một nguyên tố oxygen.
III. Hợp chất
- Hợp chất là những chất do hai hoặc nhiều nguyên tố hoá học tạo thành.
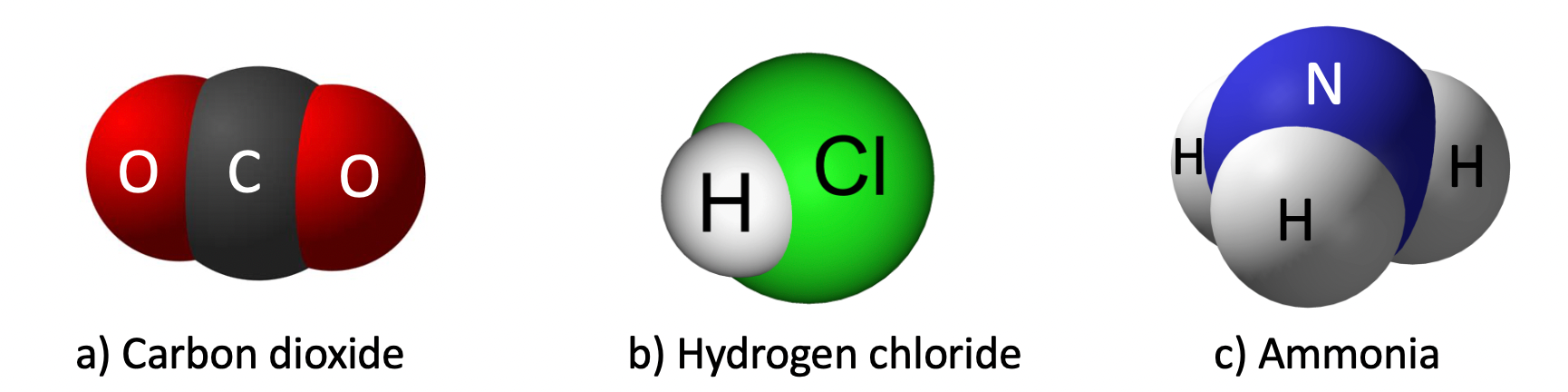
Hình 3: Mô hình phân tử một số hợp chất
Ví dụ 6:
- Khí carbon dioxide được tạo thành từ nguyên tử của hai nguyên tố carbon và oxygen.
- Khí hydrogen chloride được tạo thành từ nguyên tử của hai nguyên tố hydrogen và chlorine.
- Khí ammonia được tạo thành từ nguyên tử của hai nguyên tố nitrogen và hydrogen.
@2455789@
1. Phân tử là hạt đại diện cho chất, gồm một số nguyên tử liên kết với nhau bằng liên kết hóa học và thể hiện đầy đủ tính chất hóa học của chất.
2. Khối lượng phân tử là tổng khối lượng của các nguyên tử có trong phân tử. Đơn vị của khối lượng phân tử là amu.
3. Đơn chất là chất được tạo thành từ một nguyên tố hóa học.
4. Hợp chất là chất được tạo thành từ hai hay nhiều nguyên tố hóa học.