Bài 31. Phương trình trạng thái của khí lí tưởng
Nội dung lý thuyết
Các phiên bản khácPHƯƠNG TRÌNH TRẠNG THÁI CỦA KHÍ LÍ TƯỞNG
1. Khí thực và khí lí tưởng
- Các khí thực (chất khí tồn tại trong thực tế) chỉ tuân theo gần đúng các định luật về chất khí
- Khi ở nhiệt độ thấp, sự khác biệt giữa khí thực và khí lí tưởng không quá lớn nên ta có thể áp dụng các định luật về chất khí
2. Phương trình trạng thái của khí lí tưởng
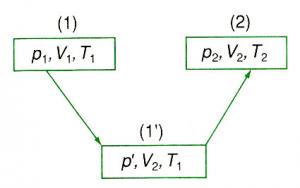
Ta chuyển lượng khí từ trạng thái 1 (\(p_1,T_1,V_1\)) sang trạng thái 2 (\(p_2,V_2,T_2\)) qua trạng thái trung gian 1' (\(p',V_2,T_1\)).
Dễ dàng thấy được, với một khối khí lí tưởng nhất định ta có
\(\dfrac{{{P}_{1}}{{V}_{1}}}{{{T}_{1}}}=\dfrac{{{P}_{2}}{{V}_{2}}}{{{T}_{2}}}\)
Trong đó: \(p_1,V_1,T_1\) là áp suất, thể tích và nhiệt độ tuyệt đối của một lượng khí ở trạng thái 1
\(p_2,V_2,T_2\) là áp suất, thể tích và nhiệt độ tuyệt đối của một lượng khí ở trạng thái 2
3. Quá trình đẳng áp
Quá trình đẳng áp là quá trình biến đổi trạng thái của một khối khí khi áp suất không đổi.
Trong quá trình đẳng áp của một lượng khí nhất định, thể tích tỉ lệ thuận với nhiệt độ tuyệt đối
\(\dfrac{{{V}_{1}}}{{{T}_{1}}}=\dfrac{{{V}_{2}}}{{{T}_{2}}}\)
Trong đó: \(V_1,T_1\) là thể tích và nhiệt độ tuyệt đối của một lượng khí ở trạng thái 1
\(V_2,T_2\) là thể tích và nhiệt độ tuyệt đối của một lượng khí ở trạng thái 2
4. Đường đẳng áp
Đường đẳng áp là đường biểu diễn sự biến thiên của thể tích theo nhiệt độ khi áp suất không đổi.
Trong hệ tọa độ (\(V,T\)) đường đẳng tích là đường thẳng mà nếu kéo dài sẽ đi qua gốc tọa độ.

- Với những áp suất khác nhau của cùng một khối lượng khí, ta có những đường đẳng áp khác nhau
- Các đường đẳng áp ở trên ứng với thể tích nhỏ hơn các đường đẳng tích ở dưới
Danh sách các phiên bản khác của bài học này. Xem hướng dẫn