Bài 2: Nguyên tố hoá học
Nội dung lý thuyết
I. Nguyên tố hoá học là gì?
Khái niệm: Nguyên tố hoá học là tập hợp những nguyên tử có cùng số proton trong hạt nhân.
Ví dụ 1: Các nguyên tử khác nhau nhưng có cùng 6 proton trong nguyên tử nên thuộc cùng nguyên tố carbon.
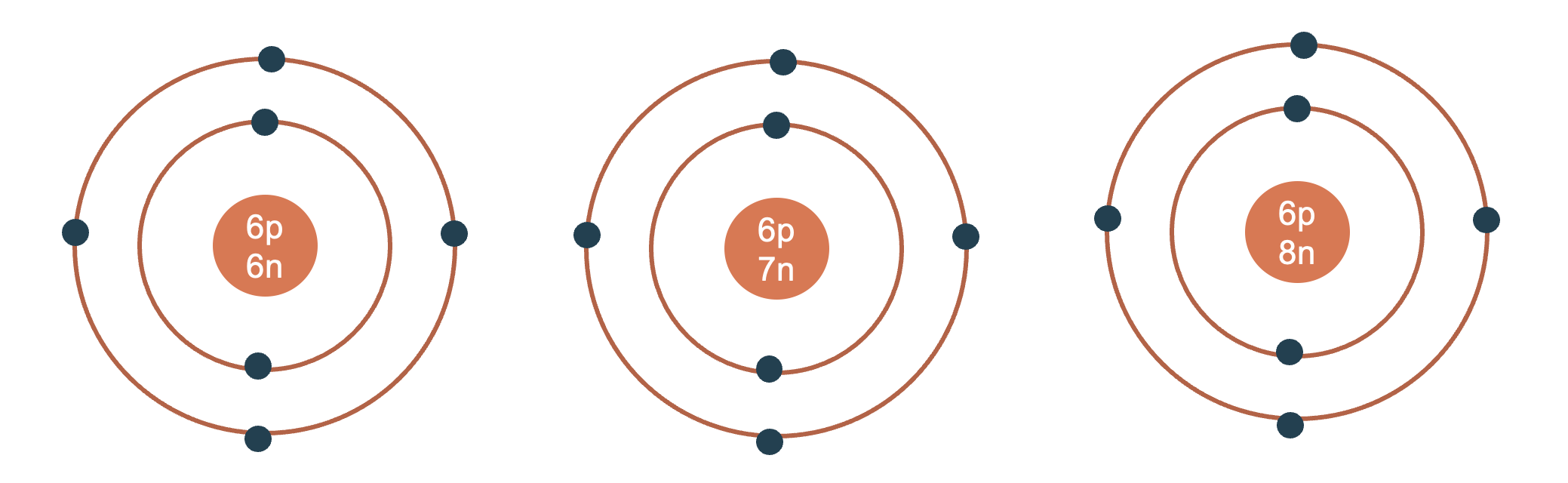
Mô hình cấu tạo các nguyên tử khác nhau thuộc cùng nguyên tố carbon
- Một nguyên tố hoá học được đặc trưng bởi số proton có trong nguyên tử.
- Các nguyên tử của cùng nguyên tố hoá học đều có tính chất hoá học giống nhau.
- Phân loại:
- Nguyên tố hoá học có trong tự nhiên (khoảng 90 nguyên tố).
- Nguyên tố hoá học nhân tạo (khoảng 28 nguyên tố).
@2449097@
II. Tên nguyên tố hoá học
- Mỗi nguyên tố hoá học đều có tên gọi riêng.
- Việc đặt tên nguyên tố dựa vào nhiều cách khác nhau (liên quan đến tính chất, ứng dụng của nguyên tố, theo tên của các nhà khoa học, theo tên của các địa danh,...).
Ví dụ 2:
- Tên nguyên tố carbon (thành phần chính của than) bắt nguồn từ tiếng Latinh, "carbo" nghĩa là than.
- Tên nguyên tố mendelevi bắt nguồn từ tên nhà hoá học người Nga D.I Mendeleev.
- Tên nguyên tố poloni bắt nguồn từ đất nước Ba Lan (Poland).
III. Kí hiệu hoá học
- Mỗi nguyên tố hoá học được biểu diễn bằng một kí hiệu riêng, được gọi là kí hiệu hoá học của nguyên tố.
- Kí hiệu hoá học của nguyên tố được biểu diễn bằng một hoặc hai chữ cái trong tên nguyên tố.
- Chữ cái đầu tiên trong kí hiệu được viết ở dạng in hoa, chữ cái thứ hai (nếu có) ở dạng chữ thường.
Ví dụ 3:
- Kí hiệu hoá học của nguyên tố hydrogen là H.
- Kí hiệu hoá học của nguyên tố carbon là C.
- Kí hiệu hoá học của nguyên tố chlorine là Cl.
@2449149@
- Trong một số trường hợp, kí hiệu hoá học của nguyên tố không tương ứng với tên theo IUPAC.
Ví dụ 4: Kí hiệu nguyên tố potassium là K, bắt nguồn từ tên La-tinh "kalium".
Bảng 2.1: Tên gọi và kí hiệu của một số nguyên tố hoá học
| STT | Tên nguyên tố hoá học | Kí hiệu | STT | Tên nguyên tố hoá học | Kí hiệu |
| 1 | Hydrogen | H | 11 | Sodium | Na |
| 2 | Helium | He | 12 | Magnesium | Mg |
| 3 | Lithium | Li | 13 | Aluminium | Al |
| 4 | Beryllium | Be | 14 | Silicon | Si |
| 5 | Boron | B | 15 | Phosphorus | P |
| 6 | Carbon | C | 16 | Sulfur | S |
| 7 | Nitrogen | N | 17 | Chlorine | Cl |
| 8 | Oxygen | O | 18 | Argon | Ar |
| 9 | Fluorine | F | 19 | Potassium | K |
| 10 | Neon | Ne | 20 | Calcium | Ca |
@2449210@
1. Nguyên tố hoá học là tập hợp những nguyên tử có cùng số proton trong hạt nhân.
2. Mỗi nguyên tố hoá học có tên gọi và kí hiệu hoá học riêng.
3. Kí hiệu hoá học của nguyên tố được biểu diễn bằng một hoặc hai chữ cái trong tên nguyên tố; trong đó, chữ cái đầu tiên được viết ở dạng chữ in hoa, chữ cái thứ (nếu có) được viết ở dạng chữ thường.