CO2−3+2H+→CO2+H2O
HCO−3+H+→CO2+H2O
Gọi số mol CO2−3CO32− và HCO−3HCO3−
cho em hỏi hóa 10 đã học dạng này chưa ạ nếu có thì ở chương mấy ạ
Sục CO2 vào dung dịch chứa 1 mol NaOH và 1 mol Ca(OH)2. Vẽ đồ thị biểu diễn quá trình
kết tủa theo số mol CO2
thầy vẽ giúp em đồ thị với ạ. Tiện thể thầy cho em hỏi nếu cho như vậy thì CO2 phản ứng với
dung dịch nào trước ạ. em cảm ơn thầy!
HD:
Trong 1 dung dịch các chất tồn tại ở dạng ion chứ không tồn tại ở phân tử, nên đối với dung dịch trên ta có các ion: Na+(1 mol), Ca2+(1 mol) và OH-(3 mol). Vì vậy CO2 phản ứng chỉ với ion OH- chứ không phản ứng với Na+ hay Ca2+. Do đó không phân biệt CO2 phản ứng với NaOH trước hay Ca(OH)2 trước nhé.
Đối với dạng bài toán CO2 phản ứng với dd có chứa ion OH-, các em phải chú ý đến tỉ lệ giữa số mol OH- và CO2 (k = nOH-/nCO2). Có các trường hợp sau:
TH1: Nếu k \(\le\) 1 tức là 3/a \(\le\) 1, suy ra a \(\ge\) 3 (ở đây a là số mol CO2), thì chỉ xảy ra phản ứng sau:
CO2 + OH- \(\rightarrow\) HCO3- (1)
Trường hợp này không thu được kết tủa, nên số mol kết tủa thu được = 0.
TH2: Nếu 1 < k < 2, tức là 1 < 3/a < 2, hay 1,5 < a < 3, thì xảy ra đồng thời 2 phản ứng sau:
CO2 + 2OH- \(\rightarrow\) CO32- + H2O
CO2 + OH- \(\rightarrow\) HCO3-
Trong trường hợp này thì số mol CO32- thu được = 3 - a mol (vì tổng số mol CO2 = a và tổng số mol OH- = 3 mol). Do đó, có phản ứng sau:
Ca2+ +CO32- \(\rightarrow\) CaCO3 (kết tủa trắng)
1 mol 3-a mol
Nếu 1 < 3-a, tức là 1,5 < a < 2 thì số mol kết tủa thu được = 1 mol. Nếu 3-a \(\le\) 1, tức là 2 \(\le\) a < 3, thì số mol kết tủa thu được = 3-a mol.
TH3: Nếu k \(\ge\) 2 tức là 3/a \(\ge\) 2, hay a \(\le\) 1,5 thì chỉ xảy ra phản ứng sau:
CO2 + 2OH- \(\rightarrow\) CO32-
Trường hợp này số mol OH- dư so với CO2 nên số mol CO32- thu được = số mol CO2 = a mol.
Ca2+ + CO32- \(\rightarrow\) CaCO3
1 mol a mol
Nếu 1 < a \(\le\) 1,5 thì số mol kết tủa thu được = 1 mol. Nếu a \(\le\) 1 thì số mol kết tủa thu được = a mol.
Như vậy qua các trường hợp trên có thể tóm tắt lại như sau:
Đặt y = số mol kết tủa. Ta có:
1) nếu 0 < a \(\le\) 1 thì y = a
2) nếu 1 < a < 2 thì y = 1
3) nếu 2 \(\le\) a < 3 thì y = 3-a
4) nếu a \(\ge\) thì y = 0.
Từ đó có thể vẽ đồ thị biểu diễn sự phụ thuộc của x vào a như sau:
Ai làm giúp em bài này với ạ: Một hỗn hợp X gồm 2 khí CO và CO2 mà nếu cứ có 13 nguyên tử thì có 8 nguyên tử O. Tính tỉ lệ mol của CO và CO2 trong hỗn hợp X
trong 13 nguyên tử :
gọi số nguyên tử C trong CO là a=> số nt O trong CO=a
gọi số nguyên tử C trong CO2 là b=> số nt O trong CO2=2b
số nguyên tử C trong 13 nt= 13-8=5
ta có hệ pt
a+b=5
a+2b=8
=> a=2;b=3
trong 13 nt có 2 phân tử CO và 3 phân tử CO2
=> n CO:nCO2=2:3
Mn giúp em bài này với ạ : Viết phương trình hóa học cho mỗi chuyển đổi hóa học sau và ghi rõ điều kiện phản ứng ( nếu có) : Na -> Na2O -> NaOH -> Na2CO3 -> CO2 -> CaCO3 -> CaCl2
$4Na + O_2 \xrightarrow{t^o} 2Na_2O$
$Na_2O + H_2O \to 2NaOH$
$2NaOH + CO_2 \to Na_2CO_3 + H_2O$
$Na_2CO_3 + 2HCl\to 2NaCl + CO_2 + H_2O$
$CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O$
$CaCO_3 + 2HCl \to CaCl_2 + CO_2 + H_2O$
4Na+O2→2Na2O
Na2O+H2O→2NaOH
NaOH+CO2→Na2CO3
Na2CO3+CaCl2−to→CaO+CO2+2NaCl
CaO+2HCl→CaCl2+H2O
4Na+O2to→2Na2O4Na+O2→to2Na2O
Na2O+H2O→2NaOHNa2O+H2O→2NaOH
2NaOH+CO2→Na2CO3+H2O2NaOH+CO2→Na2CO3+H2O
Na2CO3+2HCl→2NaCl+CO2+H2ONa2CO3+2HCl→2NaCl+CO2+H2O
CO2+Ca(OH)2→CaCO3+H2OCO2+Ca(OH)2→CaCO3+H2O
CaCO3+2HCl→CaCl2+CO2+H2O
Số mol phân tử CO2 có chứa 9.1023 phân tử CO2?
Giúp mình câu này ạ
\(n_{CO_2}=\dfrac{9\cdot10^{23}}{6\cdot10^{23}}=1.5\left(mol\right)\)
Cho phương trình hóa học: C a C O 3 → t o C O 2 + H 2 O
Để thu được 2,24 lít C O 2 ở đktc thì số mol C a C O 3 cần dùng là
A. 1 mol
B. 0,1 mol
C. 0,001 mol
D. 2 mol
Đáp án B
n C O 2 = 2 , 24 / 22 , 4 = 0 , 1 m o l C a C O 3 → t o C O 2 + H 2 O 0 , 1 ← 0 , 1 ( m o l )
Xét phản ứng:
CO (k) + H2O (h) D CO2 (k) + H2 (k).
Biết rằng nếu thực hiện phản ứng giữa 1 mol CO và 1 mol H2O thì ở trạng thái cân bằng có 2/3 mol CO2 được sinh ra. Hằng số cân bằng của phản ứng là:
A. 2
B. 4
C. 6
D. 8
Xét phản ứng:
CO (k) + H2O (h) D CO2 (k) + H2 (k).
Biết rằng nếu thực hiện phản ứng giữa 1 mol CO và 1 mol H2O thì ở trạng thái cân bằng có 2/3 mol CO2 được sinh ra. Hằng số cân bằng của phản ứng là:
A.2
B.4
C. 6
D.8
Đáp án B
CO(k) + H2O(h) D CO2(k) + H2(k)
Ban đầu 1 1 0 0(mol)
Phản ứng 2/3 2/3 ß 2/3 2/3(mol)
Cân bằng 1/3 1/3 2/3 2/3(mol)
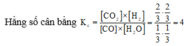
Có phương trình hóa học sau:
CaCO3 → CaO + CO2.
a) Cần dùng bao nhiêu mol CaCO3 để điều chế được 11,2g CaO?
b) Muốn điều chế được 7g CaO cần dùng bao nhiêu gam CaCO3?
c) Nếu có 3,5 mol CaCO3 tham gia phản ứng sẽ sinh ra bao nhiêu lít CO2 (đktc).
d) Nếu thu được 13,44 lít khí CO2 ở đktc thì có bao nhiêu gam chất rắn tham gia và tạo thành sau phản ứng.
Phương trình hóa học CaCO3 → CaO + CO2.
a) nCaO = 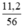 = 0,2 mol.
= 0,2 mol.
Theo PTHH thì nCaCO3 = nCaO = 0,2 (mol)
b) nCaO = 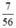 = 0,125 (mol)
= 0,125 (mol)
Theo PTHH thì nCaCO3 = nCaO = 0,125 (mol)
mCaCO3 = M.n = 100.0,125 = 12,5 (g)
c) Theo PTHH thì nCO2 = nCaCO3 = 3,5 (mol)
VCO2 = 22,4.n = 22,4.3,5 = 78,4 (lít)
d) nCO2 = 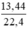 = 0,6 (mol)
= 0,6 (mol)
Theo PTHH nCaO = nCaCO3 = nCO2 = 0,6 (mol)
mCaCO3 = n.M = 0,6.100 = 60 (g)
mCaO = n.M = 0,6.56 = 33,6 (g)
Cho em hỏi dạng bài sục khí CO2 vào dung dịch gồm NaOH và KOH thì thứ tự phản ứng như thế nào ạ
NaOH,KOH phản ứng đồng thời với $CO_2$
Thứ tự phản ứng :
$2NaOH + CO_2 \to Na_2CO_3 + H_2O$
$2KOH + CO_2 \to K_2CO_3 + H_2O$
$Na_2CO_3 + CO_2 + H_2O \to 2NaHCO_3$
$K_2CO_3 + CO_2 + H_2O \to 2KHCO_3$