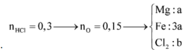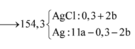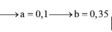Bài 1. Một hỗn hợp khí X gồm 0,1 mol Cl2; 0,2 mol CO2 và 0,3 mol O2. (a) Tính số mol và thể tích của hỗn hợp khí X (ở đkc). (b) Tính khối lượng của hỗn hợp khí X.

Những câu hỏi liên quan
Một hỗn hợp khí X gồm 0,2 mol N2; 0,15 mol Cl2 và 0,1 mol O2.
(a) Tính số mol và thể tích của hỗn hợp khí X (ở đktc).
(b) Tính khối lượng của hỗn hợp khí X.
(c) Tính khối lượng mol trung bình của hỗn hợp khí X.
(d) Hỗn hợp khí X nặng hay nhẹ hơn không khí bao nhiêu lần?
\(a.\)
\(n_{hh}=0.2+0.15+0.1=0.45\left(mol\right)\)
\(V_X=0.45\cdot22.4=10.08\left(l\right)\)
\(b.\)
\(m_X=0.2\cdot28+0.15\cdot71+0.1\cdot32=19.45\left(g\right)\)
\(c.\)
\(\overline{M}_X=\dfrac{19.45}{0.45}=43.22\left(g\text{/}mol\right)\)
\(d.\)
\(d_{X\text{/}kk}=\dfrac{43.22}{29}=1.4\)
Nặng hơn không khí 1.4 lần
Đúng 1
Bình luận (0)
Một hỗn hợp khí X gồm 0,2 mol N2; 0,15 mol Cl2 và 0,1 mol O2.
(a) Tính số mol và thể tích của hỗn hợp khí X (ở đktc).
(b) Tính khối lượng của hỗn hợp khí X.
(c) Tính khối lượng mol trung bình của hỗn hợp khí X.
(d) Hỗn hợp khí X nặng hay nhẹ hơn không khí bao nhiêu lần?
Một hỗn hợp khí X gồm 0,2 mol N2; 0,15 mol Cl2 và 0,1 mol O2.
(a) Tính số mol và thể tích của hỗn hợp khí X (ở đktc).
(b) Tính khối lượng của hỗn hợp khí X.
(c) Tính khối lượng mol trung bình của hỗn hợp khí X.
(d) Hỗn hợp khí X nặng hay nhẹ hơn không khí bao nhiêu lần?
Để đốt cháy hoàn toàn hỗn hợp X gồm 0,1 mol Al và 0,05 mol Mg cần dùng một lượng hỗn hợp khí Y gồm 0,05 mol O2 và x mol khí Cl2. Sau khi phản ứng xong, thu được m gam chất Z. Giá trị của m là
BT e: \(3n_{Al}+2n_{Mg}=4n_{O_2}+2n_{Cl_2}\)
\(\Rightarrow3\cdot0,1+2\cdot0,05=4\cdot0,05+2\cdot x\)
\(\Rightarrow x=0,1mol\)
\(m=m_{Al}+m_{Mg}+m_{O_2}+m_{Cl_2}\)
\(=0,1\cdot27+0,05\cdot24+0,05\cdot2\cdot16+0,1\cdot35,5\cdot2\)
\(=12,6g\)
Đúng 4
Bình luận (0)
Theo bảo toàn electron ta có: \(3\cdot n_{Al}+2\cdot n_{Mg}=2\cdot n_{Cl_2}+4\cdot N_{O_2}\)
\(\Rightarrow3\cdot0,1+2\cdot0,05=4\cdot0,05+2x\Rightarrow x=0,2\)
\(\Rightarrow m_Z=m_X+m_Y=0,1\cdot27+0,05\cdot24+0,05\cdot32+0,2\cdot71=19,7g\)
Đúng 0
Bình luận (0)
Cho 5,7g hỗn hợp gồm Mg và Al tác dụng vừa đủ với hỗn hợp khí gồm 0,1 mol O2 0,4 mol Cl2 thu được hỗn hợp rắn gồm các muối clorua và oxit. Tính % khối lượng
Gọi \(n_{Mg} = a(mol) ; n_{Al} = b(mol)\\ \Rightarrow 24a + 27b = 5,7(1)\)
\(Mg^0 \to Mg^{+2} + 2e\\ Al^0 \to Al^{+3} + 3e\\ O_2 + 4e \to 2O^{-2}\\ Cl_2 + 2e \to 2Cl^-\)
Bảo toàn electron : \(2n_{Mg} + 3n_{Al} = 2a + 3b = 4n_{O_2} + 2n_{Cl_2} = 1,2(mol)\)(2)
Từ (1)(2) suy ra : a = -0,85< 0 ⇒ Sai đề
Đúng 1
Bình luận (0)
X{Mg, Al} + {Cl2, O2} → Z
Áp dụng định luật BTKL: mCl2 + mO2 = mZ – mX = 19,7 – 7,8 = 11,9 gam
Theo đề bài ta có hệ phương trình:
Đúng 1
Bình luận (0)
Hỗn hợp X gồm Mg và Fe có tỉ lệ số mol tương ứng 1 : 3. Đốt cháy m gam hỗn hợp X bằng hỗn hợp khí Y gồm Cl2 và O2, sau phản ứng thu được hỗn hợp Z gồm các oxit và các muối clorua (không còn khí dư). Hòa tan Z bằng một lượng vừa đủ 300 ml dung dịch HCl 1M, thu được dung dịch T. Cho AgNO3 dư vào T thu được 154,3 gam kết tủa. Cho m gam hỗn hợp X tác dụng với dung dịch HNO3 dư thu được 0,1 mol NO; dung dịch Q. Cô cạn cẩn thận dung dịch Q thu được 95,4 gam chất rắn khan. Số mol của khí Cl2 có trong Y...
Đọc tiếp
Hỗn hợp X gồm Mg và Fe có tỉ lệ số mol tương ứng 1 : 3. Đốt cháy m gam hỗn hợp X bằng hỗn hợp khí Y gồm Cl2 và O2, sau phản ứng thu được hỗn hợp Z gồm các oxit và các muối clorua (không còn khí dư). Hòa tan Z bằng một lượng vừa đủ 300 ml dung dịch HCl 1M, thu được dung dịch T. Cho AgNO3 dư vào T thu được 154,3 gam kết tủa. Cho m gam hỗn hợp X tác dụng với dung dịch HNO3 dư thu được 0,1 mol NO; dung dịch Q. Cô cạn cẩn thận dung dịch Q thu được 95,4 gam chất rắn khan. Số mol của khí Cl2 có trong Y là?
A. 0,25
B. 0,30
C. 0,40
D. 0,35
Hỗn hợp X gồm Mg và Fe có tỉ lệ số mol tương ứng 1 : 3. Đốt cháy m gam hỗn hợp X bằng hỗn hợp khí Y gồm Cl2 và O2, sau phản ứng thu được hỗn hợp Z gồm các oxit và các muối clorua (không còn khí dư). Hòa tan Z bằng một lượng vừa đủ 300 ml dung dịch HCl 1M, thu được dung dịch T. Cho AgNO3 dư vào T thu được 154,3 gam kết tủa. Cho m gam hỗn hợp X tác dụng với dung dịch HNO3 dư thu được 0,1 mol NO; dung dịch Q. Cô cạn cẩn thận dung dịch Q thu được 95,4 gam chất rắn khan. Số mol của khí Cl2 có trong Y...
Đọc tiếp
Hỗn hợp X gồm Mg và Fe có tỉ lệ số mol tương ứng 1 : 3. Đốt cháy m gam hỗn hợp X bằng hỗn hợp khí Y gồm Cl2 và O2, sau phản ứng thu được hỗn hợp Z gồm các oxit và các muối clorua (không còn khí dư). Hòa tan Z bằng một lượng vừa đủ 300 ml dung dịch HCl 1M, thu được dung dịch T. Cho AgNO3 dư vào T thu được 154,3 gam kết tủa. Cho m gam hỗn hợp X tác dụng với dung dịch HNO3 dư thu được 0,1 mol NO; dung dịch Q. Cô cạn cẩn thận dung dịch Q thu được 95,4 gam chất rắn khan. Số mol của khí Cl2 có trong Y là?
A. 0,25
B. 0,30
C. 0,40
D. 0,35
Cho V lít hỗn hợp khí A gồm clo và oxi tác dụng vừa hết với hỗn hợp B gồm 0,2 mol Al và 0,1 mol Mg thì thu được 25,2 gam hỗn hợp muối clorua và oxit của 2 kim loại. Số mol của Cl2 có trong V lít hỗn hợp khí A là A. 0,15 B. 0,25 C. 0,2 D. 0,3
Đọc tiếp
Cho V lít hỗn hợp khí A gồm clo và oxi tác dụng vừa hết với hỗn hợp B gồm 0,2 mol Al và 0,1 mol Mg thì thu được 25,2 gam hỗn hợp muối clorua và oxit của 2 kim loại. Số mol của Cl2 có trong V lít hỗn hợp khí A là
A. 0,15
B. 0,25
C. 0,2
D. 0,3
Chọn C. Đặt nCl2=x mol và nO2=y mol. Phản ứng vừa đủ tạo muối gồm các ion sau: Al3+, Mg2+ , Cl- , O2-.
Theo định luât bảo toàn điện tích: 3nAl3+ +2nMg2+ = nCl- + 2nO2- = 2nCl2 + 4nO2
mmuối= 27nAl3+ +24nMg2+ + 35,5nCl- + 16nO2-
→ Hệ
3 . 0 , 2 + 2 . 0 , 1 = 2 x + 4 y 27 . 0 , 2 + 24 . 0 , 1 + 71 x + 32 y = 25 , 2 → x = 0 , 2 y = 0 , 1
Đúng 0
Bình luận (0)
Một hỗn hợp X gồm 8,8 gam CO2 và 19,2 gam SO2. Tính tỉ khối của X đối với:a, Khí hydrogen.b, Hỗn hợp khí Y gồm: 0,1 mol CH4 và 0,4 mol N2
Đọc tiếp
Một hỗn hợp X gồm 8,8 gam CO2 và 19,2 gam SO2. Tính tỉ khối của X đối với:
a, Khí hydrogen.
b, Hỗn hợp khí Y gồm: 0,1 mol CH4 và 0,4 mol N2
Cho hỗn hợp X gồm (0,1 mol KMnO4; 0,15 mol KClO3; 0,2 mol CaOCl2; 0,25 mol K2MnO4) tác dụng với dung dịch HCl đặc, dư thu được V lít khí Cl2 (đktc) và dung dịch Y. Số mol HCl đã tham gia phản ứng là