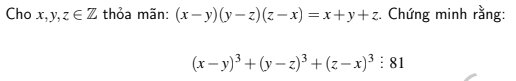
giups emmm vois moij nguoiwf
Timf soos tuwj nhieen nhor nhaast cos ba chuxw soos chia cho 11 duw 5, chia cho 13 duw 8
Giups minhf gaasp, ai ddungs minhf tichs, khoong caanf suawr laij ddeef ddaau, minhf chir caafn loiwf giair vaf ddaps ans thooi nha moij nguoiwf. GAAPS GAAPS GAAPS
Tìm hai số tự nhiên có tổng bằng 2019 biết giữa chúng có 4 số chẵn
MOIJ NGUOIWF GIAIR CHI TIEETS NHA
Em hayx ddawjc caau cos hifnh arnh nhaan hoas nois veef 1 loafi vaatj em yeeu thisch
sorry moij nguoiwf masy mifnh trar bieest lafm sao maf ko vieets tieengs vieetj
Trả lời
Chú mèo nhà em ngoan lắm
HT
|x-5|-|2x-4|=0
moij nguwowif giair giups minhf vowi
|x - 5| - |2x - 4| = 0
<=> |x - 5| = 0 + |2x - 4|
<=> |x - 5| = |2x - 4|
Xét 2 trường hợp: 2x - 4 = x - 5
2x - 4 = -(x - 5)
TH1: 2x - 4 = x - 5
<=> 2x - 4 - x = -5
<=> x - 4 = -5
<=> x = -5 + 4
<=> x = -1
TH2: 2x - 4 = -(x - 5)
<=> 2x - 4 = -x + 5
<=> 2x - 4 + x = 5
<=> 3x - 4 = 5
<=> 3x = 5 + 4
<=> 3x = 9
<=> x = 3
=> x = 3
Vậy: x = -1 hoặc x = 3
( 5x – 29 ) – ( 2x – 29 ) = - 21
3.( 2 – x ) + 4.( x – 5 ) = 14
( 2x – 1)2– 29 = - 4
x^2+ 5 = 14
giups mik vois
\(\left(5x-29\right)-\left(2x-29\right)=-21\)
\(5x-29-2x+29=-21\)
\(5x-2x=-21+29-29\)
\(3x=-21\)
\(x=-7\)
Mootj thungf dduwngj dduwowcj 47 lits xawng, mootj can dduwngj dduwowcj 9 lits xawng. Hoir 1 thungf vaf 4 can dduwngj dduwowcj bao nhieeu lits xawng?
giair giups mik vowis moij nguwowif!!!
Một thùng và bốn can đựng đc số l xăng là:
47+ 4✖9=83 (l)
Banj lamf 2 pheps tinhs dduwowcj ko aj?
Mootj ddanf gaf cos 74 con. Sau khi bans ddi 18 con gaf, nguwowif ta nhoots ddeeuf soos gaf conf laij vaof 8 chuoongf. Hoir mooix chuoongf nhoots bao nhieeu con gaf?
giups mik ddi moij nguwowif!!!
Sau khi bán còn số gà là : 74-18=56(con)
Mỗi chuồng có số gà là : 56 :8=7(con)
Đ/S: 7 con
giúp emmm
Giúp emmm
helpp emmm
Bài 1 :
\(2H_2 + O_2 \xrightarrow{t^o} 2H_2O\\ S + O_2 \xrightarrow{t^o} SO_2\\ 4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3\\ 4P + 5O_2 \xrightarrow{t^o} 2P_2O_5\)
Bài 2 :
\(3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4\\ a) n_{Fe_3O_4} = \dfrac{2,32}{232} = 0,01(mol)\\ n_{Fe} = 3n_{Fe_3O_4} = 0,03(mol)\Rightarrow m_{Fe} = 0,03.56 = 1,68(gam)\\ n_{O_2} = 2n_{Fe_3O_4} = 0,02(mol) \Rightarrow m_{O_2} = 0,02.32 = 0,64(gam)\\ b) 2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2\\ n_{KMnO_4} = 2n_{O_2} = 0,04(mol)\Rightarrow m_{KMnO_4} = 0,04.158= 6,32(gam)\)