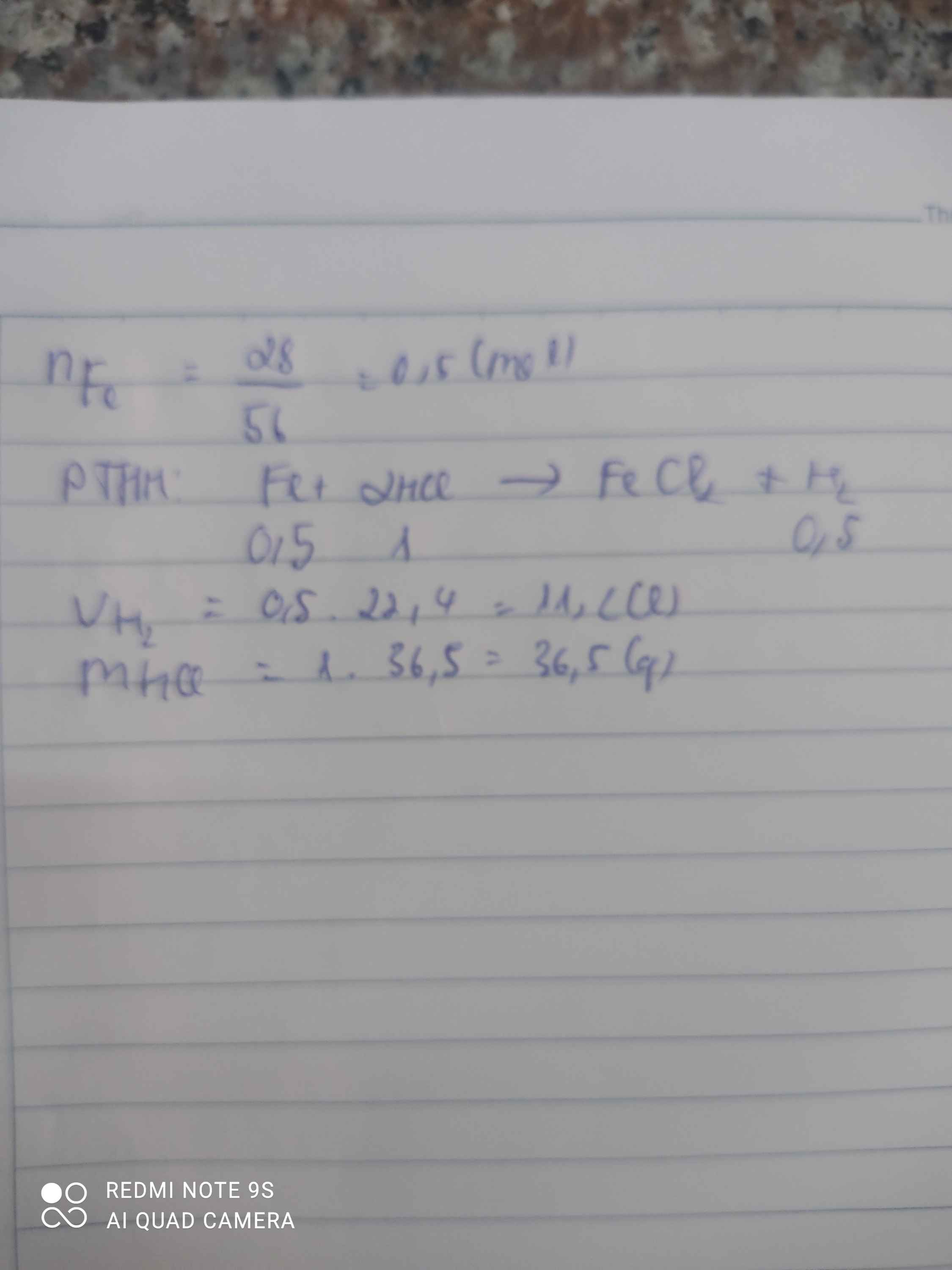cho sắt tác dụng vừa đủ với 300 ml dung dịch HCl. sau phản ứng thu được 4,958 lít khí H2 ở điều kiện chuẩn a) viết phương trình hóa học b) tính khối lượng sắt tham gia phản ứng c) tính nồng độ mol của HCl đã dùng ( cíu em với ạ TT)

Những câu hỏi liên quan
Choo kim loại sắt tác dụng với 200 ml HCl thu được 2,479 lít khí ở điều kiện tiêu chuẩn. a. viết phương trình hóa học. b. Tính khối lượng sắt tham gia phản ứng. c.Tính nồng độ mol của dung dịch HCl đã dùng.
\(n_{H_2}=\dfrac{2.479}{24.79}=0.1\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(0.1.......0.2..........0.1......0.1\)
\(m_{Fe}=0.1\cdot56=5.6\left(g\right)\)
\(C_{M_{HCl}}=\dfrac{0.2}{0.2}=1\left(M\right)\)
Đúng 2
Bình luận (0)
Cho sắt tác dụng với 200 ml dung dịch H2 SO4 thu được 6,72 lít khí bay ra ở điều kiện tiêu chuẩn vào dung dịch FeSO4 a Tính khối lượng sắt tham gia phản ứng B Tính nồng độ mol dung dịch H2SO4 ban đầu C nếu cho lượng sắt ở trên phản ứng với 49 gam dung dịch H2SO4 40% tính nồng độ các dung dịch sau phản ứng
Sửa lại câu c .
\(n_{H_2SO_4}=\dfrac{49.40}{100}:98=0,2\left(mol\right)\)
\(PTHH:\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
trc p/u : 0,3 0,2
p/u : 0,2 0,2 0,2 0,2
sau : 0,1 0 0,2 0,2
-> Fe dư
\(m_{ddFeSO_4}=0,3.56+49-0,4=65,4\left(g\right)\) ( ĐLBTKL )
\(m_{FeSO_4}=0,2.152=30,4\left(g\right)\)
\(C\%=\dfrac{30,4}{65,4}.100\%\approx46,48\%\)
Đúng 2
Bình luận (0)
PTHH :
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
0,3 0,3 0,3 0,3
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(a,m_{Fe}=0,3.56=16,8\left(g\right)\)
\(b,C_M=\dfrac{n}{V}=\dfrac{0,3}{0,2}=1,5M\)
\(c,n_{H_2SO_4}=\dfrac{\dfrac{49.40}{100}}{98}=0,2\left(mol\right)\)
\(\rightarrow n_{FeSO_4}=n_{H_2SO_4}=0,2\left(mol\right)\)
\(m_{FeSO_4}=0,2.152=30,4\left(g\right)\)
\(m_{ddFeSO_4}=49+\left(0,2.56\right)-0,2.2=59,8\left(g\right)\)( định luật bảo toàn khối lượng )
\(C\%=\dfrac{30,4}{59,8}.100\%\approx50,84\%\)
Đúng 1
Bình luận (1)
Cho một khối lượng mạt sắt dư vào 50 ml dung dịch HCl .Phản ứng xong thu được 3,36 lít khí (đktc) . Viết phương trình hóa học .Tính khối lượng mạt sắt đã tham gia phản ứng Tính nồng độ mol của dung dịch HCl đã dùng .
Giải giúp mik với ạ
\(n_{H2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
a) Pt : \(Fe+2HCl\rightarrow FeCl_2+H_2|\)
1 2 1 1
0,15 0,3 0,15
b) \(n_{Fe}=\dfrac{0,15.1}{1}=0,15\left(mol\right)\)
⇒ \(m_{Fe}=0,15.56=8,4\left(g\right)\)
c) \(n_{HCl}=\dfrac{0,15.2}{1}=0,3\left(mol\right)\)
50ml = 0,05l
\(C_{M_{ddHCl}}=\dfrac{0,3}{0,05}=6\left(M\right)\)
Chúc bạn học tốt
Đúng 4
Bình luận (0)
Hòa tan một lượng sắt bằng dung dịch h2so4 (loãng) vừa đủ phản ứng thu được 16,8 lít khí hidro ở điều kiện tiêu chuẩn a) viết phương trình hóa học của phản ứngb) tính khối lượng sắt đã phản ứng C) nếu cho khố lượng sắt vừa đủ ở trên phản ứng với 245g dung dịch H2SO4 10% thì sau phản ứng chất nào còn dư và dư bao nhiêu
Đọc tiếp
Hòa tan một lượng sắt bằng dung dịch h2so4 (loãng) vừa đủ phản ứng thu được 16,8 lít khí hidro ở điều kiện tiêu chuẩn
a) viết phương trình hóa học của phản ứng
b) tính khối lượng sắt đã phản ứng
C) nếu cho khố lượng sắt vừa đủ ở trên phản ứng với 245g dung dịch H2SO4 10% thì sau phản ứng chất nào còn dư và dư bao nhiêu
\(a,PTHH:Fe+H_2SO_4\to FeSO_4+H_2\\ b,n_{H_2}=\dfrac{16,8}{22,4}=0,74(mol)\\ \Rightarrow n_{Fe}=0,75(mol)\\ \Rightarrow m_{Fe}=0,75.56=42(g)\\ c,n_{H_2SO_4}=\dfrac{245.10\%}{100\%.98}=0,25(mol)\)
Vì \(\dfrac{n_{Fe}}{1}>\dfrac{n_{H_2SO_4}}{1}\) nên \(Fe\) dư
\(n_{Fe(dư)}=0,75-0,25=0,5(mol)\\ \Rightarrow m_{Fe(dư)}=0,5.56=28(g)\)
Đúng 0
Bình luận (0)
Cho một khối lượng bột sắt tác dụng vừa đủ với 500 ml dung dịch axit clohiđric có nồng độ 0,2 M a) viết phương trình phản ứng b) xác định khối lượng của sắt đã tham gia phản ứng c) tính khối lượng muối thu được sau phản ứng
\(n_{HCl}=0,2.0,5=0,1(mol)\\ a,Fe+2HCl\to FeCl_2+H_2\\ \Rightarrow n_{Fe}=n_{FeCl_2}=\dfrac{1}{2}n_{HCl}=0,05(mol)\\ b,m_{Fe}=0,05.56=2,8(g)\\ c,m_{FeCl_2}=0,05.127=6,35(g)\)
Đúng 3
Bình luận (0)
Cho một lượng mạt sắt dư vào 50ml dung dịch HCL. Phản ứng xong thu được 3,36 lít khí Viết phương trình hóa học Tính khối lượng mạt sắt đã tham gia phản ứng Tìm nồng độ mol của dung dịch HCL đã dùng Giúp mình với
\(n_{H2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Pt : \(Fe+2HCl\rightarrow FeCl_2+H_2|\)
1 2 1 1
0,15 0,3 0,15
\(n_{Fe}=\dfrac{0,15.1}{1}=0,15\left(mol\right)\)
⇒ \(m_{Fe}=0,15.56=8,4\left(g\right)\)
\(n_{HCl}=\dfrac{0,15.2}{1}=0,3\left(mol\right)\)
50ml = 0,05l
\(C_{M_{HCl}}=\dfrac{0,3}{0,05}=6\left(M\right)\)
Chúc bạn học tốt
Đúng 1
Bình luận (0)
Hòa tan một lượng sắt bằng dung dịch h2so4 (loãng) vừa đủ phản ứng thu được 16,8 lít khí hidro ở điều kiện tiêu chuẩn
a) viết phương trình hóa học của phản ứng
b) tính khối lượng sắt đã phản ứng
a) Fe + H2SO4 → FeSO4 + H2
b) Ta có : nH2 = \(\dfrac{16,8}{22,4}\) = 0,75 (mol)
⇒ nFe= 0,75.56 = 42(gam)
Đúng 0
Bình luận (0)
Ta có: \(n_{H_2}=\dfrac{16,8}{22,4}=0,75\left(mol\right)\)
a. \(PTHH:Fe+H_2SO_4--->FeSO_4+H_2\uparrow\)
b. Theo PT: \(n_{Fe}=n_{H_2}=0,75\left(mol\right)\)
\(\Rightarrow m_{Fe}=56.0,75=42\left(g\right)\)
Đúng 0
Bình luận (0)
cho 28 gam sắt tác dụng với axit HCl (dư) sau phản ứng thu được (II) clorua (FeCl2) và khí hiđro
a viết phương trình phản ứng
b tính thể tích khí H2 thu được ở điều kiện tiêu chuẩn?
c tính khối lượng axit HCl đã tham gia phản ứng
\(n_{Fe}=\dfrac{28}{56}=0,5mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,5 1 0,5
\(V_{H_2}=0,5\cdot22,4=11,2l\)
\(m_{HCl}=1\cdot36,5=36,5g\)
Đúng 4
Bình luận (0)
Cho săt tác dụng vừa đủ với 182,5 gam dung dịch HCl 5% đến khi phản ứng kết thúc thu được V lít khí ở đktc?
a.Viết phương trình hóa học xảy ra?
b. Tính khối lượng sắt đã phản ứng và tính V?
c. tính khối lượng HCl, khối lượng muối
d.Tính nồng độ phần trăm của dung dịch muối thu được
`a)PTHH`
`Fe + 2HCl -> FeCl_2 + H_2`
`0,125` `0,25` `0,125` `0,125` `(mol)`
`n_[HCl]=[5/100 .182,5]/[36,5]=0,25(mol)`
`b)m_[Fe]=0,125.56=7(g)`
`V_[H_2]=0,125.22,4=2,8(l)`
`c)m_[HCl]=0,25.36,5=9,125(g)`
`m_[FeCl_2]=0,125.127=15,875(g)`
`d)C%_[FeCl_2]=[15,875]/[7+182,5-0,125.2] .100~~8,39%`
Đúng 4
Bình luận (0)
\(a,m_{HCl}=\dfrac{182,5.5}{100}=9,125\left(g\right)\\ \rightarrow n_{HCl}=\dfrac{9,125}{36,5}=0,25\left(mol\right)\)
PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,125<-0,25--->0,125---->0,125
\(b,\left\{{}\begin{matrix}m_{Fe}=0,125.56=7\left(g\right)\\V_{H_2}=0,125.22,4=2,8\left(l\right)\end{matrix}\right.\\ c,m_{muối}=0,125.127=15,875\left(g\right)\\ d,m_{dd}=7+182,5-0,125.2=189\left(g\right)\\ \rightarrow C\%_{FeCl_2}=\dfrac{15,875}{189}.100\%=8,4\%\)
Đúng 2
Bình luận (0)
Xem thêm câu trả lời