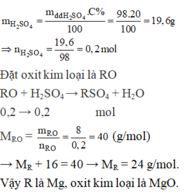Hoà tan 8 gam oxit của một kim loại hoá trị 2 vào 200 gam dd H2SO4 9.8% thì vừa đủ .Tìm oxit ?

Những câu hỏi liên quan
Hoà tan 3,2 gam oxit của một kim loại hoá trị ( III) bằng 200 gam dung dịch H2SO4 loãng. Khi thêm vào hỗn hợp sau phản ứng một lượng CaCO3 vừa đủ thấy thoát ra 0,224 dm3 CO2 (đktc), sau đó cô cạn dung dịch thu được 9,36 gam muối khan. Xác định oxit kim loại trên và nồng độ % H2SO4 đã dùng.
Gọi công thức oxit của kim loại hóa trị III là A2O3,ta có các phương trình sau
A2O3+3H2SO4--->A2(SO4)3+3H2O (1)
0,02<--0,06<---------0,02
Vì sau phản ứng (1) dung dịch còn có thể phản ứng với CaCO3 giải phóng khí CO2=>axit H2SO4 dư,ta có phương trình
H2SO4+CaCO3--->CaSO4+CO2+H2O (2)
0,01<-----0,01--------0,01<-----0,01
nCO2=0,224:22,4=0,01 mol
Khối lượng muối A2(SO4)3 sau khi cô cạn là
9,36-0,01x(40+96)=8 g
Ta thấy rằng A2O3=3,2 g,sau phản ứng tạo thành muối A2(SO4)3=8g Như vậy khối lượng tăng thêm là do 3 gốc -SO4 thay thế cho 3 nguyên tử Oxi,vậy khối lượng tăng thêm là 8-3,2 =4,8 g
nA2SO4=4,8:(96x3-16x3)=0,02 mol
=>khối lượng muối=0,02x(2xR+96x3)=8
=>R=56
R hóa trị III, có M=56=>R là Fe,công thức oxit là Fe2O3
nH2SO4=0,01+0,06=0,07 mol
mH2SO4=0,07x98=6,86g
C% đ H2SO4=(6,86:200)x100%=3,43%
Đúng 1
Bình luận (2)
Hòa tan 8 gam oxit của một kim loại hóa trị II vào 98 gam dung dịch H 2 S O 4 20% thì vừa đủ . Oxit đó là:
A. CuO
B. CaO
C. MgO
D. FeO
Hoà tan hoàn toàn 8,0 gam một oxit kim loại A (A có hoá trị II trong hợp chất) cần dùng vừa đủ 400ml dung dịch HCl 1M
1. Xác định kim loại A và công thức hoá học của oxit.
2. Cho 8,4 gam ACO3 tác dụng với 500ml dung dịch H2SO4 1M đến khi phản ứng xảy ra hoàn toàn. Tính nồng độ mol của các chất trong dung dịch sau phản ứng (coi thể tích dung dịch sau phản ứng vẫn là 500 ml).
1) Gọi công thức của oxit là AO. Số mol HCl là 0,4.1=0,4 (mol).
AO (0,2 mol) + 2HCl (0,4 mol) \(\rightarrow\) ACl2 + H2\(\uparrow\).
Phân tử khối của oxit là 8,0/0,2=40 (g/mol).
Vậy A là magie (Mg) và công thức hóa học của oxit là MgO.
2) Số mol MgCO3 và H2SO4 lần lượt là 8,4/84=0,1 (mol) và 0,5.1=0,5 (mol).
Các chất tan trong dung dịch sau phản ứng gồm MgSO4 (0,1 mol) và H2SO4 dư (0,4 mol) có nồng độ mol lần lượt là 0,1/0,5=0,2 (M) và 0,4/0,5=0,8 (M).
Đúng 2
Bình luận (0)
\(1,n_{HCl}=0,4.1=0,4\left(mol\right)\\ PTHH:AO+2HCl\rightarrow ACl_2+H_2O\\ Mol:0,2\leftarrow0,4\\ M_{AO}=\dfrac{8}{0,2}=40\left(\dfrac{g}{mol}\right)\\ \Leftrightarrow A+16=40\\ \Leftrightarrow A=24\left(\dfrac{g}{mol}\right)\\ \Leftrightarrow A.là.Mg\\ CTHH:MgO\)
\(2,n_{H_2SO_4}=1.0,5=0,5\left(mol\right)\\ PTHH:MgCO_3+H_2SO_4\rightarrow MgSO_4+CO_2\uparrow+H_2O\\ Mol:0,5\leftarrow0,5\rightarrow0,5\\ C_{M\left(MgSO_4\right)}=\dfrac{0,5}{0,5}=1M\)
\(1,n_{HCl}=0,4.1=0,4\left(mol\right)\\ PTHH:AO+2HCl\rightarrow ACl_2+H_2O\\ Mol:0,2\leftarrow0,4\\ M_{AO}=\dfrac{8}{0,2}=40\left(\dfrac{g}{mol}\right)\\ \Leftrightarrow A+16=40\\ \Leftrightarrow A=24\left(\dfrac{g}{mol}\right)\\ \Rightarrow A.là.Mg\\ CTHH:MgO\)
\(2,n_{MgCO_3}=\dfrac{8,4}{84}=0,1\left(mol\right)\\ n_{H_2SO_4}=1.0,5=0,5\left(mol\right)\\ PTHH:MgCO_3+H_2SO_4\rightarrow MgSO_4+CO_2\uparrow+H_2O\\ LTL:0,1< 0,5\Rightarrow H_2SO_4.dư\\ Theo.pt:n_{H_2SO_4\left(pư\right)}=n_{MgSO_4}=n_{MgCO_3}=0,1\left(mol\right)\\ C_{MMgSO_4}=\dfrac{0,1}{0,5}=0,2M\\ C_{MH_2SO_4\left(dư\right)}=\dfrac{0,4}{0,5}=0,8M\)
Đúng 1
Bình luận (0)
Hoà tan 8,1 gam ZnO vào 122,5 gam dung dịch H2SO4 20%.a/ Viết phương trình hoá học.b/ Tính nồng độ phần trăm các chất trong dung dịch sau phản ứng.c/ Nếu cho lượng axit còn dư phản ứng với một oxit bazo của kim loại hoá trị III, vừa đủ thì được 17,1 gam muối. Xác định công thức phân tử của oxit.
Đọc tiếp
Hoà tan 8,1 gam ZnO vào 122,5 gam dung dịch H2SO4 20%.
a/ Viết phương trình hoá học.
b/ Tính nồng độ phần trăm các chất trong dung dịch sau phản ứng.
c/ Nếu cho lượng axit còn dư phản ứng với một oxit bazo của kim loại hoá trị III, vừa đủ thì được 17,1 gam muối. Xác định công thức phân tử của oxit.
Hoà tan a gam oxit MO ( M là kim loại có hoá trị 2 không đổi ) bằng một lượng vừa đủ H2SO4 17,5 %, thu được dung dịch muối có nồng độ 20 %. Xác định kim loại M.
`MO + H_2 SO_4 -> MSO_4 + H_2 O`
`1` `1` `1` `1` `(mol)`
Giả sử `n_[H_2 SO_4] = 1 (mol)`
`m_[dd H_2 SO_4] = [ 1 . 98 ] / [ 17,5 ] . 100 = 560 (g)`
`C%_[MSO_4] = [ 1 ( M_M + 96 ) ] / [ 1 . ( M_M + 16 ) + 560 ] . 100 = 20`
`<=> M_M = 24`
`=> M` là `Mg`
Đúng 2
Bình luận (0)
Bài 7: Hoà tan 5,4g kim loại A (hoá trị III) vào dd H2SO4 19,6% lấy vừa đủ thu được 7,2 lít H2.
a) Đã dùng mấy gam dd H2SO4?
b) Tìm kim loại A.
a,\(n_{H_2\left(đkt\right)}=\dfrac{7,2}{24}=0,3\left(mol\right)\)
PTHH: 2A + 3H2SO4 → A2(SO4)3 + 3H2
Mol: 0,2 0,3 0,3
\(m_{H_2SO_4}=0,3.98=29,4\left(g\right)\)
\(m_{ddH_2SO_4}=29,4:19,6\%=150\left(g\right)\)
b, \(M_A=\dfrac{5,4}{0,2}=27\left(g/mol\right)\)
⇒ A là kim loại nhôm (Al)
Đúng 1
Bình luận (0)
Hoà tan 3,2g Oxit kim loại hoá trị III bằng 200g dung dịch H2SO4 loãng. Khi thêm vào hoà tan 1 oxit kim loai htri IV biết rằng hoà tan 8g oxit này bằng 300ml dd H2SO4 1M. sau p/ứ trung hoà lượng axit còn dư bằng 50g dd NaOH 24%. tìm cthỗn hợp sau phản ứng 1 lượng CaCO3 vừa đủ thấy 0,0224dm3 CO2 ở đktc sau đó cô cạn dung dịch thu được 9,36g muối sunfat khô. Tìn công thức õit kim loại và C% H2SO4
Oxi hoá 13,6 gam hỗn hợp 2 kim loại thu được m gam hỗn hợp 2 oxit . Để hoà tan hoàn toàn m gam oxit này cần 500ml dd
H
2
S
O
4
1M . Tính m: A. 18,4g B. 21,6g C. 23,45g D. Kết quả khác
Đọc tiếp
Oxi hoá 13,6 gam hỗn hợp 2 kim loại thu được m gam hỗn hợp 2 oxit . Để hoà tan hoàn toàn m gam oxit này cần 500ml dd H 2 S O 4 1M . Tính m:
A. 18,4g
B. 21,6g
C. 23,45g
D. Kết quả khác
Ta có:
n H 2 O s a n p h a m = n H 2 S O 4 = 1 . 0 , 5 = 0 , 5 m o l = n O / o x i t
Theo định luật bảo toàn khối lượng, ta có:
m o x i t = m K L + m O / o x i t
=13,6 + 0,5.16 = 21,6g
⇒ Chọn B.
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 8 gam một oxit kim loại A( A có hóa trị 2 trong hợp chất) cần dùng vừa đủ 400 ml dd HCl 1M
1. Xác định kim loại A và công thức hóa học của oxit
2. cho 8,4 gam ACO3 tác dụng với 500 ml dd H2SO4 1M đến khi phản ứng xảy ra hoàn toàn. Tính nồng độ mol của các chất trong dd sau phản ứng ( coi thể tích dd sau phản ứng là 500 ml )