Dung dịch có chứa CH3COOH 0,1M và CH3COONa 0,1M. Tính độ pH của dung dịch. Biết rằng hằng số axit của CH3COOH là Ka = 10-4,76.

Những câu hỏi liên quan
Tính pH của dung dịch hỗn hợp CH3COOH 0,1M và CH3COONa 0,1M. Biết rằng ở một nhiệt độ xác định t°C có
K
a
C
H
3
C
O
O
H
1
,
8
....
Đọc tiếp
Tính pH của dung dịch hỗn hợp CH3COOH 0,1M và CH3COONa 0,1M. Biết rằng ở một nhiệt độ xác định t°C có K a C H 3 C O O H = 1 , 8 . 10 - 5
A. 1
B. 1,745
C. 1,754
D. 1,7
Đáp án B
Vì CH3COONa là chất điện li mạnh nên được viết trước để tạo môi trường cho cân bằng của chất điện li yếu phân li và cân bằng:
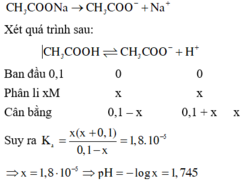
Đúng 0
Bình luận (1)
Thêm 0,001mol HCI vào 1 lít dung dịch hỗn hợp CH3COONa 0,1M và CH3COOH 0,1M thì pH dung dịch thu được là bao nhiêu?
thầy cho em hỏi cách tính pH của dung dịch đệm ạ
tính pH của dung dịch đệm gồm CH3COOH 0.1M và CH3COONa 0.1M biết hằng số điện li của CH3COOH là 1,76.10^-5
HD:
CH3COOH \(\leftrightarrow\) CH3COO- + H+
Ban đầu: 0,1 M 0,1 M 0
Cân bằng: 0,1-x 0,1+x x
Hằng số cb: ka = [CH3CO-][H+]/[CH3COOH] = (0,1+x).x/(0,1-x) = 1,76.10-5. Giải pt thu được x, mà [H+] = x nên pH = -log[H+] = -log(x).
Đúng 0
Bình luận (0)
em cũng có thể dùng công thức pH= -LogKa + Log(Cb/Ca)
với Cb,Ca là nồng độ bazo và axit
Đúng 1
Bình luận (0)
đấy là công thức gần đúng, trong một số trường hợp cần sự chính xác thì công thức đó ko dùng được
Đúng 0
Bình luận (0)
Dung dịch CH3COOH 0,1M có độ điện li α = 1%. Tính pH của dung dịch thu được.
A.1
B.2
C. 3
D. Đ/a khác
Dung dịch X gồm CH3COOH 0,03M và CH3COONa 0,01M. Biết ở 250C; Ka của CH3COOH là 1,75.10-5; bỏ qua sự phân li của nước. Giá trị pH của dung dịch X ở 250C là: A. 4,28 B. 4,04 C. 4,76 D. 6,28
Đọc tiếp
Dung dịch X gồm CH3COOH 0,03M và CH3COONa 0,01M. Biết ở 250C; Ka của CH3COOH là 1,75.10-5; bỏ qua sự phân li của nước. Giá trị pH của dung dịch X ở 250C là:
A. 4,28
B. 4,04
C. 4,76
D. 6,28
Do đây là dung dịch đệm nên ta có CT tính nhanh : pH = pKa + log(Cb/Ca) (Ca là nồng độ mol của axit ; Cb là nồng độ mol của muối)
=> pH = 4,28
=>A
Đúng 0
Bình luận (0)
Tính pH của dung dịch axit HCOOH 0,1M. Biết hằng số axit của axit fomic là 10-3,75
Cho 0.03 mol axit HCl vào 1 L của dung dịch đệm
có nồng độ 0,6 M CH3COOH and 0,6M
CH3COONa. Tính pH của dung dịch. Biết hằng số
phân li của axit CH3COOH là: 1,8x10-5 ở 25oC
$CH_3COONa + HCl \to CH_3COOH + NaCl$
$n_{CH_3COOH} = 0,6.1 + 0,03 = 0,63(mol)$
$[H^+] = 0,63.1,8.10^{-5} = 1,134.10^{-5}M$
$pH = -log([H^+]) = -log(1,134.10^{-5}) = 4,945$
Đúng 3
Bình luận (1)
cho dung dịch axit HNO2 0,1M, biết rằng hằng số phân li của axit Ka = 5.10-4. nồng độ mol/l của ion H+ là:
HNO2→H+ + NO2-
ban đầu 0,1..........0...........0
phân li x............x............x
cân bằng 0,1-x......x............x
\(Ka=\dfrac{\left[H^+\right]\left[NO_2^-\right]}{\left[HNO_2\right]}\\ 5.10^{-4}=\dfrac{x^2}{0,1-x}\)
\(\Rightarrow\left[H^+\right]=x=....\)
Em có thể tham khảo lí thuyết vào bài tập thêm trong chủ đề này
https://hoc24.vn/ly-thuyet/gia-tri-ph-cua-cac-dung-dich-axit-bazo.4749/
Đúng 0
Bình luận (0)
Tính pH của dung dịch NH4+ 10^-3M biết pK NH3=4,76 Tính pH của hỗn hợp CH3COOH 10^-2M và CH3COO- 10^-3M














