Trong 200 ml dung dịch A có chứa 0,2 mol ion Na+; 0,6 mol NH4+; 0,4 mol H+; 0,2mol Cl-; 0,5 mol SO42-. Dung dịch B chứa hh 2 hiđroxit KOH 1M và Ba(OH)2 2M .Cho 300ml dung dịch B vào dung dịch A , đun nnh. Tính khối lượng giảm sau phản ứng .

Những câu hỏi liên quan
Câu1: Một dung dịch chứa 0,2 mol Cu2+; 0,1 mol K+; 0,05 mol Cl- và x mol SO42-. Tổng khối lượng muối có trong dung dịch là m gam. Giá trị của m
Câu2: Trộn 150 ml dung dịch Na2SO4 0,5M với 50 ml dung dịch NaCl 1M thì nồng độ ion Na+ có trong dung dịch tạo thành
Câu3: Giá trị pH của dung dịch HCl 0,1M
Câu4: Trên chai hóa chất có ghi: dung dịch HCl 0,1M. Hỏi trong chai hóa chất đó chứa ion nào sau đây? (không kể sự điện li của H2O).
Câu 5: Để trung hòa 20 ml dung dịch HCl 0,1M cần 10 ml dung dịch...
Đọc tiếp
Câu1: Một dung dịch chứa 0,2 mol Cu2+; 0,1 mol K+; 0,05 mol Cl- và x mol SO42-. Tổng khối lượng muối có trong dung dịch là m gam. Giá trị của m Câu2: Trộn 150 ml dung dịch Na2SO4 0,5M với 50 ml dung dịch NaCl 1M thì nồng độ ion Na+ có trong dung dịch tạo thành Câu3: Giá trị pH của dung dịch HCl 0,1M Câu4: Trên chai hóa chất có ghi: dung dịch HCl 0,1M. Hỏi trong chai hóa chất đó chứa ion nào sau đây? (không kể sự điện li của H2O). Câu 5: Để trung hòa 20 ml dung dịch HCl 0,1M cần 10 ml dung dịch NaOH nồng độ x mol/l. Giá trị của x Câu 6: Cho m gam NaOH vào H2O để được 2 lít dung dịch NaOH có pH=12. Giá trị của m Câu 7: Trộn lẫn 250 ml dung dịch KOH 0,03M với 250 ml dung dịch HCl 0,01M được 500 ml dung dịch Y. Dung dịch Y có pH Câu 8:
Câu 3 :
\(pH=-log\left[H^+\right]=-log\left(0.1\right)=1\)
Câu 4 :
Chứa các ion : H+ , Cl-
Câu 5 :
\(n_{NaOH}=n_{HCl}=0.02\cdot0.1=0.002\left(mol\right)\)
\(\Rightarrow x=\dfrac{0.002}{0.01}=0.2\left(M\right)\)
Đúng 1
Bình luận (0)
Câu 1 :
Bảo toàn điện tích :
\(n_{SO_4^{2-}}=\dfrac{0.2\cdot2+0.1-0.05}{2}=0.225\left(mol\right)\)
\(m_{Muối}=0.2\cdot64+0.1\cdot39+0.05\cdot35.5+0.225\cdot96=40.075\left(g\right)\)
Câu 2 :
\(\left[Na^+\right]=\dfrac{0.15\cdot0.5\cdot2+0.05\cdot1}{0.15+0.05}=1\left(M\right)\)
Đúng 1
Bình luận (0)
Câu 6 :
\(pH=14+log\left[OH^-\right]=12\)
\(\Rightarrow\left[OH^-\right]=0.01\)
\(n_{NaOH}=n_{OH}=0.01\cdot2=0.02\left(mol\right)\)
\(\Rightarrow m_{NaOH\left(bđ\right)}=0.02\cdot40=0.8\left(g\right)\)
Câu 7 :
\(n_{KOH}=0.25\cdot0.03=0.0075\left(mol\right)\)
\(n_{HCl}=0.25\cdot0.01=0.0025\left(mol\right)\)
\(\Rightarrow n_{KOH\left(dư\right)}=0.0075-0.0025=0.005\left(mol\right)\)
\(\left[OH^-\right]=\dfrac{0.005}{0.25+0.25}=0.01\)
\(pH=14+log\left[OH^-\right]=14+log\left(0.01\right)=12\)
Đúng 1
Bình luận (0)
Xem thêm câu trả lời
Trong dung dịch X chứa các ion: Mg2+, Ca2+, Na+ (0,05 mol), Cl- (0,2 mol), NO3- (0,3 mol). Thêm từ từ đến hết V ml dung dịch Na3PO4 1M vào dung dịch X cho đến khi lượng kết thu được lớn nhất. Giá trị của V là A. 300 ml B. 150 ml C. 225 ml D. 130 ml
Đọc tiếp
Trong dung dịch X chứa các ion: Mg2+, Ca2+, Na+ (0,05 mol), Cl- (0,2 mol), NO3- (0,3 mol). Thêm từ từ đến hết V ml dung dịch Na3PO4 1M vào dung dịch X cho đến khi lượng kết thu được lớn nhất. Giá trị của V là
A. 300 ml
B. 150 ml
C. 225 ml
D. 130 ml
Đáp án B
Đặt công thức chung của Ca và Mg là M.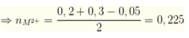
![]()
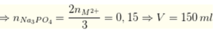
Đúng 0
Bình luận (0)
Có 100ml dung dịch S chứa các ion: H+ (x mol), Cl-(0,1 mol), SO42-(0,15 mol) và có 200ml dung dịch B chứa các ion: Na+ (0,2 mol), Ba2+ (0,2 mol), và OH- (y mol).a) Xác định x,y.b) Để trung hòa 100ml dung dịch A trên phải cần bao nhiêu ml dung dịch B?c) Trộn 100ml dung dịch A với 100ml dung dịch B sẽ thu được bao nhiêu gam muối không tan?
Đọc tiếp
Có 100ml dung dịch S chứa các ion: H+ (x mol), Cl-(0,1 mol), SO42-(0,15 mol) và có 200ml dung dịch B chứa các ion: Na+ (0,2 mol), Ba2+ (0,2 mol), và OH- (y mol).
a) Xác định x,y.
b) Để trung hòa 100ml dung dịch A trên phải cần bao nhiêu ml dung dịch B?
c) Trộn 100ml dung dịch A với 100ml dung dịch B sẽ thu được bao nhiêu gam muối không tan?
Một dung dịch Y có chứa các ion: Mg2+ (0,05 mol), K+ (0,15 mol), NO3- (0,1 mol), và SO42- (x mol). Khối lượng chất tan có trong dung dịch Y là Cho 200 ml dung dịch X chứa các ion NH4+ (0,5M), K+ (0,1M), SO42- (0,25M), Cl- (aM). Biết rằng dung dịch X được điều chế bằng cách hoà tan 2 muối vào nước. Khối lượng của 2 muối được lấy làgiải dùm mình cần gấp tối nay lúc 10h giúp dùm mình cần gấp
Đọc tiếp
Một dung dịch Y có chứa các ion: Mg2+ (0,05 mol), K+ (0,15 mol), NO3- (0,1 mol), và SO42- (x mol). Khối lượng chất tan có trong dung dịch Y là
Cho 200 ml dung dịch X chứa các ion NH4+ (0,5M), K+ (0,1M), SO42- (0,25M), Cl- (aM). Biết rằng dung dịch X được điều chế bằng cách hoà tan 2 muối vào nước. Khối lượng của 2 muối được lấy là
giải dùm mình cần gấp tối nay lúc 10h giúp dùm mình cần gấp
Bài : Tính số mol của các ion trong các dung dịch sau: A)200 ml dung dịch Al2(SO4)3 28,5% (có d = 1,2 g/ml). B)100 ml dung dịch chứa hỗn hợp HCl 3M và HNO3 1M.
a) \(m_{ddAl_2\left(SO_4\right)_3}=200\cdot1,2=240\left(g\right)\)
\(\Rightarrow m_{Al_2\left(SO_4\right)_3}=\dfrac{240\cdot28,5}{100}=68,4\left(g\right)\)
\(\Rightarrow n_{Al_2\left(SO_4\right)_3}=0,2mol\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Al^{3+}}=2n_{Al_2\left(SO_4\right)_3}=0,4mol\\n_{SO^{2-}_4}=0,6mol\end{matrix}\right.\)
b) \(n_{HCl}=0,1\cdot3=0,3mol\) \(\Rightarrow n_{Cl^-}=0,3mol\)
\(n_{HNO_3}=0,1\cdot1=0,1mol\) \(\Rightarrow n_{NO^-_3}=0,1mol\)
\(\Sigma n_{H^+}=n_{HCl}+n_{HNO_3}=0,3+0,1=0,4mol\)
Đúng 1
Bình luận (0)
Tính nồng độ mol/lit của các ion trong dung dịch sau: 200 ml dung dịch chứa 49 gam H2SO4?
\(n_{H^+}=2.n_{H_2SO_4}=\dfrac{2.49}{98}=1\left(mol\right)\Rightarrow\left[H^+\right]=\dfrac{1}{0,2}=5M\)
\(n_{SO_4^{2-}}=n_{H_2SO_4}=\dfrac{49}{98}=0,5\left(mol\right)\Rightarrow\left[SO_4^{2-}\right]=\dfrac{0,5}{0,2}=2,5M\)
Đúng 0
Bình luận (0)
Tính nồng độ mol/l các ion trong mỗi dd sau:
a) 100ml dd chứa 4,26 gam Al(NO3)3.
b) Tính nồng độ mol của ion Na+ trong dung dịch chứa NaNO3 0,1M,
Na2SO4 0,02M và NaCl 0,3M.
c) Dung dịch H2SO4 15% ( d= 1,1g/ml)
a) Ta có: \(n_{Al\left(NO_3\right)_3}=\dfrac{4,26}{213}=0,02\left(mol\right)\) \(\Rightarrow\left\{{}\begin{matrix}n_{Al^+}=0,02\left(mol\right)\\n_{NO_3^-}=0,06\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\left[Al^+\right]=\dfrac{0,02}{0,1}=0,2\left(M\right)\\\left[NO_3^-\right]=\dfrac{0,06}{0,1}=0,6\left(M\right)\end{matrix}\right.\)
b) Ta có: \(\left[Na^+\right]=0,1+0,02\cdot2+0,3=0,304\left(M\right)\)
c) Bạn xem lại đề !!
Đúng 0
Bình luận (0)
Dung dịch A có chứa 5 ion:
Mg
2
+
,
Ba
2
+
,
Ca
2
+
và 0,1 mol Cl- và 0,2 mol
NO
3
-
. Thêm dần V ml dung dịch
K
2
CO
3
...
Đọc tiếp
Dung dịch A có chứa 5 ion: Mg 2 + , Ba 2 + , Ca 2 + và 0,1 mol Cl- và 0,2 mol NO 3 - . Thêm dần V ml dung dịch K 2 CO 3 1M vào dung dịch A đến khi thu được lượng kết tủa lớn nhất. V có giá trị là
A. 150 ml.
B. 300 ml.
C. 200 ml.
D. 250 ml.
Một dung dịch có chứa các ion: Na+ (0,2 mol), Mg2+ (0,1 mol), Ca2+ (0,05 mol), NO3- (0,15 mol) và Cl- (x mol). Giá trị của x là A. 0,35 B. 0,3 C. 0.15 D. 0,2
Đọc tiếp
Một dung dịch có chứa các ion: Na+ (0,2 mol), Mg2+ (0,1 mol), Ca2+ (0,05 mol), NO3- (0,15 mol) và Cl- (x mol). Giá trị của x là
A. 0,35
B. 0,3
C. 0.15
D. 0,2
Chọn A
Bảo toàn điện tích ⇒ 0,2.1 + 0,1.2 + 0,05.2 = 0,15.1 + 1.x x = 0,35
Đúng 0
Bình luận (0)



















