Propyne phản ứng với nước trong điều kiện tương tự như acetylene. Viết phương trình phản ứng minh hoạ.

Những câu hỏi liên quan
Trong những hiđrocacbon sau, những chất nào có phản ứng thế với brom ? Có phản ứng cộng với brom ? Viết phương trình hoá học minh hoạ và ghi rõ điều kiện phản ứng :
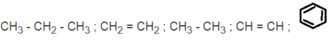
Chất có phản ứng thế với brom khi chiếu sáng . CH 3 - CH 2 - CH 3 ; CH 3 - CH 3
- Phản ứng thế với brom khi có mặt bột sắt và đun nóng : C 6 H 6 (benzen).
- Chất có phản ứng cộng với brom (trong dung dịch): CH 2 = CH 2 ; CH ≡CH.
Các chất tham gia phản ứng thế brom:
CH 3 - CH 2 - CH 3 + Br 2 → as CH 3 - CHCl - CH 3 (spc) + CH 3 - CH 2 - CH 2 Cl (spp) + HCl
CH 3 - CH 3 + Br 2 → as CH 3 - CH 2 Br + HBr
C 6 H 6 + Br 2 → bột Fe , t ° C 6 H 5 Br + HBr
Phản ứng cộng:
C 2 H 2 + 2 Br 2 → C 2 H 2 Br 4
Đúng 0
Bình luận (0)
Tương tự như natri, các kim loại kali K và canxi Ca cũng tác dụng được với nước tạo thành bazơ tan và giải phóng khí hiđro.
a) Hãy viết các phương trình phản ứng xảy ra.
b) Các phản ứng hóa học trên thuộc loại phản ứng hóa học nào?
a) Phương trình phản ứng xảy ra là:
2K + 2H2O → 2KOH + H2.
Ca + 2H2O → Ca(OH)2 + H2.
b) Các phản ứng trên thuộc loại phản ứng oxi hóa – khử.
Đúng 0
Bình luận (0)
Có các phát biểu sau đây về mức phản ứng: (1). Mức phản ứng là tập hợp các kiểu hình của cùng một kiểu gen tương ứng với điều kiện môi trường. (2). Mức phản ứng là kết quả sự tự điều chỉnh của kiểu hình trong giới hạn tương ứng với môi trường. (3). Tính trạng số lượng có mức phản ứng rộng, tính trạng chất lượng có mức phản ứng hẹp. (4). Mức phản ứng do môi trường quy định, không di truyền. Phương án trả lời đúng là: A. (1) sai, (2) đúng), (3) sai, (4) đúng B. (1) sai), 2 (đúng), (3) sai), (4)...
Đọc tiếp
Có các phát biểu sau đây về mức phản ứng:
(1). Mức phản ứng là tập hợp các kiểu hình của cùng một kiểu gen tương ứng với điều kiện môi trường.
(2). Mức phản ứng là kết quả sự tự điều chỉnh của kiểu hình trong giới hạn tương ứng với môi trường.
(3). Tính trạng số lượng có mức phản ứng rộng, tính trạng chất lượng có mức phản ứng hẹp.
(4). Mức phản ứng do môi trường quy định, không di truyền.
Phương án trả lời đúng là:
A. (1) sai, (2) đúng), (3) sai, (4) đúng
B. (1) sai), 2 (đúng), (3) sai), (4) sai
C. (1) đúng, (2) sai), (3) đúng), (4) sai
D. (1) đúng, (2) sai, (3) sai, (4) đúng
Dạng I: Viết PTHH của phản ứngBài 1: 1) Viết PTHH của phản ứng xảy ra (ghi rõ điều kiện phản ứng nếu có) khi cho H2 lần lượt tác dụng với các chất: O2, PbO, Fe2O3, Fe3O4, CuO.2) Cacbon oxit (CO) có tính chất tương tự như H2 (tính khử). Viết PTHH của phản ứng xảy ra (ghi điều kiện phản ứng nếu có) khi cho CO lần lượt tác dụng với: O2; CuO; Fe3O4?Bài 2: Xác định các chất A; B và viết PTHH (ghi rõ điều kiện phản ứng) thực hiện chuyển đổi hóa học sau:H2O A B Fe3O4Dạng II: Nhận biết – Tách và tinh...
Đọc tiếp
Dạng I: Viết PTHH của phản ứng
Bài 1: 1) Viết PTHH của phản ứng xảy ra (ghi rõ điều kiện phản ứng nếu có) khi cho H2 lần lượt tác dụng với các chất: O2, PbO, Fe2O3, Fe3O4, CuO.
2) Cacbon oxit (CO) có tính chất tương tự như H2 (tính khử). Viết PTHH của phản ứng xảy ra (ghi điều kiện phản ứng nếu có) khi cho CO lần lượt tác dụng với: O2; CuO; Fe3O4?
Bài 2: Xác định các chất A; B và viết PTHH (ghi rõ điều kiện phản ứng) thực hiện chuyển đổi hóa học sau:
H2O ![]() A
A ![]() B
B ![]() Fe3O4
Fe3O4
Dạng II: Nhận biết – Tách và tinh chế chất:
Bài 3: Có 4 bình khí A, B, C, D mỗi bình chứa 1 trong các chất khí sau: khí cacbonic, khí oxi, khí hiđro, không khí. Biết rằng:
- Khí trong bình A làm đục nước vôi trong.
- Hỗn hợp của khí trong bình B và D là hỗn hợp nổ.
- Khí D làm CuO (màu đen) chuyển sang màu đỏ khi nung nóng.
Xác định chất khí đựng trong các bình A, B, C, D và viết PTHH của các phản ứng xảy ra?
Bài 4: Có hỗn hợp khí gồm H2, CO2.
1) Trình bày cách để loại bỏ CO2 ra khỏi hỗn hợp? Viết PTHH của phản ứng xảy ra?
2) Tách riêng H2 và CO2 ra khỏi hỗn hợp trên?
Dạng III: Phương pháp bảo toàn khối lượng và bảo toàn nguyên tố
Bài 5: Dẫn luống khí H2 dư qua ống sứ đựng 24 gam hỗn hợp gồm CuO và Fe2O3 (![]() ) nung nóng. Sau khi phản ứng xảy ra hoàn toàn thu được m gam chất rắn.
) nung nóng. Sau khi phản ứng xảy ra hoàn toàn thu được m gam chất rắn.
1) Viết PTHH của phản ứng xảy ra?
2) Không dựa vào PTHH hãy:
a) Tính thể tích khí H2 (đktc) đã tham gia phản ứng?
b) Tính m?
Bài 6: Dẫn hỗn hợp X gồm H2 và CO từ từ đến dư qua ống sứ đựng 19,6g hỗn hợp A gồm CuO và Fe3O4 (trong đó CuO chiếm 40,82% về khối lượng), sau khi các phản ứng xảy ra hoàn toàn thu được hỗn hợp khí và hơi Y (gồm CO2 và hơi nước). Chất rắn B thu được trong ống sứ khối lượng giảm m gam so với hỗn hợp A ban đầu.
1) Viết PTHH của phản ứng xảy ra?
2) Tính m và khối lượng của hỗn hợp B?
3) Khối lượng của Y nặng hay nhẹ hơn khối lượng hỗn hợp X ban đầu? bao nhiêu gam? Tính tổng thể tích hỗn hợp A đã tham gia phản ứng?
Bài 7: Hỗn hợp X gồm Al; Mg; Zn.
- Cho m gam hỗn hợp X tác dụng hết với dung dịch H2SO4 loãng thấy thoát ra 8,96 lít H2 (đktc).
- Mặt khác, đốt cháy hoàn toàn m gam hỗn hợp X cần dùng vừa đủ V lít O2 (đktc).
1) Viết PTHH của phản ứng xảy ra?
2) Tính V? (Phương pháp ghép ẩn)
Dạng IV: Bài toán: Tính theo PTHH – tăng, giảm khối lượng
Bài 8: Người ta tiến hành thí nghiệm sau:
- Đặt lên 2 đĩa cân (cân Robecvan): Đĩa cân A: cốc đựng dung dịch HCl; đĩa cân B: cốc đựng dung dịch H2SO4 loãng. Cân ở vị trí thăng bằng.
- Thêm vào cốc A một dây Mg có khối lượng 3,6g; thêm vào cốc B lá nhôm có khối lượng 5,4g. Để cho toàn bộ kim loại tan hết.
1) Viết PTHH của các phản ứng xảy ra?
2) So sánh thể tích khí thoát ra ở 2 cốc?
3) Xác định trạng thái của cân sau thí nghiệm? Cần phải thêm nước vào cốc nào? Bao nhiêu gam nước để cân trở lại vị trí thăng bằng?
Bài 9: Người ta tiến hành thí nghiệm sau:
- Đặt lên 2 đĩa cân (cân Robecvan): Đĩa cân A: cốc đựng dung dịch HCl; đĩa cân B: cốc đựng dung dịch H2SO4 loãng. Cân ở vị trí thăng bằng.
- Thêm vào cốc A vài viên Zn có khối lượng a gam; thêm vào cốc B lá nhôm có khối lượng b gam. Sau khi toàn bộ kim loại tan hết, thấy cân vẫn ở vị trí thăng bằng.
1) Viết PTHH của các phản ứng xảy ra
2) Tính a/b?
Dạng V: Bài toán: Xác định thành phần hỗn hợp – Nồng độ dung dịch
Bài 10: Khử hoàn toàn 32g hỗn hợp X gồm CuO và Fe2O3 bằng khí H2 ở nhiệt độ cao. Sau phản ứng thu được 24g hỗn hợp Y gồm 2 kim loại.
1) Viết PTHH của phản ứng xảy ra?
2) Tính thể tích H2 (đktc) đã tham gia phản ứng?
3) Tính thành phần % về khối lượng mỗi oxit trong X?
Bài 11: Cho 6,06g hỗn hợp A gồm Al và Zn tác dụng với 200g dung HCl 6,935%. Sau khi phản ứng xảy ra hoàn toàn thu được dung dịch B và thoát ra 4,032 lít H2 (đktc).
1) Viết PTHH của phản ứng xảy ra?
2) Chứng tỏ rằng, hỗn hợp A tan hết; HCl còn dư.
3) Tính tổng khối lượng muối có trong dung dịch B?
4) Tính thành phần % về khối lượng mỗi kim loại trong A?
5) Tính nồng độ % của các chất trong dung dịch B?
Bài 12: Hoà tan 3,87g hỗn hợp kim loại gồm Mg và Al trong 250 ml dung dịch HCl 2M thu được dung dịch A và khí B.
1) Viết PTHH của phản ứng xảy ra?
2) Chứng minh rằng sau phản ứng với Mg và Al thì axit vẫn còn dư.
3) Nếu thể tích khí B thu được là 4,368 lit (đktc):
a) Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu?
b) Tính nồng độ mol của các chất trong dung dịch A? Coi thể tích dung dịch không thay đổi trong quá trình phản ứng?
Bài 13: Khử hoàn toàn 24g hỗn hợp X gồm CuO và Fe2O3 bằng V lít (đktc) hỗn hợp khí A gồm CO và H2 (vừa đủ). Sau phản ứng thu được m gam hỗn hợp Y (gồm 2 kim loại); hỗn hợp khí và hơi B (CO2; hơi nước) nặng hơn hỗn hợp A ban đầu 6,4g.
1) Viết PTHH của các phản ứng xảy ra?
2) Tính m và V?
3) Tính khối lượng mỗi oxit trong X?
Dạng VI: Bài toán: Xác định CTHH của chất
Bài 14: Hoà tan hoàn 18,4g kim loại M (hoá trị II) và N (hoá trị III) trong dung dịch HCl thu được dung dịch Q và 11,2 lít H2 (đktc). Cô cạn dung dịch Q thu được m gam muối khan.
1) Tính m?
2) Xác định tên 2 kim loại M, N. Biết rằng trong hỗn hợp tỉ lệ số mol nM : nN = 1: 1và 2MN < MM < 3MN
Bài 15: Khi lấy 6,72 lít H2 ở trên khử vừa đủ 19,6 gam hỗn hợp CuO và FexOy tạo ra hỗn hợp kim loại C, ngâm hỗn hợp kim loại C trong dung dịch HCl dư thu được 3,36 lít H2. Biết: các thể tích đo ở điều kiện tiêu chuẩn; Cu không tác dụng với dung dịch HCl.
1) Tính khối lượng hỗn hợp C.
2) Xác định công thức oxit sắt?
Bài 16: Cho 11,6 gam MxOy vào ống sứ, nung nóng và dẫn 8,96 lít khí CO (đktc) đi qua. Khi phản ứng xảy ra hoàn toàn thu được chất rắn và hỗn hợp khí Y có tỉ khối so với khí oxi là 1,125. Tìm công thức oxit.
Bài 17: Khử hoàn toàn 3,48g một oxit kim loại RxOy cần dùng 1,344 lít H2. Toàn bộ lượng kim loại thu được cho tác dụng với dung dịch HCl dư thu được 1,008 lít khí. Các thể tích khí đo ở đktc. Xác định kim loại M và oxit của nó?
bài 1: 1) 2H2+ O2 -to-> 2H2O
PbO + H2 -to-> Pb + H2O
Fe2O3 + 3H2 -to-> 2Fe + 3H2O
Fe3O4 + 2H2 -to-> 3Fe + 2H2O
CuO + H2 -to-> Cu + H2O
b) O2 + 2CO -to-> 2CO2
CuO + CO -to-> Cu + CO2
Fe3O4 + 4CO -to-> 3Fe + 4CO2
Đúng 0
Bình luận (0)
bài 3
khí trong bình A là CO2 pthh CO2 + 2Ca(OH) --> 2CaCO3 + H2O
khí B là O2 khí D là H2 pthh 2H2 + O2 --> 2H2O
CuO +H2 -to-> Cu + H2O
khí C là không khí
Đúng 0
Bình luận (0)
Trong phòng thí nghiệm người ta lắp đặt bộ dụng cụ điều chế khí X theo phương pháp dời chỗ nước như hình bên. Hãy lựa chọn 2 cặp chất tương ứng với (1) và (2) phù hợp để có thể điều chế được khí X. Viết phương trình phản ứng xảy ra. Tại sao khí X có thể thu được bằng phương pháp đó
Đọc tiếp
Trong phòng thí nghiệm người ta lắp đặt bộ dụng cụ điều chế khí X theo phương pháp dời chỗ nước như hình bên.
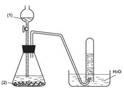
Hãy lựa chọn 2 cặp chất tương ứng với (1) và (2) phù hợp để có thể điều chế được khí X. Viết phương trình phản ứng xảy ra. Tại sao khí X có thể thu được bằng phương pháp đó
Viết các phương trình hoá học dưới dạng CTCT thu gọn của các phản ứng sau: (ghi rõ điều kiện phản ứng nếu có)
a) Phản ứng của axit focmic với Al.
b) Phản ứng đime hóa axetilen.
c) Phản ứng chứng minh ảnh hưởng của nhóm –OH đến gốc –C6H5 trong phân tử phenol.
d) Phản ứng oxi hóa propan-1-ol bằng CuO.
a/ 3HCOOH + Al \(\rightarrow\) (HCOO)3Al + \(\frac{3}{2}\)H2
b/ 2CH\(\equiv\)CH \(\underrightarrow{CuCl\text{/}NH4Cl,t}\) CH2\(=\)CH\(-\)C \(\equiv\)CH
c/ + 3Br2 \(\rightarrow\) C6H2OHBr3 + 3HBr
d/ CH3\(-\)CH2CH2\(-\)OH + CuO \(\underrightarrow{t}\) CH3\(-\)CH2CHO +Cu + H2O
Đúng 0
Bình luận (0)
trời fan sơn tùng ak tui là anti fan sơn tùng nè hihi
Đúng 0
Bình luận (0)
trời ??? anti , bn đùa à????
Đúng 0
Bình luận (1)
Xem thêm câu trả lời
Bài tập 1: Viết phương trình hóa học biểu diễn phản ứng của hiđro với các chất: O2, Fe2O3, Fe3O4, PbO. Ghi rõ điều kiện phản ứng. Giải thích và cho biết mỗi phản ứng trên thuộc loại phản ứng gì ? *Bài tập 2: Dẫn 2,24 lít khí H2 (đktc) vào một ống có chứa 12 gam CuO đã nung nóng tới nhiệt độ thích hợp. Kết thúc phản ứng trong ống nghiệm còn lại a gam chất rắn. a/ Viết phương trình phản ứng. b/ Tính khối lượng nước tạo thành sau phản ứng. c/ Tính a ? GIUP MIK NHE
Đọc tiếp
Bài tập 1: Viết phương trình hóa học biểu diễn phản ứng của hiđro với các chất: O2, Fe2O3, Fe3O4, PbO. Ghi rõ điều kiện phản ứng. Giải thích và cho biết mỗi phản ứng trên thuộc loại phản ứng gì ? *
Bài tập 2: Dẫn 2,24 lít khí H2 (đktc) vào một ống có chứa 12 gam CuO đã nung nóng tới nhiệt độ thích hợp. Kết thúc phản ứng trong ống nghiệm còn lại a gam chất rắn. a/ Viết phương trình phản ứng. b/ Tính khối lượng nước tạo thành sau phản ứng. c/ Tính a ?
GIUP MIK NHE
So sánh tính chất hoá học của etylbenzen với stiren, viết phương trình hoá học của phản ứng để minh hoạ.
a. Giống nhau: đều phản ứng thế
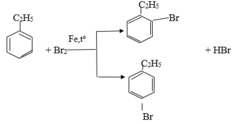
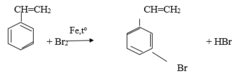
b. Khác nhau:
Etylbenzen có tính chất giống ankan
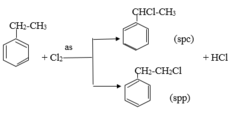
Stiren có tính chất giống anken
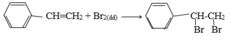
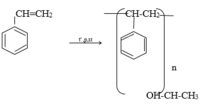
Đúng 0
Bình luận (0)
5,4 g Al tác dụng với O2 .Viết phương trình phản ứng .Tính khối lượng sản phẩm.
11,2 g Fe tác dụng với không khí( điều kiện chuẩn )tạo sắt từ oxit .Viết phương trình phản ứng tính thể tích của không khí (điều kiện chuẩn), khối lượng sản phẩm. Tính m Fe và O2 cần
\(n_{Al}=\dfrac{5.4}{27}=0.2\left(mol\right)\)
\(4Al+3O_2\underrightarrow{^{^{t^0}}}2Al_2O_3\)
Ta có :
\(n_{Al_2O_3}=\dfrac{0.2\cdot2}{4}=0.1\left(mol\right)\)
\(m_{Al_2O_3}=0.1\cdot102=10.2\left(g\right)\)
Đúng 3
Bình luận (0)
\(n_{Fe}=\dfrac{11.2}{56}=0.2\left(mol\right)\)
\(3Fe+2O_2\underrightarrow{^{^{t^0}}}Fe_3O_4\)
\(0.2.......\dfrac{2}{15}.....\dfrac{1}{15}\)
\(V_{O_2}=\dfrac{2}{15}\cdot22.4=2.98\left(l\right)\)
\(m_{Fe_3O_4}=\dfrac{1}{15}\cdot232=15.46\left(g\right)\)
Đúng 2
Bình luận (0)
















