so sánh hàm lượng chủa o trong hợp chất MFe(NO3)3

Những câu hỏi liên quan
Mọi ng xin giúp càng nhanh càng tốt !
C1 : Tính các % của các nguyên tố trong trường hợp chất sau
CUSO4, CO2, CO
C2 : Hãy cho biết trong các công thức sau N2O, No, N2O3, No2, N2O5 ( Hợp chất nào có hàm lượng cao nhất )
C3 : Hãy xác định CTHH của HCA gồm Fe và O
( % mfe = 70% ; %O=30% )
C1:
%mCu(CuSO4)=\(\frac{64}{160}\).100%=40%
%mS(CuSO4)=\(\frac{32}{160}\).100%=20%
%mO(CuSO4)=100%-40%-20%=40%
%mC(CO2)=\(\frac{12}{44}\).100%=27,27%
%mO(CO2)=100%-27,27%=72,73%
%mC(CO)=\(\frac{12}{28}\).100%=42,86%
%mO(CO)=100%-42,86%=57,14%
C2:
%mN(N2O)=\(\frac{28}{44}\).100%=63,64% (1)
%mN(NO)=\(\frac{14}{30}\),100%=46,67% (2)
%mN(N2O3)=\(\frac{28}{76}\).100%=36,84% (3)
%mN(N2O5)=\(\frac{28}{108}\).100%=25,93% (4)
Từ (1),(2),(3)và(4) ta thấy hàm lượng Nitơ trong N2O cao nhất (63,64%)
C3:
Gọi CTHH của hợp chất A là FexOy
Ta có :
x : y = \(\frac{70\%}{56}\) : \(\frac{30\%}{16}\)
= 1,25 : 1,875
= 2 : 3
=> Fe2O3
Đúng 0
Bình luận (0)
Xác định CTHH của
a) Oxit sắt có mFe : mo = 21:8
b) Hợp chất có % Ca : %C : %O = 10:3:12 theo khối lượng
c) Tỉ lệ khối lượng mMg : mC : mO = 2:1:4
Tìm số nguyên tử của mỗi nguyên tố trong 8,4g hợp chất trên
b)
%Ca : %C : %O = 10 :3 : 12
=> 40.nCa : 12.nC : 16.nO = 10 : 3 : 12
=> nCa : nC : nO = 1 : 1 : 3
=> CTHH: CaCO3
c)
24.nMg : 12.nC : 16.nO = 2:1:4
=> nMg : nC : nO = 1 : 1 : 3
=> CTHH: MgCO3
\(n_{MgCO_3}=\dfrac{8,4}{84}=0,1\left(mol\right)\)
=> Số nguyên tử Mg = 0,1.1.6.1023 = 0,6.1023
=> Số nguyên tử C = 0,1.1.6.1023 = 0,6.1023
=> Số nguyên tử O = 0,1.3.6.1023 = 1,8.1023
Đúng 3
Bình luận (0)
a: Theo đề, ta có:
\(\dfrac{n_{Fe}\cdot56}{n_O\cdot16}=\dfrac{21}{8}\Leftrightarrow\dfrac{n_{Fe}}{n_O}=\dfrac{3}{4}\)
Vậy: Công thức là \(Fe_3O_4\)
Đúng 2
Bình luận (0)
1 Nếu hàm lượng phần trăm của 1 kim loại trong hợp chất của kim loại với nhóm (CO3) LÀ 40% thì hàm lượng % của kim loại đó trong hợp chất của nó với nhóm (PO4) là bao nhiêu?
2 Có các hợp chất của sắt FeO; Fe2O3; Fe3O4. Nếu hàm lượng của sắt trong hợp chất là 72,41% theo khối lượng thì đó là hợp chất nào?
1. CO3 = 12+ 16.3 = 60g
kim loại đó mkl = 40% = 40g = Ca
PO4 = 31 + 16.4 = 95
% Ca = 40/(95+40).100% = 29,6%
2. % Fe trong fe0 = 56/(56+16) = 77,41%
vay nó là FeO
Đúng 0
Bình luận (2)
Làm thế nào để:
-Tính được số nguyên tử, số phân tử của các chất trong một mẫu chất có khối lượng, thể tích cho trước:
-Tính được thể tích chủa một lượng khí(mà ko phải đo)
-So sánh được khối lượng của cùng một thể tích của 2 khí ở cùng điều kiện về nhiệt độ, áp suất(mà ko phải cân)
a, tính số mol rồi lấy số mol.6.1023
b, V=n.22,4
c d\(\frac{A}{B}\) = \(\frac{M_A}{M_B}\)
Đúng 0
Bình luận (0)
-Lấy số mol nhân cho 6.1023
-Lấy số mol nhân cho 22,4(ở đktc)
-\(d_{A/B}=\dfrac{M_A}{M_B}\)
Chúc bạn học tốt![]()
Đúng 0
Bình luận (0)
Bài 2. Một hợp chất X gồm các nguyên tố Fe, O, S có tỉ lệ khối lượng mFe : mO : mS = 7: 12 : 6. Hãy xác định:
a) Công thức hóa học và gọi tên của hợp chất X biết khối lượng mol của X là 400 g/mol.
b) Số mol nguyên tử của mỗi nguyên tố có trong 60 gam hợp chất X.
a)
Gọi CTHH là $Fe_xS_yO_z$
Ta có :
\(\dfrac{56x}{7}=\dfrac{32y}{6}=\dfrac{16z}{12}=\dfrac{400}{7+6+12}\)
Suy ra x = 2 ; y = 3; z = 12
Vậy CTHH là $Fe_2(SO_4)_3$ :Sắt III sunfat
b)
$n_X = \dfrac{60}{400} =0,15(mol)$
Số nguyên tử Fe = 0,15.2.6.1023 = 1,8.1023 nguyên tử
Số nguyên tử S = 0,15.3.6.1023 = 2,7.1023 nguyên tử
Số nguyên tử O = 0,15.12.6.1023 = 10,8.1023 nguyên tử
Đúng 1
Bình luận (0)
a, Xác định Thành phần % theo khối lượng các nguyên tố có trong hợp chất SO3
b, Xác định công thức hóa họng hợp chất tạo bởi 40% S, 60% O, khối lượng của mol hợp chất là 80 gam. So sánh chất khí trên nặng hay nhẹ ko khi bao nhiêu lần ?
a) mso3 = 32 + 48 = 80g
%ms = 32/80.100% = 40%
% mo = 48/80 .100% = 60%
b) nhìn vào a) ta thấy ngay cthh của chất này là SO3
So với kk = 80/29 = 2,76 (lần) nặng hơn kk
Đúng 0
Bình luận (0)
1) Cho hỗn hợp khí A gồm KNO3 và Cu(NO3)2 vào lò nung đến khối lượng không đổi được 12,5 gam chất rắn và hỗn hợp khí B có tỉ khối so với H2 là 18,8. Tính khối lượng từng chất trong hỗn hợp A và thể tích (ở đktc) của từng khí trong B.
2) Nung 44g hỗn hợp X gồm Cu và Cu(NO3)2 trong bình khí đến khi muối nitrat bị phản hủy hoàn toàn được chất rắn Y. Hoà tan hết Y với lượng vừa đủ 600ml dung dịch H2SO4 0,5M. Tính khối lượng mỗi chất trong X.
Đọc tiếp
1) Cho hỗn hợp khí A gồm KNO3 và Cu(NO3)2 vào lò nung đến khối lượng không đổi được 12,5 gam chất rắn và hỗn hợp khí B có tỉ khối so với H2 là 18,8. Tính khối lượng từng chất trong hỗn hợp A và thể tích (ở đktc) của từng khí trong B.
2) Nung 44g hỗn hợp X gồm Cu và Cu(NO3)2 trong bình khí đến khi muối nitrat bị phản hủy hoàn toàn được chất rắn Y. Hoà tan hết Y với lượng vừa đủ 600ml dung dịch H2SO4 0,5M. Tính khối lượng mỗi chất trong X.
tính:
1.khối lượng hợp chất Ba(NO3)2 có chứa 14 gam N.
2.khối lượng hợp chất Ca(OH)2 có chứa 2 gam Ca.
3.khối lượng hợp chất Fe(NO3)3 có chứa 11,2 gam Fe.
1) Số mol của nito
nN = nBa(NO3)2 = \(\dfrac{m_N}{M_N}=\dfrac{14}{14}=1\left(mol\right)\)
Khối lượng của bari nitrat
mBa(NO3)2 = nBa(NO3)2 . MBa(NO3)2
= 1 . 261
= 261 (g)
2) Số mol của canxi
nCa= nCa(OH)2= \(\dfrac{m_{Ca}}{M_{Ca}}=\dfrac{2}{40}=0,05\left(mol\right)\)
Khối lượng của canxi hidroxit
mCa(OH)2= nCa(OH)2. MCa(OH)2
= 0,05 . 74
= 3,7 (g)
3) Số mol của sắt
nFe= nFe(NO3)2 = \(\dfrac{m_{Fe}}{M_{Fe}}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
Khối lượng của sắt (II) nitrat
mFe(NO3)2= nFe(NO3)2. MFe(NO3)2
= 0,2 . 180
= 36 (g)
Chúc bạn học tốt
Đúng 1
Bình luận (1)
Ba nguyên tố cơ bản là chất dinh dưỡng cho thực vật, đó là : nitơ (N), photpho (P), kali (K).Hợp chất của nitơ làm tăng trưởng lá cây và tinh bột trong ngũ cốc. Hợp chất của photpho kích thích bộ rễ phát triển và hoa quả chín sớm.Hợp chất của kali tăng cường sức chịu đựng cho thực vật.Dưới đây là hàm lượng của N, P, K có trong 4 mẫu phân bón kép NPK :Dùng số liệu của bảng, hãy :Vẽ biểu đồ so sánh hàm lượne của nitơ có trong 4 loại phân bón.
Đọc tiếp
Ba nguyên tố cơ bản là chất dinh dưỡng cho thực vật, đó là : nitơ (N), photpho (P), kali (K).
Hợp chất của nitơ làm tăng trưởng lá cây và tinh bột trong ngũ cốc. Hợp chất của photpho kích thích bộ rễ phát triển và hoa quả chín sớm.
Hợp chất của kali tăng cường sức chịu đựng cho thực vật.
Dưới đây là hàm lượng của N, P, K có trong 4 mẫu phân bón kép NPK :
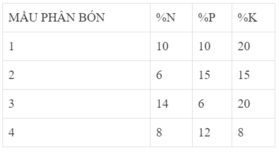
Dùng số liệu của bảng, hãy :
Vẽ biểu đồ so sánh hàm lượne của nitơ có trong 4 loại phân bón.