Cho 22g hỗn hợp al ,fe phản ứng hoàn toàn với H2SO4 thu được 20.16 lít SO2 sản phẩm khử duy nhất ở dktc và dung dịch A a) tính khối lượng của mỗi kim loại trong hỗn hợp b) cô cạn dung dịch A thì thu được bao nhiêu gam muối khan

Những câu hỏi liên quan
Hoà tan hoàn toàn 16,2g hỗn hợp X gồm Cu và Fe bằng lượng dư dung dịch h2so4 đặc nóng thu được dung dịch Y và 8,96 lít khí so2 ( sản phẩm khử duy nhất,đo ở đktc)
a. Tính % theo khối lượng mỗi kim loại trong hỗn hợp X
b. Nếu đem 22g hỗn hợp X nói trên cho tác dụng với lượng dư dung dịch h2so4 loãng thì thể tích khí thu được (đo ở đktc) là bao nhiêu lít ( giả sử hỗn hợp X được trộn đều)
Giúp vs ạ
Đọc tiếp
Hoà tan hoàn toàn 16,2g hỗn hợp X gồm Cu và Fe bằng lượng dư dung dịch h2so4 đặc nóng thu được dung dịch Y và 8,96 lít khí so2 ( sản phẩm khử duy nhất,đo ở đktc) a. Tính % theo khối lượng mỗi kim loại trong hỗn hợp X b. Nếu đem 22g hỗn hợp X nói trên cho tác dụng với lượng dư dung dịch h2so4 loãng thì thể tích khí thu được (đo ở đktc) là bao nhiêu lít ( giả sử hỗn hợp X được trộn đều) Giúp vs ạ
\(n_{Cu}=a\left(mol\right),n_{Fe}=b\left(mol\right)\)
\(m_X=64a+56b=16.2\left(g\right)\left(1\right)\)
\(n_{SO_2}=\dfrac{8.96}{22.4}=0.4\left(mol\right)\)
Bảo toàn e :
\(2a+3b=0.4\cdot2=0.8\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.0475,b=0.235\)
\(\%Cu=\dfrac{0.0475\cdot64}{16.2}\cdot100\%=18.76\%\)
\(\%Fe=81.24\%\)
\(b.\)
\(\dfrac{a}{b}=\dfrac{0.0475}{0.235}=\dfrac{19}{94}\)
\(\Rightarrow n_{Cu}=19x\left(mol\right),n_{Fe}=94x\left(mol\right)\)
\(m_X=19x\cdot64+94x\cdot56=22\left(g\right)\)
\(\Rightarrow x=\dfrac{11}{3240}\)
\(n_{H_2}=n_{Fe}=\dfrac{11}{3240}\cdot94=\dfrac{517}{1620}\left(mol\right)\)
\(V_{H_2}=7.15\left(l\right)\)
Đúng 1
Bình luận (0)
Câu 1. Cho 11 g hỗn hợp Al, Fe phản ứng hoàn toàn với lượng dư dung dịch H,SO4 đặc nóng thu được 11,1555 L SO2 (sản phẩm khử duy nhất, ở đkc ) và dung dịch A. Tính % theo khối lượng của mỗi kim loại trong hỗn hợp.
Ta có: 27nAl + 56nFe = 11 (1)
\(n_{SO_2}=0,45\left(mol\right)\)
BT e, có: \(3n_{Al}+3n_{Fe}=2n_{SO_2}=0,9\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Al}=0,2\left(mol\right)\\n_{Fe}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,2.27}{11}.100\%\approx49,09\%\\\%m_{Fe}\approx50,91\%\end{matrix}\right.\)
Đúng 2
Bình luận (0)
Cho 11g hỗn hợp Al, Fe phản ứng hoàn toàn với H2SO4 đặc nóng dư, thu được 10,08 lít SO2 sản phẩm khử duy nhất ở đktc và đúng dịch A. a. Tính % theo khối lượng của mỗi kim loại trong hỗn hợp. b. Tính khối lượng dd H2SO4 đã dùng biết dd H2SO4 có nồng độ 98% và đã dùng dư 20% so lượng cần thiết đểu phản ứng.
Bài 6. Hỗn hợp A gồm Fe, Mg, Al (khối lượng Mg bằng khối lượng Fe). Hòa tan hoàn toàn 16,14 gam hỗn hợp A trong dung dịch H2SO4 đặc, nóng dư thì thu được 13,664 lít SO2 (đktc, sản phẩm khử duy nhất). Tính khối lượng mỗi kim loại trong hỗn hợp A.
<3
\(n_{SO_2}=\dfrac{13,644}{22,4}=0,61\left(mol\right)\)
Đặt n Fe = x (mol) =>\(m_{Fe}=56x\)
Vì m Fe = mMg => \(n_{Mg}=\dfrac{56x}{24}=\dfrac{7}{3}x\)
nAl = y(mol)
=> 56x + 56x + 27y = 16,14 (1)
\(Fe\rightarrow Fe^{3+}+3e\) \(S^{+6}+2e\rightarrow S^{+4}\)
\(Mg\rightarrow Mg^{2+}+2e\)
\(Al\rightarrow Al^{3+}+3e\)
Bảo toàn e : 3x + \(\dfrac{7}{3}.2x\) + 3y = 0,61.2 (2)
Từ (1), (2) => x=0,12 ; y=0,1
=> mFe =mMg=0,12.56 = 6,72(g)
m Al = 0,1.27=2,7(g)
Đúng 2
Bình luận (0)
Bài 6. Hỗn hợp A gồm Fe, Mg, Al (khối lượng Mg bằng khối lượng Fe). Hòa tan hoàn toàn 16,14 gam hỗn hợp A trong dung dịch H2SO4 đặc, nóng dư thì thu được 13,664 lít SO2 (đktc, sản phẩm khử duy nhất). Tính khối lượng mỗi kim loại trong hỗn hợp A.
Gọi $n_{Fe} = a ; n_{Mg} = b; n_{Al} = c$
Ta có :
$24b = 56a(1)$
$56a + 24b + 27c = 16,14(2)$
$n_{SO_2} = 0,61(mol)$
Bảo toàn electron : $3n_{Fe} + 2n_{Mg} + 3n_{Al} = 2n_{SO_2}$
$\Rightarrow 3a + 2b + 3c = 0,61.2(3)$
Từ (1)(2)(3) suy ra a = 0,12 ; b = 0,28 ; c = 0,1
$m_{Fe} = m_{Mg} = 0,12.56 = 6,72(gam)$
$m_{Al} = 0,1.27 = 2,7(gam)$
Đúng 3
Bình luận (0)
Câu 1) Cho 11gam hỗn hợp Al,Fe phản ứng hoàn toàn với H2SO4đặc nóng dư thu đc 10,08 lít SO2 sản phẩm khử duy nhất ở điều kiện khuẩn và dung dịch Xa) Viết phương trình phản ứng xảy ra b) TÍnh % theo khối của mỗi kim loại trong hỗn hợpc) Tính khối lượng muối tạo thành trong dung dịch XCâu 2) cho 1,28 gam hỗn hợp Fe và Mg tác dụng vừa đủ với dung dịch H2SO4đặc, nóng thu đc 1,008 lít SO2 ở điều kiện chuẩn a) Viết phương trình phản ứng xảy ra b) Tính % theo khối của mỗi kim loại trong hỗn hợpc) Tính...
Đọc tiếp
Câu 1) Cho 11gam hỗn hợp Al,Fe phản ứng hoàn toàn với H2SO4đặc nóng dư thu đc 10,08 lít SO2 sản phẩm khử duy nhất ở điều kiện khuẩn và dung dịch X
a) Viết phương trình phản ứng xảy ra
b) TÍnh % theo khối của mỗi kim loại trong hỗn hợp
c) Tính khối lượng muối tạo thành trong dung dịch X
Câu 2) cho 1,28 gam hỗn hợp Fe và Mg tác dụng vừa đủ với dung dịch H2SO4đặc, nóng thu đc 1,008 lít SO2 ở điều kiện chuẩn
a) Viết phương trình phản ứng xảy ra
b) Tính % theo khối của mỗi kim loại trong hỗn hợp
c) Tính khối lượng dung dịch H2SO4 80% đã dùng
a)
nSO2=\(\dfrac{10,08}{22,4}\)= 0,45(mol)
2Al + 6H2SO4 --> Al2(SO4)3 + 6H2O +3SO2
x ---------------------------------------------> 3/2x
2Fe + 6H2SO4 --> Fe2(SO4)3 + 6H2O + 3SO2
y --------------------------------------------------> 3/2y
b) ta có hệ pt sau
\(\left\{{}\begin{matrix}27x+56y=11\\\dfrac{3}{2}x+\dfrac{3}{2}y=0,45\end{matrix}\right.\)
\(\left\{{}\begin{matrix}x=0,2\\y=0,1\end{matrix}\right.\)
%mAl = \(\dfrac{0,2.27}{11}.100\)= 49%
%mFe=\(49-100\) =51%
c) m Al2(SO4)3= 0,1.342=34,2 g
mFe2(SO4)3=0,05.400=20 g
Đúng 1
Bình luận (0)
Câu 1. Cho 11 g hỗn hợp Al, Fe phản ứng hoàn toàn với lượng dư dung dịch H,SO4 đặc nóng thu được 11,1555 L SO2 (sản phẩm khử duy nhất, ở đkc ) và dung dịch A. Tính % theo khối lượng của mỗi kim loại trong hỗn hợp.
Đúng 0
Bình luận (0)
Cho 9,2 gam hỗn hợp gồm Zn và Al phản ứng hoàn toàn với lượng dư dung dịch
H
2
S
O
4
đặc, nóng thu được 5,6 lít khí
S
O
2
(ở đktc, là sản phẩm khử duy nhất). Khối lượng Al có trong hỗn hợp là A. 2,7 gam. B. 5,4 gam C. 8,1 gam. D. 6,75 gam.
Đọc tiếp
Cho 9,2 gam hỗn hợp gồm Zn và Al phản ứng hoàn toàn với lượng dư dung dịch H 2 S O 4 đặc, nóng thu được 5,6 lít khí S O 2 (ở đktc, là sản phẩm khử duy nhất). Khối lượng Al có trong hỗn hợp là
A. 2,7 gam.
B. 5,4 gam
C. 8,1 gam.
D. 6,75 gam.
Chọn A
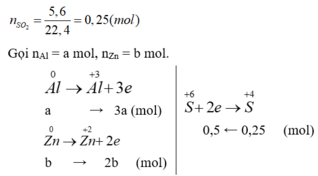
Ta có: m h h = 9 , 2 g → 27a + 65b = 9,2 (*)
Bảo toàn số mol electron có: 3a + 2b = 0,5 (**)
Giải (*), (**): a = b = 0,1 mol.
m A l = 0 , 1 . 27 = 2 , 7 g a m
Đúng 0
Bình luận (0)
Cho 9,2 gam hỗn hợp gồm Zn và Al phản ứng hoàn toàn với lượng dư dung dịch H2SO4 đặc, nóng thu được 5,6 lít khí SO2 (ở đktc, là sản phẩm khử duy nhất). Khối lượng Al có trong hỗn hợp là A. 2,7 gam B. 5,4 gam C. 8,1 gam D. 6,75 gam
Đọc tiếp
Cho 9,2 gam hỗn hợp gồm Zn và Al phản ứng hoàn toàn với lượng dư dung dịch H2SO4 đặc, nóng thu được 5,6 lít khí SO2 (ở đktc, là sản phẩm khử duy nhất). Khối lượng Al có trong hỗn hợp là
A. 2,7 gam
B. 5,4 gam
C. 8,1 gam
D. 6,75 gam
Cho 9,2 gam hỗn hợp gồm Zn và Al phản ứng hoàn toàn với lượng dư dung dịch H2SO4 đặc, nóng thu được 5,6 lít khí SO2 (ở đktc, là sản phẩm khử duy nhất). Khối lượng Al có trong hỗn hợp là:
A. 2,7 gam.
B. 5,4 gam.
C. 8,1 gam.
D. 6,75 gam.
Đáp án A.
Gọi nAl = a mol, nZn = b mol.

Ta có: 27a + 65b = 9,2 (*)
3a + 2b = 0,5 (**)
Giải (*), (**): a = b = 0,1 mol.
mAl = 0,1.27 = 2,7 gam
Đúng 0
Bình luận (0)



















