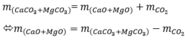cho 26,8g hh CaCO3, MgCO3 sau phản ứng thu được 13,6g hỗn hợp 2 oxit và khí CO2
a)viết các phương trình hóa học
b)tính % theo khối lượng của 2 muối trong hỗn hợp đầu
c)tính thể tích khí CO2 (đktc)

Những câu hỏi liên quan
1)Nung hoàn toàn 26,8g hỗn hợp CaCO3 và MgCO3.Sau khi phản ứng kết thúc thu được khí Co2 và 13,6g hỗn hợp rắn thể tích khí co2 thu được là A.6,72l B.6l C.3,36l D.10,08l2) nung 13,44g Fe với khí clo sau phản ứng kết thúc khối lượng sản phẩm thu được là 29,25 gam hiệu suất của phản ứng là A.80% B.75% C.96,8% D.90,8% 3) lượng clo thu đc khi điện phân 200g dd NaCl 35,1% sẽ tác dụng hết với bao nhiêu gam sắt?
Đọc tiếp
1)Nung hoàn toàn 26,8g hỗn hợp CaCO3 và MgCO3.Sau khi phản ứng kết thúc thu được khí Co2 và 13,6g hỗn hợp rắn thể tích khí co2 thu được là A.6,72l B.6l C.3,36l D.10,08l
2) nung 13,44g Fe với khí clo sau phản ứng kết thúc khối lượng sản phẩm thu được là 29,25 gam hiệu suất của phản ứng là A.80% B.75% C.96,8% D.90,8%
3) lượng clo thu đc khi điện phân 200g dd NaCl 35,1% sẽ tác dụng hết với bao nhiêu gam sắt?
3) lượng clo thu đc khi điện phân 200g dd NaCl 35,1% sẽ tác dụng hết với bao nhiêu gam sắt?
mNaCl=35,1%. 200= 70,2(g)
nNaCl= 70,2/58,5=1,2(mol)
PTHH: 2 NaCl -đpnc-> 2 Na + Cl2
1,2_____________________0,6(mol)
2 Fe + 3 Cl2 -to-> 2 FeCl3
0,4___0,6(mol)
nCl2=nNaCl/2= 1,2/2=0,6(mol)
nFe=2/3. nCl2=2/3 . 0,6=0,4(mol)
=> mFe=0,4. 56=22,4(g)
Đúng 2
Bình luận (0)
1)Nung hoàn toàn 26,8g hỗn hợp CaCO3 và MgCO3.Sau khi phản ứng kết thúc thu được khí Co2 và 13,6g hỗn hợp rắn thể tích khí co2 thu được là A.6,72l B.6l C.3,36l D.10,08l
---
Đặt: nCaCO3=x(mol); nMgCO3=y(mol)
PTHH: CaCO3 -to-> CaO + CO2
x________________x_____x(mol)
MgCO3 -to-> MgO + CO2
y_________y______y(mol)
Ta có hpt: \(\left\{{}\begin{matrix}100x+84y=26,8\\56x+40y=13,6\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
=> nCO2= x+y=0,1+0,2=0,3(mol)
=> V(CO2,đktc)=0,3.22,4=6,72(l)
=> CHỌN A
Đúng 2
Bình luận (0)
2) nung 13,44g Fe với khí clo sau phản ứng kết thúc khối lượng sản phẩm thu được là 29,25 gam hiệu suất của phản ứng là A.80% B.75% C.96,8% D.90,8%
---
nFe= 13,44/56=0,24(mol)
PTHH: 2 Fe + 3 Cl2 -to-> 2 FeCl3
nFeCl3(TT)=29,25/162,5=0,18(mol)
Mà theo PTHH: nFeCl3(LT)= nFe=0,24(mol)
=> H= (0,18/0,24).100=75%
=> CHỌN B
Đúng 2
Bình luận (0)
đang gấp cho mình xin dáp án
Đốt cháy hoàn toàn 3,6 g hỗn hợp metan và etilen thu được 5,6 l khí CO2 điều kiện tiêu chuẩn
A viết phương trình hóa học
b Tính khối lượng của từng chất trong hỗn hợp ban đầu
c Tính thể tích không khí điều kiện tiêu chuẩn cần đốt một lượng hiđrocacbon trên biết O2 chiếm 20% thể tích không khí
\(n_{CO_2}=\dfrac{5,6}{22,4}=0,25mol\)
\(\left\{{}\begin{matrix}CH_4:x\left(mol\right)\\C_2H_4:y\left(mol\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}16x+28y=3,6\\BTC:x+2y=n_{CO_2}=0,25\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,05mol\\y=0,1mol\end{matrix}\right.\)
a)\(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
b)\(m_{CH_4}=0,05\cdot16=0,8g\)
\(m_{C_2H_4}=0,1\cdot28=2,8g\)
c)\(\Sigma n_{O_2}=2n_{CH_4}+3n_{C_2H_4}=2\cdot0,05+3\cdot0,1=0,4mol\)
\(\Rightarrow V_{O_2}=0,4\cdot22,4=8,96l\)
\(\Rightarrow V_{kk}=5V_{O_2}=5\cdot8,96=44,8l\)
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn 14,6 gam một hỗn hợp gồm kẽm và kẽm oxit bằng dung dịch axit HCL thì thu được 2,24l khí hidro
a, Viết các phương trình hóa học của các phản ứng xảy ra b, Tính khối lượng của kẽm và kẽm oxit trong hỗn hợp ban đầu
c, tính thể tích axit HCL tham gia phản ứng
a)
$Zn + 2HCl \to ZnCl_2 + H_2$
$ZnO + 2HCl \to ZnCl_2 + H_2O$
b)
$n_{Zn} = n_{H_2} = \dfrac{2,24}{22,4} = 0,1(mol)$
$m_{Zn} = 0,1.65 = 6,5(gam)$
$m_{ZnO} = 14,6 - 6,5 = 8,1(gam)$
c)
$n_{ZnO} = \dfrac{8,1}{81} = 0,1(mol)$
$n_{HCl} = 2n_{Zn} + 2n_{ZnO} = 0,4(mol)$
$\Rightarrow V_{dd\ HCl} = \dfrac{0,4}{C_{M_{HCl}}}$
Đúng 2
Bình luận (0)
Bài 3: Nung hỗn hợp 2 muối CaCO3 và MgCO3 thu được 76 gam hỗn hợp 2 oxit (CaO và MgO) và 3,36 lít khí CO2 ( ở đktc). Tính khối lượng hỗn hợp muối ban đầu?
\(m_{CO_2}=\dfrac{3,36}{22,4}.44=6,6(g)\)
Áp dụng định luật BTKL: \(m_{\text{hh muối}}=m_{\text{hh oxit}}+m_{CO_2}=76+6,6=82,6(g)\)
Đúng 3
Bình luận (0)
Đốt cháy hỗn hợp khí gồm CO và H2 cần dùng 3,36 lít khí O2 ở đktc và thu đc 1,8 gam nước ngưng tụ
a) Viết PT phản ứng xảy ra
b) Tính thể tích mỗi khí có trong hỗn hợp ban đầu
c) Tính khối lượng khí CO2 đc tạo thành theo 2 phương pháp khác nhau
\(a)\\ 2CO + O_2 \xrightarrow{t^o} 2CO\\ 2H_2 + O_2 \xrightarrow{t^o} 2H_2O\\ n_{H_2} = n_{H_2O} = \dfrac{1,8}{18} = 0,1(mol)\\ \)
Theo PTHH :
\(2n_{O_2} = n_{CO} + n_{H_2}\\ \Leftrightarrow 2.\dfrac{3,36}{22,4} = n_{CO} + 0,1\\ \Leftrightarrow n_{CO} = 0,2(mol)\\ \%V_{H_2} = \dfrac{0,1}{0,1+ 0,2}.100\% = 33,33\%\\ \%V_{CO} = 100\%-33,33\% = 66,67\%\\ c) Cách\ 1 :\\ n_{CO_2} = n_{CO} = 0,2(mol)\\ m_{CO_2} = 0,2.44 = 8,8(gam)\\ Cách\ 2 : \\ m_{hh} = m_{CO} + m_{H_2} = 0,2.28 + 0,1.2 = 5,8(gam) \)
Bảo toàn khối lượng :
\(m_{hh} + m_{O_2} = m_{H_2O} + m_{CO_2}\\ \Rightarrow m_{CO_2} = 5,8 + 0,15.32 - 1,8 = 8,8(gam)\)
Đúng 2
Bình luận (0)
Nung hỗn hợp X gồm
C
a
C
O
3
và
M
g
C
O
3
theo phản ứng :
C
a
C
O
3
→
t
°
C
a
O
+
C
O
2
M
g
C
O
3
→
t
°
M
g...
Đọc tiếp
Nung hỗn hợp X gồm C a C O 3 và M g C O 3 theo phản ứng :
C a C O 3 → t ° C a O + C O 2
M g C O 3 → t ° M g O + C O 2
Nếu đem nung 31,8 gam hỗn hợp X thì thu được 7,84 lít C O 2 (đktc). Tính khối lượng của hỗn hợp của oxit thu được.
Nung nóng m gam hỗn hợp CaCO 3 và MgCO 3 đến phản ứng hoàn toàn, sau phản ứng thu được 2,72 gam hỗn hợp 2 oxit và 1344 ml khí CO 2 (ở đktc). Hãy tính giá trị của m.
Phương trình hóa học của phản ứng:
CaCO 3 → t ° CaO + CO 2
MgCO 3 → t ° MgO + CO 2
n CaCO 3 = x; n MgCO 3 = y
n CO 2 = 1344/22400 = 0,06
Ta có hệ phương trình
56x + 40y = 2,72
x + y = 0,06
Giải ra, ta có: x = 0,02(mol); y = 0,04(mol)
m = m CaCO 3 + m MgCO 3 = 0,02 x 100 + 0,04 x 84 = 5,36g
Đúng 0
Bình luận (0)
Hòa tan 450g canxi cacbonat CaCO3 vào dung dịch axit clohiđric, phản ứng xảy ra theo phương trình:
CaCO3 + HCl - - - > CaCl2 + H2O + CO2
a. Lập phương trình hóa học
b. Tính khối lượng axit clohiđric tham gia phản ứng
c. Tính thể tích khí CO2 thoát ra ở đktc
a) CaCO3 + 2HCl → CaCl2 + H2O + CO2
b) nCaCO3 = \(\dfrac{450}{100}\)=4,5 mol
=> nHCl phản ứng = 4,5.2 = 9mol
<=> mHCl = 9 . 36,5 = 328,5 gam
c) nCO2 = nCaCO3 = 4,5 mol => V CO2 = 4,5 . 22,4 = 100,8 lít
Đúng 1
Bình luận (0)
Hòa tan 6 gam hỗn hợp hai muối MgCO3 và MgSO4 bằng dung dịch H2SO4 vừa đủ thì thu được 0,672 lít khí CO2 (đktc).
a.Viết phương trình hóa học xảy ra.
b.Tính thành phần phần trăm theo khối lượng của mỗi muối trong hỗn hợp ban đầu.
C .Tính khối lượng muối MgSO4 thu được sau phản ứng.
Ta có: \(n_{CO_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
a. PTHH:
\(MgCO_3+H_2SO_4--->MgSO_4+H_2O+CO_2\)
\(MgSO_4+H_2SO_4--\times-->\)
b. Theo PT: \(n_{MgCO_3}=n_{CO_2}=0,03\left(mol\right)\)
\(\Rightarrow m_{MgCO_3}=0,03.84=2,52\left(g\right)\)
\(\Rightarrow m_{MgSO_4}=6-2,52=3,48\left(g\right)\)
\(\Rightarrow\%_{m_{MgCO_3}}=\dfrac{2,52}{6}.100\%=42\%\)
\(\%_{m_{MgSO_4}}=100\%-42\%=58\%\)
c. Theo PT: \(n_{MgSO_4}=n_{CO_2}=0,03\left(mol\right)\)
\(\Rightarrow m_{MgSO_4}=0,03.120=3,6\left(g\right)\)
\(\Rightarrow m_{MgSO_{4_{thu.được.sau.phản.ứng}}}=3,6+3,48=7,08\left(g\right)\)
Đúng 1
Bình luận (0)