hòa tan 84,5 gam oleum X vào nước thu được dung dịch Y.Để trung hòa Y cần 1 lít dung dịch NaOH 2M. phần trăm khối lượng lưu huỳnh trong X là ?
Cho 0,015 mol một loại hợp chất oleum vào nước thu được 200ml dung dịch X. Để trung hòa 100 ml dung dịch X cần dùng 200 ml dung dịch NaOH 0,15M. Thành phần phần trăm về khối lượng của nguyên tố lưu huỳnh trong oleum trên là
A. 37,86%
B. 35,96%
C. 23,97%
D. 32,655%
Cho 0,015 mol một loại hợp chất oleum vào nước thu được 200 ml dung dịch X. Để trung hòa 100 ml dung dịch X cần dùng 200 ml dung dịch NaOH 0,15M. Phần trăm về khối lượng của nguyên tố lưu huỳnh trong oleum trên gần nhất với giá trị nào sau đây?
A.35,96%.
B.32,65%.
C.37,86%.
D.23,97%.
Cho 0,1 mol một loại hợp chất oleum vào nước thu được 2,0 lít dung dịch X. Để trung hoà 1 lít dung dịch X cần dùng 400 ml dung dịch KOH 1M. Phần trăm về khối lượng của nguyên tố lưu huỳnh trong oleum trên là
A. 35,96%.
B. 37,21%.
C. 37,87%.
D. 38,28%.
Hòa tan 23,1 gam hỗn hợp X gồm K và BaO vào 177,1 gam nước thì thu được 2,24 lít khí (đktc) và dung dịch Y
a) Tính phần trăm khối lượng mỗi chất trong X.
b) Tính nồng độ phần trăm của dung dịch Y.
c) Để trung hòa vừa đủ dung dịch Y cần V ml dung dịch HCl 0,5M. Tính V
a)
$2K + 2H_2O \to 2KOH + H_2$
$BaO + H_2O \to Ba(OH)_2$
Theo PTHH :
$n_K = 2n_{H_2} = 0,2(mol)$
$\%m_K = \dfrac{0,2.39}{23,1}.100\% = 33,77\%$
$\%m_{BaO} = 100\%- 33,77\% = 66,23\%$
b)
$n_{BaO} = \dfrac{23,1 - 0,2.39}{153} = 0,1(mol)$
$m_{dd} = 23,1 + 177,1 - 0,1.2 = 200(gam)$
$C\%_{KOH} = \dfrac{0,2.56}{200}.100\% = 5,6\%$
$C\%_{Ba(OH)_2} = \dfrac{0,1.171}{200}.100\% = 8,55\%$
c)
$KOH + HCl \to KCl + H_2O$
$Ba(OH)_2 + 2HCl \to BaCl_2 + 2H_2O$
$n_{HCl} = 2n_{Ba(OH)_2} + n_{KOH} = 0,4(mol)$
$V = \dfrac{0,4}{0,5} = 0,8(lít) = 800(ml)$
hòa tan 8,6 gam oleum X vào nước được dung dịch Y . Để trung hòa dung dịch Y cần 200 ml dung dịch NaOH 1M . Công thức của oleum X là gì ?
Gọi CT oleum là H2SO4.nSO3 a mol
Hòa tan vào H2O tổng nH2SO4=a+an mol
nNaOH cần=0,2 mol
SO3 + H2O =>H2SO4
an mol =>an mol
H2SO4 +2 NaOH =>Na2SO4 + 2H2O
0,1 mol<=0,2 mol
=>a+an=0,1
Mà m oleum=8,6=a(98+80n)
Giải hpt có a=1/30 và an=1/15
=>n=2
CT oleum H2SO4.2SO3
Cho 0,015 mol một loại hợp chất oleum vào nước thu được 200 ml dung dịch X. Để trung hoà 100 ml dung dịch X cần dùng 200 ml dung dịch NaOH 0,15M. Phần trăm về khối lượng của nguyên tố lưu huỳnh trong oleum trên gần với giá trị nào nhất sau đây?
A. 35,96%.
B. 32,65%.
C. 37,86%.
D. 23,97%.
Đáp án A
Số mol NaOH là: n NaOH = 0 , 2 . 0 , 15 = 0 , 03 mol
Dung dịch X chính là dung dịch H2SO4
Trung hoà 100 ml dung dịch X:
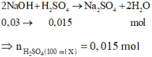
Số mol H2SO4 trong 200 ml dung dịch X là:
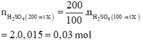
Đặt công thức của oleum là H2SO4.nSO3
Phương trình hoá học:
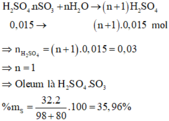
Cho 1,69 gam một oleum có công thức H2SO4.3SO3 vào nước dư thu được dung dịch X. Để trung hòa dung dịch X cần dùng vừa đủ V lít dung dịch NaOH 2M. Giá trị của V là:
A. 20
B. 40
C. 80
D. 10
Đáp án : A
nOleum = 0,005 mol => nH2SO4 sau hòa tan = nS(Oleum) = 4nOleum = 0,02 mol
=> nNaOH = 2V = 2nH2SO4 = 0,04 mol => V = 0,02 lit = 20 ml
Hòa tan 3,38 gam oleum A vào lượng nước dư ta được dung dịch A. Để trung hòa 1/20 lượng dung dịch A cần dùng 40 ml dung dịch NaOH 0,1M. Tìm công thức của oleum
CTPT oleum: H2SO4.nSO3 có x (mol)
H2SO4.nSO3 + nH2O → (n + 1)H2SO4
x → x(n + 1)
H2SO4 + 2NaOH → Na2SO4 + 2H2O
x(n + 1)→ 2x(n + 1)
=> (98 + 80n)x = 3,38 và 2x (n + 1) = 0,08
=> x = 0,01 và nx = 0,03
=> n = 3
Suy ra CTPT oleum: H2SO4.3SO3
Bài 7: Hòa tan hết 12,4 gam Na2O vào nước, thu được 200 gam dung dịch X. a) Tính nồng độ phần trăm của dung dịch X. b) Hấp thụ toàn bộ V lít khí SO2 (ở 25oC và 1 bar) vào lượng dung dịch X ở trên, thu được dung dịch Y chỉ chứa muối trung hòa. - Tính giá trị của V. - Tính nồng độ phần trăm của dung dịch Y.