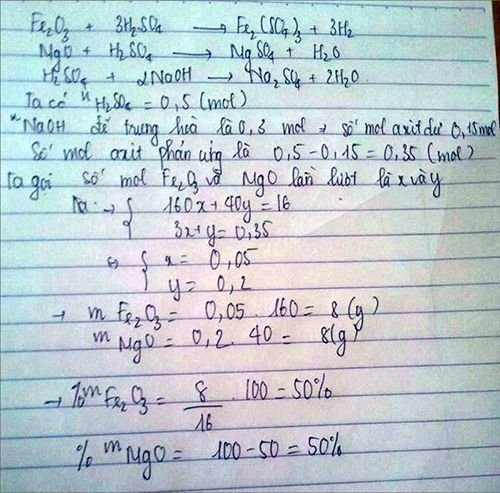LẤY 6 g hh MgO và Fe2O3 tan hết trong 0,5 l dD H2SO4 1M sau phản ứng để trung hòa axít còn dư bằng 50 g dd NAOH 24% tính khối lượng phần trăm mỗi axít trong hh ban đầu

Những câu hỏi liên quan
Lấy 16g hh MgO và Fe2O3 tan hết trong 0,5 l dd H2SO4 1M sau pu để trung hoà axit còn dư bằng 50g dd NaOH tính % klg mỗi axit trong hh
Lấy 16g hh MgO và Fe2O3 tan hết trong 0,5 l dd H2SO4 1M sau pu để trung hoà axit còn dư bằng 50g dd NaOH tính % klg mỗi axit trong hh
16g hh gồm MgO và Fe2O3 hòa tan hết trong 0,5l dd axit sunfuric 1M. Sau pư để trung hòa lượng axit còn dư cần 50g dd NaOH 24% Tính % lượng oxit trong hh
cho 16 g hỗn hợp gồm MgO và Fe2O3 tan hết trong 0,5 lít dung dịch H2SO4 sau phản ứng, trung hòa axit còn dư bằng 50 gam dung dịch NaOH 24% . Tính phần trăm khối lượng mỗi oxit trong hỗn hợp ban đầu?
Đề của bạn còn thiếu thì phải, bạn kiểm tra lại nha
Đúng 0
Bình luận (0)
Cho 16 g hỗn hợp MgO , Fe2O3 tan hết trong 0,5 l dd H2SO4 1M .Sau phản ứng trung hòa axit còn dư bằng 50g NaOH 24% .Tính % mỗi axit
\(PTHH:2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
\(n_{NaOH}=\frac{50.24}{100.40}=0,3\left(mol\right)\)
\(PTHH:MgO+H_2SO_4\rightarrow MgSO_4+H_2O\)
\(PTHH:Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
\(n_{MgO}=x;n_{Fe_2O_3}=y\\ hpt:\left\{{}\begin{matrix}40x+160y=16\\x+3y=0,5.1-\frac{0,3}{2}\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,05\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{MgO}=\frac{0,2.40}{16}.100\%=50\%\\\%m_{Fe_2O_3}=100-50=50\%\end{matrix}\right.\)
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Cho 26,7 g hh A gồm Mg, Fe, Al tan hết trong dd H2SO4 lấy dư .sau phản ứng xong thu được 17,92 lít khí( ĐKTC). Biết thể tích khí thoát ra do Sắt hòa tan gấp 2 lần thể tích khí tạo ra khi Magie tan
a) Tính thành phần phần trăm khối lượng mỗi chất trong hh A
b) Tính khối lượng H2SO4
b) Tính khối lượng H2SO4 dư sau pư, biết H2SO4 đã lấy dư so với lượng pư là 10%
Hòa tan hoàn toàn 12,8g hh A gồm Fe và FeO trong 250 ml dd H2SO4 1M loãng (lấy dư) thu được 2,24l H2 (đktc) và dung dịch B.
a. Tính phần trăm khối lượng mỗi chất trong hh A .
b, Trung hòa dung dịch B cần dùng V ml dung dịch NaOH 1M. Tính giá trị V
a, gọi a= nFe
b= nFeO
=> 56a + 72b= 12,8 (1)
Fe +H2SO4 -> FeSO4 +H2
a b b a
FeO +H2SO4 -> FeSO4 +H2O
b b b
a=nH2 = 2,24/22,4= 0,1 mol
từ (1) => b= 0,1
mFe= 56.0,1=5,6(g)
m FeO = 72.0,1= 7,2(g)
b, nH2SO4 (bđ) = 0,25 mol
nH2SO4 pứ = a+b =0,2 mol
=> nH2SO4 dư = 0,25-0,2=0,05 mol
2NaOH +H2SO4 -> Na2SO4 +2H2O
0,1 0,05
V(NaOH)= 0,1/ 1= 0,1 lit =100ml
Đúng 1
Bình luận (1)
E tham khảo! Anh nãy làm tại câu hỏi bấm lộn xóa

Đúng 2
Bình luận (0)
Hòa tan 13,2g hh bột Fe,FeO,và Fe2O3 vào dd HCl.sau phản ứng thu được chất răn A là kim loại ; 0,56l khí B và một dd C.Cho dd C tác dụng hết với dd NaOH dư thu được kết tủa D.Nung kết tủa D trong không khí đến khối lượng không đổi thu được 12g chất rắn.Mặt khác,nếu lấy khối lượng chất rắn A đúng bằng khối lượng của nó đem hòa tan hoàn trong H2SO4 đặc,nóng dư thu được 3,36l khí mùi xốc(đktc).tính %FeO trong hh.
Đọc tiếp
Hòa tan 13,2g hh bột Fe,FeO,và Fe2O3 vào dd HCl.sau phản ứng thu được chất răn A là kim loại ; 0,56l khí B và một dd C.Cho dd C tác dụng hết với dd NaOH dư thu được kết tủa D.Nung kết tủa D trong không khí đến khối lượng không đổi thu được 12g chất rắn.Mặt khác,nếu lấy khối lượng chất rắn A đúng bằng khối lượng của nó đem hòa tan hoàn trong H2SO4 đặc,nóng dư thu được 3,36l khí mùi xốc(đktc).tính %FeO trong hh.
Cho 200g dd H2SO4 9.8% tác dụng với kim loại kẽm. Viết PTHH và tính? a, Khối lượng kém tham gia phản ứng? Khối lượng muối tại thành? Và thể tích khí H2 (đktc) b, Trung hòa lượng axít H2SO4 trên bằng 200ml dd NaOH 3M. Sau phản ứng chất nào còn dư? Dư bao nhiêu